абдоминалгия что это такое
Абдоминальный болевой синдром: этиология, патогенез и вопросы терапии
По механизму возникновения боли в брюшной полости подразделяются на висцеральные, паристальные (соматические), отраженные (иррадиирующие) и психогенные Каковы причины абдоминального болевого синдрома? В чем заключается терапия абдоминального болевог
По механизму возникновения боли в брюшной полости подразделяются на висцеральные, паристальные (соматические), отраженные (иррадиирующие) и психогенные
Каковы причины абдоминального болевого синдрома?
В чем заключается терапия абдоминального болевого синдрома?
Абдоминальный болевой синдром является ведущим в клинике большинства заболеваний органов пищеварения. Боль — это спонтанное субъективное ощущение, возникающее вследствие поступления в центральную нервную систему патологических импульсов с периферии (в отличие от болезненности, которая определяется при обследовании, например, при пальпации). Тип боли, ее характер не всегда зависят от интенсивности инициальных стимулов. Органы брюшной полости обычно нечувствительны ко многим патологическим стимулам, которые при воздействии на кожу вызывают сильную боль. Разрыв, разрез или раздавливание внутренних органов не сопровождаются заметными ощущениями. В то же время растяжение и напряжение стенки полого органа раздражают болевые рецепторы. Так, натяжение брюшины (опухоли), растяжение полого органа (например, желчная колика) или чрезмерное сокращение мышц вызывают абдоминальные боли. Болевые рецепторы полых органов брюшной полости (пищевод, желудок, кишечник, желчный пузырь, желчные и панкреатические протоки) локализуются в мышечной оболочке их стенок. Аналогичные рецепторы имеются в капсуле паренхиматозных органов, таких как печень, почки, селезенка, и их растяжение также сопровождается болью. Брыжейка и париетальная брюшина чувствительны к болевым стимулам, в то время как висцеральная брюшина и большой сальник лишены болевой чувствительности.
Абдоминальные боли подразделяются на острые, которые развиваются, как правило, быстро или, реже, постепенно и имеют небольшую продолжительность (минуты, редко несколько часов), а также хронические, для которых характерно постепенное нарастание. Эти боли сохраняются или рецидивируют на протяжении недель и месяцев. Этиологическая классификация абдоминальных болей представлена в табл. 1.
По механизму возникновения боли в брюшной полости подразделяются на висцеральные, париетальные (соматические), отраженные (иррадиирующие) и психогенные.
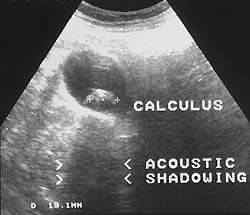 |
| Рисунок 1. Причиной абдоминальной боли может быть калькулезный холецистит (УЗИ) |
Висцеральная боль возникает при наличии патологических стимулов во внутренних органах и проводится симпатическими волокнами. Основными импульсами для ее возникновения являются внезапное повышение давления в полом органе и растяжение его стенки (наиболее частая причина), растяжение капсулы паренхиматозных органов, натяжение брыжейки, сосудистые нарушения.
Соматическая боль обусловлена наличием патологических процессов в париетальной брюшине и тканях, имеющих окончания чувствительных спинномозговых нервов.
Основными импульсами для ее возникновения являются повреждение брюшной стенки и брюшины.
Дифференциально-диагностические признаки висцеральной и соматической боли представлены в табл. 2.
Иррадиирующая боль локализуется в различных областях, удаленных от патологического очага. Она возникает в тех случаях, если импульс висцеральной боли чрезмерно интенсивен (например, прохождение камня) или при анатомическом повреждении органа (например, ущемление кишки). Иррадиирующая боль передается на участки поверхности тела, которые имеют общую корешковую иннервацию с пораженным органом брюшной области. Так, например, при повышении давления в кишечнике вначале возникает висцеральная боль, которая затем иррадиируют в спину, при билиарной колике — в спину, в правую лопатку или плечо.
Психогенная боль возникает при отсутствии периферического воздействия либо когда последнее играет роль пускового или предрасполагающего фактора. Особая роль в ее возникновении принадлежит депрессии. Последняя часто протекает скрыто и не осознается самими пациентами. Тесная связь депрессии с хронической абдоминальной болью объясняется общими биохимическими процессами и, в первую очередь, недостаточностью моноаминергических (серотонинергических) механизмов. Это подтверждается высокой эффективностью антидепрессантов, особенно ингибиторов обратного захвата серотонина, в лечении болевого синдрома. Характер психогенных болей определяется особенностями личности, влиянием эмоциональных, когнитивных, социальных факторов, психологической стабильностью больного и его прошлым «болевым опытом». Основными признаками данных болей являются их длительность, монотонность, диффузный характер и сочетание с другими локализациями (головная боль, боль в спине, во всем теле). Нередко психогенные боли могут сочетаться с другими, указанными выше типами болей и оставаться после их купирования, существенно трансформируя их характер, что необходимо учитывать при терапии.
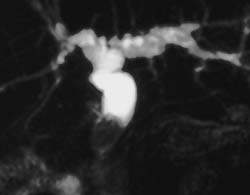 |
| Рисунок 2. Камень в общем желчном протоке у пациента после холецистэктомии (МРТ) |
Одной из разновидностей болей центрального генеза является абдоминальная мигрень. Последняя чаще встречается в молодом возрасте, носит интенсивный разлитой характер, но может быть локальной в параумбиликальной области. Характерны сопутствующие тошнота, рвота, понос и вегетативные расстройства (побледнение и похолодание конечностей, нарушения ритма сердца, артериального давления и др.), а также мигренозная цефалгия и характерные для нее провоцирующие и сопровождающие факторы. Во время пароксизма отмечается увеличение скорости линейного кровотока в брюшной аорте. Наиболее важными механизмами контроля болевого синдрома являются эндогенные опиатные системы. Опиатные рецепторы локализуются в окончаниях чувствительных нервов, в нейронах спинного мозга, в стволовых ядрах, в таламусе и лимбических структурах головного мозга. Связь данных рецепторов с рядом нейропептидов, таких как эндорфины и энкефалины, обусловливает морфиноподобный эффект. Опиатная система работает по следующей схеме: активация чувствительных окончаний приводит к выделению субстанции Р, что вызывает появление периферических восходящих и центральных нисходящих ноцицептивных (болевых) импульсов. Последние активизируют выработку эндорфинов и энкефалинов, которые блокируют выделение субстанции Р и снижают болевые ощущения.
Существенное значение в формировании болевого синдрома имеют серотонин и норадреналин. В структурах мозга находится большое количество серотонинергических и норадренергических рецепторов, а в состав нисходящих антиноцицептивных (противоболевых) структур входят серотонинергические и норадренергические волокна. Уменьшение уровня серотонина приводит к снижению болевого порога и усилению болей. Норадреналин опосредует увеличение активности антиноцицептивных систем.
Наличие болевого абдоминального синдрома требует углубленного обследования больного для уточнения механизмов его развития и выбора тактики лечения. Подавляющему большинству больных с наличием соматических болей, как правило, необходимо хирургическое лечение. Висцеральные боли, возникающие у больных как с наличием органических поражений органов пищеварения, так и без них, являются следствием нарушения, в первую очередь, моторной функции последних. В результате в полых органах повышается давление и/или наблюдается растяжение его стенки, и возникают условия для формирования восходящих ноцицептивных импульсов.
В регуляции транспорта ионов кальция участвуют ряд нейрогенных медиаторов: ацетилхолин, катехоламины (норадреналин), серотонин, холецистокинин, мотилин и др. Связывание ацетилхолина с М-холинорецепторами способствует открытию натриевых каналов и вхождению ионов натрия в клетку. Последнее снижает электрический потенциал клеточной мембраны (фаза деполяризации) и приводит к открытию кальциевых каналов, через которые ионы кальция поступают в клетку, вызывая мышечное сокращение.
Серотонин оказывает существенное влияние на моторику желудочно-кишечного тракта, активируя ряд рецепторов, локализирующихся на эффекторных клетках. Выделяют несколько подтипов рецепторов (5-МТ1-4), однако наиболее изучены 5-МТ3 и 5-МТ4. Связывание серотонина с 5-МТ3 способствует расслаблению, а с 5-МТ4 — сокращению мышечного волокна. В то же время механизмы действия серотонина на мышечные волокна желудочно-кишечного тракта до конца не установлены. Имеются лишь предположения о вовлечении в эти процессы ацетилхолина.
Тахикинины, в состав которых входят три типа пептидов (субстанция Р, нейрокинин А и В), связываясь с соответствующими рецепторами миоцитов, повышают их моторную активность не только в результате прямой активации, но и вследствие выделения ацетилхолина. Определенную роль в регуляции моторной функции кишечника играют эндогенные опиаты. При связывании их с μ- и δ-опиоидными рецепторами миоцитов происходит стимуляция, а с κ-рецепторами — замедление моторики пищеварительного тракта.
Основные направления купирования болевого абдоминального синдрома включают: а) этиологическое и патогенетическое лечение основного заболевания; б) нормализацию моторных расстройств; в) снижение висцеральной чувствительности; г) коррекцию механизмов восприятия болей.
Нарушения двигательной функции органов желудочно-кишечного тракта играют значительную роль в формировании не только болевого синдрома, но и большинства диспепсических расстройств (чувство переполнения в желудке, отрыжка, изжога, тошнота, рвота, метеоризм, поносы, запоры). Большинство из указанных выше симптомов могут иметь место как при гипокинетическом, так и при гиперкинетическом типе дискинезии, и только углубленное исследование позволяет уточнить их характер и выбрать адекватную терапию.
Одним из наиболее частых функциональных нарушений, в том числе и с наличием органической патологии органов пищеварения, является спастическая (гиперкинетическая) дискинезия. Так, при спастической дискинезии любого отдела пищеварительного тракта наблюдается повышение внутрипросветного давления и нарушение продвижения содержимого по полому органу, что создает предпосылки для возникновения боли. При этом скорость нарастания давления в органе пропорциональна интенсивности боли.
Спастическая дискинезия мышечной оболочки стенки полого органа или сфинктеров представляет собой наиболее частый механизм развития болевого синдрома при эзофагоспазме, дисфункции сфинктера Одди и пузырного протока, синдроме раздраженного кишечника.
В настоящее время для купирования болевого синдрома в комплексном лечении вышеуказанных заболеваний используются релаксанты гладкой мускулатуры, которые включают несколько групп препаратов. Антихолинергические средства снижают концентрацию интрацеллюлярных ионов кальция, что приводит к мышечной релаксации. Важно отметить, что степень релаксации находится в прямой зависимости от предшествующего тонуса парасимпатической нервной системы. Последнее обстоятельство определяет существенные различия индивидуальной эффективности препаратов данной группы. В качестве спазмолитиков используют как неселективные (препараты красавки, метацин, платифиллин, бускопан и др.), так и селективные М1-холиноблокаторы (гастроцепин и др.). Однако довольно низкая эффективность и широкий спектр побочных эффектов ограничивают их применение для купирования болевого синдрома у значительной части больных.
Механизм действия миотропных спазмолитиков в конечном итоге сводится к накоплению в клетке цАМФ и уменьшению концентрации ионов кальция, что тормозит соединение актина с миозином. Эти эффекты могут достигаться ингибированием фосфодиэстеразы, или активацией аденилатциклазы, или блокадой аденозиновых рецепторов, либо их комбинацией. Основными представителями данной группы препаратов являются дротаверин (но-шпа, но-шпа форте, спазмол), бенциклан (галидор), отилония бромида (спазмомен), метеоспазмил и др. При использовании миогенных спазмолитиков, так же как и М-холиноблокаторов, необходимо учитывать существенные индивидуальные различия их эффективности, отсутствие селективности эффектов (действуют практически на всю гладкую мускулатуру, включая мочевыделительную систему, кровеносные сосуды и др.), развитие гипомоторной дискинезии и гипотонии сфинктерного аппарата пищеварительного тракта, особенно при длительном применении. Данные препараты используются кратковременно (от однократного приема до двух-трех недель) для купирования спазма, а следовательно, болевого синдрома.
В ряду миотропных спазмолитиков следует отметить препарат мебеверин (дюспатолин), механизм действия которого сводится к блокаде быстрых натриевых каналов клеточной мембраны миоцита, что нарушает поступление натрия в клетку, замедляет процессы деполяризации и блокирует вход кальция в клетку через медленные каналы. В результате прекращается фосфорилирование миозина и отсутствует сокращение мышечного волокна. Известно также, что выход ионов кальция из внутриклеточных депо в результате активации α1-адренорецепторов приводит к открытию калиевых каналов, выходу ионов калия из клетки, гиперполяризации и отсутствию мышечного сокращения, что может становиться в течение длительного времени причиной мышечной гипотонии. В отличие от других миотропных спазмолитиков мебеверин препятствует пополнению внутриклеточных кальциевых депо, что в конечном итоге приводит лишь к кратковременному выходу ионов калия из клетки и ее гипополяризации. Последняя предупреждает развитие постоянного расслабления или гипотонии мышечной клетки. Следовательно, назначение мебеверина (дюспатолина) приводит только к снятию спазма без развития гипотонии гладкой мускулатуры, т. е. не нарушает моторики желудочно-кишечного тракта. Препарат оказался эффективным для купирования абдоминальных болей и дискомфорта, нарушений стула, обусловленных синдромом раздраженного кишечника, а также возникающих на фоне органических заболеваний.
Среди миотропных спазмолитиков также обращает на себя внимание препарат гимекромон (одестон). Одестон (7-гидрокси-4-метилкумарин) оказывает избирательное спазмолитическое действие на сфинктер Одди и сфинктер желчного пузыря, обеспечивает отток желчи в двенадцатиперстную кишку, снижает давление в билиарной системе и, как следствие, купирует билиарный болевой синдром. Одестон не обладает прямым желчегонным действием, но облегчает приток желчи в пищеварительный тракт, тем самым усиливая энтерогепатическую рециркуляцию желчных кислот, которые участвуют в первой фазе образования желчи. Преимущество одестона по сравнению с другими спазмолитиками заключается в том, что он практически не оказывает влияния на другие гладкие мышцы, в частности, кровеносной системы и кишечной мускулатуры.
Чрезвычайно перспективным направлением в лечении моторных расстройств является использование селективных блокаторов кальциевых каналов. В настоящее время из этой группы широкое распространение получил пинавериум бромид (дицетел). Дицетел блокирует потенциалзависимые кальциевые каналы миоцитов кишечника, резко снижает поступление в клетку экстрацеллюлярных ионов кальция и тем самым предотвращает мышечное сокращение. К числу достоинств дицетела относятся местное (внутрикишечное) действие препарата, тканевая селективность, отсутствие побочных, в т. ч. и кардиоваскулярных эффектов. Препарат можно применять в течение длительного времени, не опасаясь развития гипотонии кишечника. Клинические исследования показали высокую эффективность дицетела в лечении синдрома раздраженного кишечника и других заболеваний, при которых наблюдается спастическая дискинезия толстой кишки.
В купировании болевого синдрома особая роль отводится препаратам, влияющим на висцеральную чувствительность и механизмы восприятия болей. Это касается, в первую очередь, больных с функциональными заболеваниями желудочно-кишечного тракта (функциональная диспепсия, синдром раздраженного кишечника, функциональные абдоминальные боли и др.) и психогенными абдоминальными болями.
В настоящее время широко обсуждается возможность использования антидепрессантов, антагонистов 5-НТ3, агонистов κ-опиоидных рецепторов, аналогов соматостатина (октреотида). Из них лучше всего изучены антидепрессанты, реализующие противоболевой эффект двумя путями: 1) за счет уменьшения депрессивной симптоматики, учитывая тот факт, что хроническая боль может быть маской депрессии; 2) за счет активации антиноцицептивных серотонинергических и норадренергических систем. Антидепрессанты назначаются в терапевтических (но не в низких) дозах (амитриптилин 50-75 мг/сут., миансерин 30-60 мг/сут. и т. д.), продолжительность их приема должна составлять не менее 4-6 недель. Препараты эффективны в комплексной терапии.
Таким образом, генез абдоминальных болей является полиэтиологическим и полипатогенетическим. Лечение болевого синдрома должно быть направлено на нормализацию структурных и функциональных нарушений пораженного органа, а также на нормализацию функций нервной системы, отвечающих за восприятие болей.
Литература.
1. Вегетативные расстройства. Руководство для врачей. Под ред. проф. А.М. Вейна. М., 1998.
2. Вейн А. М., Данилова А. Б. Кардиалгии и абдоминалгии // РМЖ, 1999. 7, № 9. С. 428-32.
3. Григорьев П. Я., Яковенко А. В. Клиническая гастроэнтерология. М.: Медицинское информационное агентство, 2001. С. 704.
4. Ивашкин В. Т. Синдром раздраженной кишки // Рос. журн. гастроэнтерол., гепатол., колопроктол. 1993, т. 2, № 3. С. 27-31.
5. Яковенко Э. П. Григорьев П. Я. Хронические заболевания внепеченочных желчевыводящих путей. Диагностика и лечение. Метод. пособие для врачей. М.: Медпрактика, 2000. С. 31.
Таблица 1. Этиология абдоминальных болей
Интраабдоминальные причины
Экстраабдоминальные причины
Примечание. Частота заболеваний в рубриках указана в убывающем порядке.
Абдоминальная боль: трудности трактовки и методы купирования.
А. И. Лобаков, Е. А. Белоусова.
Возникшая в органе патология приводит к нарушению координации на любой из указанных осей и всей системы в целом. Именно поэтому большинство хронических гастроэнтерологических заболеваний с синдромом хронической абдоминальной боли сопровождается различными нейропсихическими отклонениями, чаще всего депрессией.
Нередко при хронической абдоминальной боли назначаются НПВС, что при многих гастроэнтерологических заболеваниях противопоказано. «Любимым» назначением в хирургии при панкреатитах в течение нескольких десятилетий остается малоэффективная «глюкозо-новокаиновая смесь». В то же время, в терапевтической и гастроэнтерологической практике недооценивается необходимость назначения психотропных препаратов, как аналгезирующих средств, особенно антидепрессантов, поскольку в структуру хронической абдоминальной боли у гастроэнтерологических больных входят невротические нарушения. Подобные ошибки многочисленны и обусловлены, вероятнее всего, недостаточным знанием врачами причин этой боли. Часто назначение аналгетиков маскирует ее истинные причины и подменяет собой базисное лечение основного заболевания, вызывающего боль, что способствует его прогрессированию. Необоснованное применение аналгетиков приводит к полипрагмазии, лекарственным взаимодействиям и осложняет течение заболевания. Мы полагаем, что при хронической абдоминальной боли, в силу разнообразия ее механизмов, подход к назначению аналгетических препаратов должен быть более взвешенным и дифференцированным. В основе, естественно, должно лежать лечение основного заболевания. Но и методы обезболивания должны, прежде всего, базироваться на патогенетическом принципе, для чего необходимо оценивать болевой синдром с разных позиций. В ряде случаев, при правильно построенной патогенетической терапии основного заболевания, боль купируется как результат лечения и необходимости в назначении аналгезирующих средств не возникает.
Для купирования хронической абдоминальной боли, с нашей точки зрения, должны учитываться, как минимум, четыре параметра: топография и интенсивность боли, доминирующий механизм ее формирования и выраженность психоневротических реакций.
Правильное определение топографии (источника) боли в большой степени способствует правильному диагнозу. В гастроэнтерологической практике хроническая абдоминальная боль не всегда ощущается больным вблизи ее непосредственного источника. Это связано с многочисленными зонами иррадиации, перекрывающими друг друга, или с атипичной локализацией болевых ощущений. Иногда боль в зоне иррадиации воспринимается больным сильнее, чем боль основной локализации. Большое значение имеет атипичная локализация боли, как, например status gastralgicus при остром инфаркте миокарда или, наоборот, боль за грудиной при заболеваниях пищевода. Нетипичная локализация боли в правом подреберье, правой подвздошной области или поясничной области может встречаться при хроническом панкреатите. Разлитая боль в верхней части живота бывает в первые сутки острого аппендицита, при почечной колике. Описаны случаи боли в животе при острой пневмонии. Разлитая или перемещающаяся боль может быть также связана с близким анатомическим соседством разных органов, одновременно вовлеченных в патологический процесс (соседство двенадцатиперстной кишки, желчного пузыря и поджелудочной железы при желчнокаменной болезни или хроническом панкреатите). Подобных ситуаций, когда локализация боли не соответствует местоположению больного органа, можно привести много. Ошибочный диагноз при неправильной трактовке боли чреват опасными последствиями. Необходимость учитывать все вышесказанное прежде всего касается врачей-терапевтов из поликлиник.
В настоящей статье не рассматривается хроническая абдоминальная боль при онкологических заболеваниях и острой хирургической патологии.
Приведенные причины при большинстве гастроэнтерологических заболеваний встречаются в различных сочетаниях, однако в каждом случае можно выделить доминирующие механизмы. Природа абдоминальной боли может быть органической и/или функциональной. В рамках одной статьи мы ограничимся лишь разбором болевых механизмов и лечебных подходов при наиболее часто встречающихся заболеваниях.
Тактика лечения должна быть направлена на патогенез основного заболевания, механизмы которого часто совпадают с механизмами болевого синдрома. Правильно подобранное лечение приводит к исчезновению или уменьшению боли как главного симптома болезни. В таких случаях не возникает необходимости в дополнительном назначении аналгетиков. Так, при гастральных и дуоденальных язвах применение Н2-блокаторов или ингибиторов протоновой помпы приводит к исчезновению боли через 3-4 дня. Тем не менее, в лечебных учреждениях, особенно в поликлиниках, при обострении язвенной болезни часто назначают различные аналгетики, иногда в ущерб базисному лечению.
У значительного количества больных хроническая абдоминальная боль связана не с органическими заболеваниями, а с функциональными расстройствами желудочно-кишечного тракта. Различные функциональные нарушения органов пищеварения описаны с 1980 г., но лишь в 1999 г. в Риме был принят международный консенсус по функциональным гастроинтестинальным расстройствам, который получил название «Римские критерии II» (в продолжение Римских критериев I, которые были приняты на первом рабочем совещании 1988 г.). В этих документах сформулированы определения, изложена классификация, основные диагностические критерии и методы лечения функциональных расстройств, которые широко распространены, особенно в промышленноразвитых странах. Этой патологией страдает предположительно 20% населения земного шара, преимущественно женщины.
Функциональные гастроинтестинальные расстройства (Рим II):
В формировании функциональных расстройств пусковая роль принадлежит психосоциальным факторам и нарушениям нейрогуморальной регуляции на оси мозг-желудочно-кишечный тракт, которые приводят к нарушениям двигательной функции желудочно-кишечного тракта. В патологических взаимодействиях немаловажную роль играет нарушение баланса нейротрансмиттеров и регуляторных пептидов (холецистокинин, мотилин, серотонин, нейротензин, эндогенные опиаты-энкефалины и эндорфины, вазоактивный интестинальный пептид), контролирующих основные кишечные функции.
Большая часть функциональных расстройств из приведенного перечня сопровождается хронической абдоминальной болью. Самым распространенным среди функциональных расстройств является синдром раздраженного кишечника. Согласно Римским критериям (Рим I, 1988), синдром раздраженного кишечника определяется как комплекс функциональных (т.е. не связанных с органическим поражением кишечника) расстройств продолжительностью свыше 3 месяцев, основными клиническими симптомами которого являются боли в животе (обычно уменьшающиеся после дефекации), сопровождающиеся метеоризмом, урчанием, чувством неполного опорожнения кишечника или императивными позывами на дефекацию, а также нарушениями кишечных функций: запорами, поносами или их чередованием.
В зависимости от ведущего симптома выделяют 3 клинических варианта синдрома раздраженного кишечника:
Если функциональный метеоризм, запор или диарея не ассоциированы с абдоминальной болью, то они выделяются в самостоятельные нарушения. Абдоминальная боль без нарушения кишечных функций также выделена в отдельную категорию.
Моторные нарушения при синдроме раздраженного кишечника носят гиперкинетический характер и приводят к спазму гладких мышц и нарушению пассажа содержимого по кишечнику или усилению пропульсии, что сопровождается болью. Нарушения моторики при разных функциональных расстройствах могут также протекать по типу гипотонии и атонии. В этих случаях боль обусловлена не спастическим компонентом, а растяжением стенок полого органа с повышением внутрипросветного давления.
Кроме синдрома раздраженного кишечника, существенная роль среди причин хронической абдоминальной боли принадлежит билиарным дисфункциям.
Функциональные нарушения могут сопутствовать органическим заболеваниям и вносят дополнительный вклад в основные механизмы хронической абдоминальной боли. В таких случаях они не рассматриваются как самостоятельная патология, но должны быть обязательно учтены при назначении лечения.
Для функциональных расстройств с синдромом хронической абдоминальной боли, кроме моторных, очень характерны сенсорные отклонения, характеризующиеся висцеральной гиперчувствительностью, т.е. изменением чувствительности рецепторного аппарата к различным раздражителям и снижением болевого порога. В развитии гиперчувствительности повинны те же механизмы, причем в реализации болевых ощущений принимают участие как центральные, так и периферические болевые рецепторы.
Очень важную роль в развитии функциональных расстройств и в возникновении хронической абдоминальной болезни играют психосоциальные факторы и социальная дизадаптация.
Независимо от характера боли, особенностью болевого синдрома при функциональных расстройствах является возникновение болей в утреннее или дневное время при активности больного и стихание их во время сна, отдыха, отпуска.
Лечение функциональных расстройств должно быть комплексным, направленным на ликвидацию взаимозависимых центральных и висцеральных вредных воздействий, нормализацию моторной и сенсорной функций.
Для снижения сократительной активности гладких мышц, устранения спазма и восстановления нормального транзита применяют релаксанты гладкой мускулатуры желудочно-кишечного тракта.
Холинолитики. Поскольку сократительная активность гладких мышц опосредована парасимпатической нервной системой, то применение антихолинэргических средств абсолютно обосновано и достаточно эффективно. Однако, холинолитики, обладая системным действием, имеют большое количество хорошо известных побочных эффектов, что особенно сильно проявляется при курсовом приеме.
Миотропные спазмолитики прямого действия (но-шпа, папаверин) широко применяются для купирования спазмов и хронической абдоминальной боли. Наибольшей антиспастической активностью обладает мебеверин (дюспаталин), который также оказывает прямое миотропное действие, однако он имеет ряд преимуществ перед другими спазмолитическими средствами. Дюспаталин почти селективно расслабляет гладкие мышцы пищеварительного канала, преимущественно толстой кишки, не влияя на гладкомышечную стенку сосудов. Механизм действия дюспаталина заключается в том, что он блокирует поступление в миоциты ионов натрия, что опосредовано приводит к закрытию кальциевых каналов и уменьшению мышечных сокращений. Препарат оказывает не только антиспастическое, но и нормализующее действие на стенку кишки, не подавляя полностью кишечные сокращения после гипермоторики, т.е. не вызывает рефлекторной гипотонии. Это свойство позволяет применять его у больных с хронической абдоминальной болью функционального генеза, сопровождающуюся как запором, так и диареей. Дюспаталин обладает пролонгированным действием и принимается не чаще двух раз в сутки в виде капсул по 200 мг.
При снижении двигательной активности или дискоординации по смешанному типу используют прокинетики. Моторные нарушения верхних отделов желудочно-кишечного тракта хорошо коррегируются блокаторами дофаминовых рецепторов. В течение многих лет успешно применяется метоклопрамид (церукал, реглан) и более активный домперидон (мотилиум). Обе группы имеют сродство и к центральным и к периферическим рецепторам, однако у метоклопрамида центральные эффекты в виде сонливости, нарушения внимания выражены сильнее, поэтому его не рекомендуют назначать больным в ситуациях, требующих особой сосредоточенности. На моторику дистальной части тонкой кишки и толстую кишку препараты не действуют. Универсальным средством, нормализующим двигательную функцию на всех уровнях желудочно-кишечного тракта является, полный агонист опиатных рецепторов дебридат. Нормализация моторики приводит к уменьшению боли.
Снижению висцеральной чувствительности в настоящее время уделяется большое внимание во всем мире, однако для этого пока нет лекарственных средств с доказанной эффективностью. Гиперчувствительность опосредуется болевыми рецепторами в центральной нервной системе и на периферии в энтеральной нервной системе. В медиации боли принимают участие многочисленные регуляторные пептиды и нейротрансмитеры. Перспективы в этом направлении связывают с препаратами, влияющими на эти структуры, в частности, на разные типы серотониновых рецепторов. Эти средства сейчас находятся на стадии клинических испытаний. На них же возлагаются надежды как на активные регуляторы моторики. На сегодняшний день для уменьшения гиперчувствительности реально применяются только антидепресссанты.
При учете всех параметров функциональных расстройств и подборе комплексного лечения значительно улучшается состояние больного, уменьшается или полностью купируется боль.
В итоге можно сделать следующее заключение:
Определить и устранить истинную причину функциональных нарушений в большинстве случаев невозможно, но топография и механизм боли при них могут быть установлены при тщательном сборе анамнеза и детальном обследовании.