адренархе у девочек что это
Преждевременное половое развитие: причины, диагностика, лечение
Преждевременное половое развитие является частым нарушением полового созревания у детей и по своей этиологии и патогенезу является гетерогенным заболеванием. В статье обобщены современные данные о причинах нарушения становления гипоталамо-гипофизарно-гона
Precocious sexual development is the frequent violation of puberty in children and in their etiology and pathogenesis is a heterogeneous disease. The article summarizes the current data on the causes of violations of formation of the hypothalamic-pituitary-gonadal relationships cause premature sexual development. A classification of diagnosis and treatment of this pathology.
Половое созревание — генетически обусловленный процесс превращения детского организма во взрослый, способный к воспроизводству. В широком смысле достижение половой зрелости включает в себя не только физиологический процесс, но и социальную адаптацию.
В настоящее время средний возраст наступления пубертата у девочек колеблется от 8 до 13 лет, а у мальчиков — от 9 до 14 лет.
Существенное влияние на сроки начала полового созревания оказывают пол ребенка, расовая принадлежность, наследственная предрасположенность, факторы окружающей среды, характер питания, социально-экономическое положение. Неблагоприятную роль могут играть, например, ожирение и экзогенное поступление гормонов [1].
Физиология полового развития
Мужские и женские гонады формируются из одного недифференцированного зачатка. Развитие половых желез у обоих полов на ранних стадиях протекает одинаково (индифферентная стадия). Ген, определяющий дифференцировку гонады по мужскому типу, локализован в Y-хромосоме.
Основой развития внутренних половых органов являются вольфовы (у мальчиков) и мюллеровы (у девочек) протоки.
Формирование наружных гениталий плода мужского пола начинается с 8-й недели внутриутробного периода и происходит под влиянием дигидротестостерона, образующегося из тестостерона фетальных яичек. Андрогены необходимы для дифференцировки эмбриональных закладок по мужскому типу. Клетки Лейдига, в которых вырабатываются андрогены, функционируют под действием хорионического гонадотропина плаценты. Из полового бугорка формируется половой член, наружные генитальные складки образуют мошонку. На 18–20 неделе внутриутробного развития заканчивается формирование наружных гениталий по мужскому типу, хотя процесс опускания тестикул в мошонку происходит значительно позже, к 8–9 месяцу гестации. После рождения выработка тестостерона стимулируется гонадотропинами гипофиза.
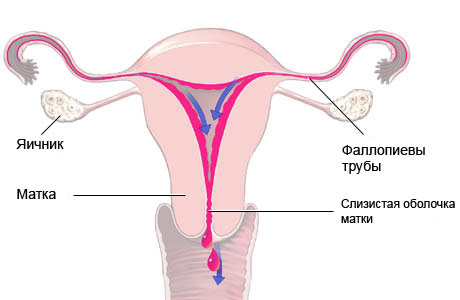
При формировании организма женского пола из верхней трети протоков Мюллера развиваются маточные трубы; средняя часть протоков, сливаясь, образуют тело и шейку матки. Вольфовы протоки регрессируют.
С 12-й по 20-ю неделю внутриутробного периода формируются влагалище, клитор, большие и малые половые губы, преддверие влагалища с раздельными наружным отверстием мочеиспускательного канала и входом во влагалище. У плода женского пола дифференцировка наружных гениталий происходит независимо от состояния гонад [2].
Пусковой механизм полового созревания, связанный с активацией нейроэндокринной системы, на сегодняшний момент недостаточно ясен. Однако известно, что инициирует этот процесс импульсная секреция гонадотропин-рилизинг-гормона (люлиберин, рилизинг-гормон лютеинизирующего гормона (ЛГ-РГ)) нейронами, расположенными в ядрах гипоталамуса. Развитие гипоталамо-гипофизарно-гонадной оси (гонадостат) происходит на протяжении всего периода жизни ребенка, начиная с внутриутробного [3].
У новорожденного ребенка гипоталамо-гипофизарно-гонадное регулирование полностью сформировано. У мальчиков эта система функционирует до 6–12 месяцев, у девочек до 2–3 лет жизни. Затем следует длительный период (до пубертата) ее угнетения — «ювенильная пауза». Резко снижается импульсная секреция ЛГ-РГ. Несмотря на низкое содержание в крови половых стероидов этот период является критическим для преждевременного полового развития (ППР) центрального генеза.
К концу «ювенильной паузы» — к 6–7 годам у девочек и к 8–9 у мальчиков — начинают интенсивно синтезироваться надпочечниковые андрогены, вызывая у девочек развитие вторичного оволосения (лобкового и подмышечного). У мальчиков эту роль играют главным образом андрогены тестикулярного происхождения. Этот период, предшествующий пубертату, обозначают как фазу адренархе.
Окончательное формирование гонадостата происходит в пубертатный период. Активация генератора импульсной секреции ЛГ-РГ стимулирует выработку лютеинизирующего гормона (ЛГ) и фолликулостимулирующего гормона (ФСГ) гипофиза, которые необходимы для образования гонадных стероидов — андрогенов и эстрогенов. В основе регуляции этой системы в репродуктивном возрасте лежит принцип обратной связи между этими гормонами.
У мальчиков основным гормоном полового созревания является тестестерон, который секретируется клетками Лейдига в семенниках и частично в коре надпочечников. Сам тестостерон малоактивен. В органах-мишенях с помощью фермента 5α-редуктазы он превращается в активную форму — дигидротестостерон. Нарастающая продукция андрогенов увеличенными тестикулами вызывает развитие вторичных половых признаков (понижение и огрубление голоса, рост волос на лице и теле по мужскому типу, превращение пушковых волос в терминальные, усиление секреции пота и изменение его запаха, увеличение размеров полового члена, пигментацию и развитие складчатости кожи мошонки, пигментацию сосков, формирование мужского типа лица и скелета, увеличение размеров простаты), регулирует сперматогенез и половое поведение.
В яичниках вырабатываются два основных гормона, которые оказывают наибольшее влияние на состояние и функционирование женской половой системы, — эстрадиол и прогестерон [2].
Эстрогены — общее собирательное название подкласса стероидных гормонов, производимых в основном фолликулярным аппаратом яичников у женщин. В небольших количествах эстрогены производятся также тестикулами у мужчин и корой надпочечников у обоих полов. Из различных биологических жидкостей человека выделено более 30 видов эстрогенов, основными из них считаются три: эстрон (Э1), 17-β-эстрадиол (Э2) и эстриол (Э3). Эстрадиол и некоторое количество эстрона синтезируются в яичниках. Эстрон и эстриол образуются преимущественно в печени из эстрадиола, а также в других тканях из андрогенов, главным образом из андростендиона. Синтез эстрогенов в фолликулах регулируется ФСГ.
Признаки начала полового созревания
Тестикулы имеют две основных функции: продукция гормонов и выработка сперматозоидов, причем первая начинается раньше и стимулирует вторую. Уже через год после начала полового созревания в утренней моче мальчиков можно обнаружить сперматозоиды (сперматурия). Половой член (пенис) начинает расти вскоре после начала роста тестикул. По мере роста полового члена возникают эрекции, а затем поллюции. В среднем, потенциальной фертильности мальчики достигают к 13-летнему возрасту, а полной — к 14–16 годам.
Под влиянием андрогенов происходит рост гортани, удлинение и утолщение голосовых связок, что делает голос более низким. Изменение голоса обычно сопутствует скачку роста тела.
Оволосенение (адренархе) начинается с лобка, вскоре после начала роста тестикул. Появившись в небольшом количестве у основания полового члена, волосы постепенно становятся гуще и занимают весь лобковый треугольник, после чего распространяются на бедра и по белой линии живота к пупку. Следом, по истечении нескольких месяцев и даже лет, начинается рост волос в подмышечных областях, около заднего прохода, на верхней губе, около ушей, вокруг сосков и на подбородке. Последовательность и темп роста волос подвержены индивидуальным различиям. В течение жизни волосы продолжают расти и становятся гуще на руках, ногах, груди, животе и спине.
К концу пубертата у юношей формируется мужской тип скелета: узкий таз и относительно широкий плечевой пояс.
Рост молочных желез (телархе) является первым признаком полового созревания у девочек и наблюдается в среднем в возрасте 10,5 лет. Сначала под ареолой с одной или обеих сторон появляется небольшое, болезненное уплотнение. По прошествии 6–12 месяцев уплотнение начинает отмечаться с обеих сторон, оно увеличивается в размерах, становится более мягким и выходит за пределы ореолы. За 2 года молочные железы достигают зрелого размера и формы, соски становятся четко выраженными. Размеры и форма молочных желез у девушек имеют выраженные индивидуальные различия.
Волосы на лобке появляются через несколько месяцев после начала роста молочных желез. У 15% девочек этот признак появляется первым. Сначала это единичные волоски на половых губах, за 6–12 месяцев распространяющиеся на лобок. В дальнейшем волосы разрастаются и покрывают весь лобковый треугольник. Под влиянием эстрогенов эпителий влагалища утолщается и клетки начинают активно слущиваться с его поверхности, увеличивается васкуляризация влагалища. В яичниках начинают расти фолликулы.
При проведении ультразвукового исследования в этом периоде можно увидеть множество мелких кист — фолликулов. Первая менструация (менархе) обычно наступает через 2 года после начала роста молочных желез [3].
В течение пубертата под влиянием высокого уровня эстрогенов происходит рост костей таза в ширину, в результате чего бедра становятся шире. Жировая ткань нарастает, и к концу пубертата объем жировой ткани у девушек превышает таковой у юношей в два раза. Жир откладывается, в основном, в области молочных желез, бедер, ягодиц, плечевого пояса, лобка.
Преждевременное половое развитие
Под ППР понимают появление симптомов пубертата до достижения возраста 8 лет у девочек и 9 лет — у мальчиков. Данная патология может быть обусловлена нарушением в системе гонадостата на различных уровнях. Большинство авторов придерживаются патогенетической классификации ППР.
Выделяют истинные, или церебральные, формы заболевания, патогенез которых связан с преждевременной импульсной секрецией ЛГ-РГ гипоталамусом. Повышенный синтез половых стероидов в этих случаях обусловлен избыточной продукцией гипофизарных гонадотропных гормонов. Особенностью истинного ППР является то, что оно протекает как изосексуальное, а биологические изменения организма соответствуют стадиям нормального полового развития, но в ускоренном темпе. Избыточная секреция половых стероидов увеличивает скорость роста и способствует быстрому закрытию зон роста.
В особую группу относят так называемые гонадотропиннезависимые формы ППР, при которых автономная активация деятельности половых желез обусловлена генетическими нарушениями. Эти варианты ППР имеют все признаки развернутого пубертата — увеличение половых желез, ускорение роста и костного созревания, формирование вторичных половых признаков.
Встречаются больные с единственным признаком преждевременного пубертата: изолированное развитие вторичного оволосения (преждевременное пубархе) и изолированное развитие молочных желез (преждевременное телархе). Это неполные формы ППР.
Истинное преждевременное половое развитие
Причиной истинного ППР могут быть различные поражения центральной нервной системы (ЦНС) неопухолевого характера (органические, воспалительные и др.), а также воздействие неблагоприятных факторов во внутриутробном периоде (травмы, гипоксия, инфекции). У таких детей часто выявляют гидроцефальный синдром. Причиной ППР могут быть арахноидальные кисты дна 3-го желудочка и хиазмально-селлярной области головного мозга. Кисты формируются в период эмбриогенеза, реже — в результате перенесенного менингита, энцефалита, травмы головного мозга.
У части больных с истинным ППР не удается выявить причину заболевания. В таких случаях при исключении органических заболеваний ЦНС ставится диагноз идиопатической формы ППР. Однако совершенствование методов исследования (применение компьютерной и магнитно-резонансной томографии) головного мозга позволяет чаще выявлять причину церебральной формы ППР.
О конституциональном характере ППР можно предположить, если при сборе анамнеза выясняется, что у родственников пубертат начался на 2–3 года раньше.
Современные методы обследования позволяют рано визуализировать опухоли ЦНС.
Гамартома — одна из часто выявляемых опухолевых образований ЦНС у детей с истинным ППР в возрасте до 3 лет. Гамартома гипоталамуса — это доброкачественная опухоль, состоящая из скопления дифференцированных нервных клеток, образованных в период эмбриогенеза. По существу она является следствием порока развития нервной ткани. Прижизненная диагностика стала возможной лишь с внедрением в практику магнитно-резонансных томографов.
Ведущим синдромом гипоталамических гамартом является ППР, это связано с тем, что нейросекреторные клетки гамартом выделяют ЛГ-РГ, который стимулирует образование в гипофизе ЛГ с последующей избыточной продукцией в гонадах стероидных гормонов. Следует отметить, что нарушение миграции эмбриональных клеток, секретирующих ЛГ-РГ, может вести к эктопии этих клеток, т. е. они могут находиться вне гипоталамуса. Считается, что ППР в этом случае развивается через эндогенный пульсирующий выброс ЛГ-РГ самостоятельно либо совместно с ЛГ-РГ секретирующими нейронами гипоталамуса. Есть предположение, что ППР может быть вызвано с помощью непрямого действия глиальных факторов, в том числе преобразованием альфа-фактора роста, который стимулирует секрецию гонадолиберина в гипоталамусе. Удаление гамартомы не во всех случаях тормозит половое развитие. У этих больных вторичная активация астроглиальных клеток в окружающих гипоталамус тканях может вызвать повышенную секрецию ЛГ-РГ, тем самым сохраняя клинику ППР [5].
У детей с гамартомой заболевание проявляется в виде истинного ППР в раннем возрасте. Частота развития заболевания одинакова у мальчиков и девочек. Из неврологической симптоматики могут отмечаться малые эпилептические приступы в виде насильственного смеха, снижение памяти, агрессивность.
Большинство опухолей хиазмы и гипоталамуса у детей — это низкодифференцированные глиомы. В супраселлярной области чаще выявляются астроцитомы [3].
Глиомы ствола головного мозга, вызывающие ППР, часто встречаются при нейрофиброматозе 1-го типа (болезнь Реклингхаузена). Это заболевание имеет аутосомно-доминантный тип наследования и встречается с частотой 1:3500 новорожденных.
Поломка гена, ответственного за синтез белка нейрофибромина, вызывает бурный неконтролируемый рост клеток. В клинической картине характерны пигментные пятна на коже от светло- до темно-коричневого цвета. Нейрофибромы — доброкачественные небольшие новообразования — располагаются на коже, радужной оболочке глаз, центральной нервной системе. Характерны множественные костные дефекты. Патогномоничным симптомом этого заболевания является наличие пигментных пятен на коже цвета «кофе с молоком» размером более 0,5 см. Патогенез ППР при доброкачественных опухолях и кистах ЦНС не ясен, но у больных выявляли пубертатные показатели гонадостата. Особенность этого процесса заключается в том, что неврологическая симптоматика (головные боли, судороги, нарушения зрения и другие) предшествуют симптомам ППР [6].
Синдром Рассела–Сильвера характеризуется комплексом наследственных аномалий (предположительно аутосомно-рецессивный тип наследования): внутриутробной и постнатальной задержкой роста и нарушениями формирования скелета. Частота встречаемости 1:30 000 населения. Дети рождаются небольшой длины (до 45 см) и с малой массой тела (1,5–2,5 кг) при доношенной беременности. С годами отставание в росте сохраняется, в связи с чем окончательный рост у женщин составляет менее 150 см, у мужчин — немногим выше 150 см. Масса тела у взрослых нормальная или даже избыточная. Часты аномалии наружных половых органов: крипторхизм, гипоспадия, гипоплазия полового члена, мошонки. Характерна асимметрия тела (лица, туловища, длины ног). Лицо треугольной формы, псевдогидроцефалия, большой лоб и гипоплазия нижней челюсти, высокое небо, нередко с расщелиной, оттопыренные уши. Клинодактилия V пальца за счет девиации дистальной фаланги, узкая грудная клетка, короткие руки, поясничный лордоз. Часто наблюдаются аномалии строения мочевыделительной системы. Интеллект обычно нормальный. Половое развитие начинает прогрессировать в 5–6 лет и имеет гонадотропинзависимый характер. Типичен повышенный уровень ЛГ и ФСГ на фоне гипогликемии [7].
Туберозный склероз (синдром Бурневиля–Прингла) — одна из форм факоматоза — характеризуется врожденной нервно-эктомезодермальной дисплазией с наличием доброкачественных опухолей. Встречается с частотой 1:10 000 новорожденных, чаще у мальчиков. Предположительно, заболевание имеет аутосомно-доминантный тип наследования. Фиброзные бляшки — облигатный признак этого заболевания. В мозге размер этих бляшек варьирует от нескольких миллиметров до нескольких сантиметров. Они могут быть единичными и множественными. В зависимости от локализации бляшки вызывают различные клинические симптомы: головную боль, рвоту, снижения зрения, эпилепсию, судорожные пароксизмы, гидроцефалию, признаки ППР.
Причиной истинного ППР могут быть опухоли, продуцирующие хориогонический гонадотропин человека (ХГЧ) (ХГЧ-секретирующие опухоли). К ним относятся герминогенные опухоли ЦНС, гепатобластомы и другие забрюшинные опухоли. Герминогенные опухоли развиваются из плюрипотентных зародышевых клеток. Многие из таких опухолей в период эмбриогенеза могут продуцировать ХГЧ. В процессе нарушенной миграции подобные клетки могут развиваться не только в гонадах, но и в других органах и тканях. Герминогенные опухоли составляют 3–8% от всех злокачественных новообразований детского и подросткового возраста. Нередко они сочетаются с различными генетическими синдромами (синдром Клайнфельтера, атаксия-телеангиоэктазия и др.).
Злокачественные герминогенные опухоли в 2–3 раза чаще встречаются у девочек, а интракраниальные — у мальчиков. У последних синдром ППР, связанный с избыточной секрецией ХГЧ, сочетается с симптомами несахарного диабета, повышенным внутричерепным давлением, сужением полей зрения, гемипарезами и др. Герминогенные опухоли, локализующиеся в головном мозге, интенсивно васкуляризированы и поэтому легко выявляются при компьютерной томографии с контрастированием. В сыворотке крови и в спинномозговой жидкости повышены уровни альфа-фетопротеина (АФП) и бета-ХГЧ; уровень тестостерона соответствует пубертатному периоду. Обнаруживается кажущееся повышение уровня ЛГ (из-за перекрестной иммунологической реактивности между ХГЧ и ЛГ). Однако уровень ЛГ не возрастает после стимуляции гонадолиберином. Уровень ФСГ снижен.
Не опустившиеся тестикулы представляют риск развития опухолей яичка. В клинической картине следует обратить внимание на объем яичек, которые увеличиваются умеренно и не соответствуют признакам достигнутого пубертата. Причина этого феномена в том, что у детей гонадостат остается незрелым. Из двух гонадотропных гормонов (ФСГ и ЛГ) опухолевые клетки тестикул продуцируют ЛГ, который гиперплазирует клетки Лейдига. В то же время клетки Сертоли, которые требуют воздействия ФСГ, остаются интактными. У мальчиков ППР развивается по изосексуальному типу.
Герминогенные опухоли разделяют на секретирующие бета-ХГЧ и не секретирующие его. В диагностике герминогенных опухолей важную роль играет определение АФП и бета-ХГЧ. Одним из маркеров злокачественного опухолевого процесса является раковый эмбриональный антиген (РЭА).
Ведущая роль в лечении герминогенных опухолей принадлежит химиотерапии. Лучевая терапия имеет очень ограниченное применение, она эффективна при лечении дисгермином яичника. Оперативное лечение направлено на удаление первичной опухоли [8].
Гепатобластома — злокачественная опухоль печени, развивающаяся из эмбриональной плюрипотентной закладки. Опухоль обычно представлена узлом беловато-желтого цвета, который прорастает в ткань печени. Гепатобластомы встречаются у детей до достижения 3-летнего возраста, после 5 лет жизни эта форма опухоли печени встречается очень редко. Точные причины возникновения гепатобластомы не выяснены. Гепатобластома может сочетаться с другими опухолями детского возраста, например, с опухолью Вильмса (нефробластомой). Повышенный риск возникновения гепатобластомы наблюдается у детей, перенесших гепатит B в период новорожденности, глистную инвазию, имеющих полипоз толстого кишечника, метаболические нарушения — наследственную тирозинемию, гликогеновую болезнь I типа и др. В начальном периоде развитии гепатобластомы выраженной симптоматики нет, прогрессирование сопровождается симптомами общей интоксикации и (редко) симптомами ППР вследствие продукции ХГЧ опухолью. Гепатобластома представляет собой быстрорастущую опухоль с высоким риском гематогенного метастазирования в легкие, головной мозг, кости и брюшную полость. Лечение гепатобластомы — хирургическое, заключающееся в удалении опухоли путем частичной гепатэктомии. Прогноз выживаемости при 1-й стадии заболевания в течение 2,5 лет — 90% и более, при 4-й стадии — меньше 30%.
Гонадотропиннезависимое ППР
Первые признаки заболевания ассоциируются с характерными светло-коричневыми пигментными пятнами на коже, которые имеются у новорожденного или появляются в течение первого года жизни.
Фиброзно-кистозная дисплазия проявляется в виде поражения длинных трубчатых костей. Измененные кости деформируются, возникают патологические переломы.
Из других эндокринных нарушений встречаются узловой эутиреоидный зоб, аденомы гипофиза (синдром Иценко–Кушинга, тиреотоксикоз и повышение уровня других гормонов).
Тестостероновый токсикоз обусловлен избыточной нерегулируемой секрецией тестостерона гиперплазированными клетками Лейдига. Это семейное, аутосомно-доминантное заболевание с неполной пенетрантностью, проявляющееся у лиц мужского пола. Избыточная продукция тестостерона вызвана точечной мутацией гена рецептора ЛГ. Мутантные гены вызывают внутриклеточную активацию метаболизма клеток Лейдига в отсутствии ЛГ [10].
Вторичные половые признаки обычно появляются в 3–5 лет, а первые симптомы андрогенизации могут наблюдаться уже в возрасте 2 года. Изменяется тембр голоса, характерны телосложение маскулинное, acne vulgaris, увеличение полового члена, эрекции, ускоряется рост и созревание скелета. Объем тестикул увеличен, но не соответствует степени андрогенизации. По клинической картине тестотоксикоз сходен с истинным ППР.
При исследовании гонадостата выявляются высокие уровни тестостерона при препубертатных показателях ЛГ и ФСГ. Отсутствует реакция ЛГ и ФСГ на тест с люлиберином (ЛГ-РГ), а также импульсная спонтанная секреция ЛГ, характерная для пубертатного периода.
При биопсии яичек обнаруживают хорошо развитые извитые семенные канальцы, избыток зрелых клеток Лейдига, половые клетки на разных стадиях сперматогенеза. В некоторых извитых семенных канальцах выявляются дегенерирующие половые клетки. У взрослых результаты пробы с гонадолиберином нормальные; у некоторых больных с повреждением сперматогенного эпителия повышен уровень ФСГ. У большинства мужчин с семейным тестотоксикозом фертильность не нарушена.
Окончание статьи читайте в следующем номере.
ГБОУ ВПО РНИМУ им. Н. И. Пирогова МЗ РФ, Москва
Пубертатный период (телархе, пубархе, менархе)
Пубертатный период (пубертат) включает серию стадий развития организма, при которых происходит половое созревание девочки и становление ее репродуктивной функции. Этот процесс сопровождается маркерными нейроэндокринными и физиологическими изменениями репродуктивной системы и достигает кульминации во время развития вторичных половых признаков, способности к овуляции и менструации, достижения фертильности.
Значительный скачок соматического роста, а также драматические психосоциальные изменения также характеризуют пубертатное развитие. Но изменения роста и психосоциального развития не всегда являются синхронными изменениям в репродуктивной системе, что приводит к неверной трактовки индивидуальной «зрелости». У девочек пубертатный период происходит быстрее, чем у мальчиков. Так, девочки завершают пубертатный развитие за 3 года, тогда как мальчики — за 5 лет.
Формирование вторичных половых признаков
К началу фенотипических изменений в связи с регенерацией ретикулярной зоны коры надпочечников возникает адренархе (в 6-8 лет). Гонадархе (около 8 лет) происходит с началом стимуляции под действием гонадотропин-рилизинг-гормона (ГнРГ) секреции передней долей гипофиза лютеинизирующего гормона (ЛГ) и фолликулостимулирующего гормона (ФСГ). Это, в свою очередь, является триггером к началу последующих физических изменений, включая развитие молочных желез (телархе), развитие лобкового и аксилярного оволосения (пубархе), скачок роста и начало менструаций (менархе), обычно в таком порядке. Адренархе и гонадархе не является частями пубертатного развития.
Гормональные изменения перед пубертатным периодом — адренархе и гонадархе
Адренархе — рост продукции андрогенов надпочечниками — возникает между 6 и 8-м годами жизни. В надпочечниках начинается регенерация ретикулярной зоны, которая была подавлена сразу после рождения девочки, с сопутствующим повышением активности Р450 микросомальных энзимов. Этот внутренний слой коры надпочечников является ответственным за секрецию половых стероидных гормонов. В результате возрастает продукция андрогенных стероидных гормонов надпочечников — дегидроэпиандростерона сульфата (ДГЭАС), дегидроэпиандростерона (ДГЭА) и андростендиона, что имеет место от 6-8 до 13-15 лет.
Гонадархе — установление нормальной функции яичников — начинается около 8 лет, когда возрастает пульсирующая секреция ГнРГ гипоталамусом. Это ведет к стимуляции синтеза гонадотропинов ФСГ и ЛГ передней долей гипофиза, происходит преимущественно во время сна и не сопровождается никакими фенотипическими изменениями.
Первым признаком пубертатного периода является увеличение пульсационной секреции ЛГ ночью. Эту пульсационную секрецию ЛГ ночью меняет Пульсационная секреция ЛГ и ФСГ в течение дня, что приводит к росту уровня эстрогенов вследствие роста фолликулов в яичниках. Положительная обратная связь от увеличения уровня эстрадиола инициирует пик ЛГ, необходимый для индукции овуляции.
Адренархе не является обязательным для нормальной функции яичников — гонадархе. Это подтверждается тем фактом, что пациентки с гипофункцией коры надпочечников имеют нормальное пубертатное развитие. Яичники, в свою очередь, могут начинать функционировать до адренархе в случае преждевременного пубертатного развития. С другой стороны, гонадная функция не является необходимой для функции надпочечников — доказательством служит нормальное адренархе у пациенток с дисгенезией гонад.
Первым фенотиповым изменением в пубертатном периоде в большинстве случаев является начало развития молочных желез (телархе), которое происходит около 10 лет. Но иногда может наблюдаться увеличение скорости линейного роста за 1-2 года до начала телархе, извещающее о начале пубертатного развития.
После телархе начинает развиваться лобковые оволосение, пубархе (нередко вместе с аксиллярным), что имеет место около 11 лет. Дальнейшими событиями обычно являются пубертатный скачок роста (9 см / год), который наблюдается около 12 лет и, наконец, менархе — около 13 лет. Менархе происходит обычно через 2-2,5 года после телархе. Нормальное пубертатное развитие начинается в пределах 2,5 стандартных отклонений от средних значений, т.е. между 8 и 14 годами.
Телархе
Первой стадией телархе является развитие почек молочных желез, обычно происходит около 10-11 лет. Телархе обычно является первым фенотиповым изменением в серии событий пубертатного возраста и возникает вследствие роста уровня циркулирующих эстрогенов. Одновременно с телархе происходит эстрогенизация слизистой оболочки влагалища и развитие влагалища и матки. Дальнейшее развитие молочных желез происходит в течение пубертатного и подросткового периода. Соответствующие изменения молочных желез разделяют на 5 стадий, согласно классификации Маршалла и Таннера.
Пубархе
Начало роста лобковых волос обычно происходит после телархе, примерно в 11 12 лет, и часто сопровождается ростом аксилярных волос. Пубархе обычно происходит после телархе, но одновременное развитие телархе и пубархе также является нормальным. У представительниц черной расы пубархе может предшествовать телархе, что не является патологией.
Развитие лобкового и аксилярного оволосения происходит вторично вследствие увеличения концентрации циркулирующих андрогенов. Иногда понятие пубархе и адренархе употребляют как синонимы, но это не совсем верно. Пубархе — развитие лобкового оволосения, что происходит под действием надпочечниковых андрогенов в возрасте после 10 лет в стадии пубертатного развития, а адренархе — активизация синтеза андрогенов в надпочечниках, что происходит между 6 и 8-м годами жизни и предшествует началу пубертатного развития.
Пубертатный скачок роста
Увеличение секреции эстрогенов стимулирует продукцию гормона роста, который, в свою очередь, стимулирует инсулиноподобный фактор роста I, что способствует увеличению соматического роста. Пубертатный скачок роста характеризуется ускорением роста девочки, начинается в возрасте 9-10 лет и достигает максимальной скорости между 12 и 13-м годами (9 см / год).
Но эти взаимоотношения являются дозозависимыми, и чрезмерный уровень эстрогенов приводит к угнетению выделения гормона роста и соматомедина-С. В дальнейшем, в результате влияния эстрогенов на прекращение роста эпифизарных зон роста длинных трубчатых костей, за быстрым скачком роста может произойти прекращение роста.
Эстрогены усиливают рост костей, особенно осевого скелета. Гормон роста имеет большее влияние на рост длинных трубчатых костей. Это объясняет тот факт, что больные с гипогонадизмом часто имеют короткое туловище с относительно длинными конечностями (евнухоидный габитус). При дефиците гормона роста больные нередко имеют противоположную генетическому полу внешность. Эстрогены также способствуют закрытию эпифизарных зон роста трубчатых костей. Итак, пациенты с преждевременным половым развитием имеют раннее начало роста, но, окончательно, имеют невысокий рост вследствие преждевременного закрытия эпифизарных зон роста, если не проводится своевременное лечение.
Менархе
Средний возраст менархе (первой менструации) колеблется между 12 и 13 годами (12,7 года). Менархе происходит обычно через 2 года после телархе (развития зачатков молочных желез). Менструальный цикл у подростков обычно является нерегулярным течение первых 6 мес-1 года после менархе, что свидетельствует об ановуляторных циклах. Установление регулярных овуляторных циклов от-ходит примерно через 2 года после менархе.
Задержка менархе может иметь место у гимнасток, бегунов на длинные дистанции и балерин. Высказываются мнения, что сигналом для начала менархе является достижение определенной массы тела (17-22% жировой ткани), обычно имеет место при массе тела> 45 кг. Но нет точных данных, что больше влияет на задержку менархе: недостаток жировой ткани или стрессовые и физические нагрузки.
Овуляторные менструальные циклы сопровождаются повышением уровня прогестерона после овуляции. Овуляция обычно является непостоянной в течение 1-2 лет после менархе, что проявляется нерегулярными менструальными циклами. После этого периода менструальный цикл у подростков должен установиться, и отсутствие регулярных циклов может свидетельствовать о репродуктивных расстройствах.
Нарушение пубертатного развития
Нормальное пубертатное развитие начинается между 8 и 14-м годами (± 2,5 стандартных отклонения от средних значений). Если у девочки вторичные половые признаки появляются в 8 лет, или если вторичные половые признаки отсутствуют до 14 лет, или если у девочки с развитыми вторичными половыми признаками отсутствует менструация до 16 лет, такие пациентки подлежат дополнительному обследованию.
У представительниц черной расы пубертатный период в норме может начинаться до 8 лет. Могут иметь место изолированное преждевременное телархе или пубархе без других признаков пубертатного развития, не требует срочного обследования, но свидетельствует о необходимости наблюдения для исключения возможного преждевременного пубертатного развития. Преждевременное телархе обычно возникает в первые 7 лет жизни, а преждевременное пубархе может быть ранним признаком синдрома поликистозных яичников в дальнейшей жизни. Преждевременное пубертатное развитие более частое у девочек (в 5 раз чаще, чем у мальчиков), а задержка пубертатного развития более частая у мальчиков.
Пубертатное развитие может начинаться раньше из-за следующих обстоятельств:
Позднее начало полового развития может наблюдаться:
1) при сахарном диабете;
2) при значительных степенях ожирения;
3) при недостаточном питании;
4) при чрезмерных стрессовых и физических нагрузках.
Преждевременное пубертатное развитие
Преждевременный пубертатный развитие — это появление вторичных половых признаков до 8 лет. У девочек около 75% преждевременного пубертатного развития является идиопатическим, тогда как у мальчиков — только 40%. Современные возможности высокочувствительных методов интракраниальной визуализации, в частности магнитно-резонансной томографии, возможно, позволят выявить причины этих так называемых «идиопатических» состояний.
Изосексуальное преждевременное пубертатное развитие — это преждевременный пубертатный период, соответствующий генетическому полу индивида.
Гетеросексуальное преждевременное пубертатный развитие — преждевременное пубертатное развитие, которое развивается по типу, противоположному генетическому полу индивида. Гетеросексуальное преждевременное пубертатное развитие у девочек отражает чрезмерную продукцию андрогенов надпочечниками или яичниками. Изосексуальное преждевременное развитие более частое, чем гетеросексуальное преждевременное половое развитие.
Выделяют две формы преждевременного полового развития: ГнРГ-зависимую и ГнРГ-независимую. ГнРГ-зависимая форма преждевременного полового развития («настоящая», «полная», «центральная») развивается вследствие преждевременной активации гипоталамо-гипофизарно-гонадной оси, а именно при ранней активации гипоталамического генератора ГнРГ-пульсации, и обычно являются идиопатический.
Лечение этого состояния заключается в назначении агонистов гонадотропин-рилизинг-гормонов (золадекс, диферелин, люпрон) с целью супрессии преждевременной активации ГнРГ-пульсации. Одной из наиболее серьезных причин ГнРГ-зависимого преждевременного пубертатного развития являются опухоли ЦНС), в частности гамартомы. Лечение гамартром может быть хирургическим, лучевым или медикаментозным (агонисты ГнРГ).
ГнРГ-независимая форма преждевременного полового развития (неполная, периферическая, преждевременное псевдопубертатное развитие) развивается вследствие продукции половых стероидов яичниками, которая не зависит от гипоталамо-гипофизарно-гонадной регуляции. В некоторых случаях периферическая продукция гормонов может активировать гипоталамо-гипофизарно-гонадную систему, что приводит к смешанной форме преждевременного полового развития.
Наиболее частыми причинами ГнРГ-независимого преждевременного полового развития могут быть следующие состояния:
Диагностика преждевременного полового развития и его форм начинается по сбору анамнеза больной. Выясняют особенности роста ребенка, особенности появления признаков пубертатного периода, семейный анамнез относительно возможных репродуктивных аномалий, наличие экзогенного гормонального воздействия, симптомы заболеваний щитовидной железы, неврологических и цереброваскулярных болезней (инсульт).
При объективном обследовании оценивают рост, массу тела относительно возрастных стандартов, массо-ростовой коэффициент. Оценивают выраженность вторичных половых признаков по шкале Таннера, выполняют исследования состояния щитовидной железы и неврологического статуса, обследуют кожу о наличии «кофейных пятен», проводят ультрасонографию, абдоминальное и тазовое (вагинальное или ректальное) исследование по выявлению функциональных кист и опухолей яичников.
Лабораторные анализы включают оценку сывороточных уровней эстрадиола, ЛГ, ФСГ, ТТГ (ТТГ) и хорионического гонадотропина человека (ХГЧ). В случае гетеросексуального полового развития, оценивают уровень ДГЭАС, 17-гидроксипрогестерона и тестостерона.
Наиболее важным радиологическим тестом является оценка костного возраста (в костях левого запястья) для оценки зрелости скелета. Костный возраст при всех формах преждевременного пубертатного развития был увеличен, за исключением первичного гипотиреоидизма (задержка костного возраста).
Задержка пубертатного развития
Задержка пубертатного развития — отсутствие развития вторичных половых признаков до 14 лет или отсутствие менархе до 16 лет. Отсутствие менархе до 16 лет называется первичной аменореей.
Пациенток с задержкой полового развития и первичной аменореей классифицируют по признаку наличия или отсутствия развития молочных желез (признак наличия продукции эстрогенов), а также присутствия или отсутствия матки:
2. Если развитие молочных желез отсутствует, оценивают уровень ФСГ, что позволяет выявить яичниковых недостаточность (высокий ФСГ) или гипоталамо-гипофизарную недостаточность (низкий ФСГ).
3. Случаи отсутствия матки и отсутствия развития молочных желез является исключительно редкими.
4. При наличии матки и наличии развития молочных желез ведение пациенток аналогично таковому при вторичной аменорее.
Наиболее частой причиной первичной аменореи и задержки полового развития является дисгенезия гонад (синдромы Тернера, Шерешевского-Тернера). На втором месте по частоте является агенезия матки и влагалища (первичная аменорея при наличии вторичных половых признаков при синдроме Майера-Рокитанского-Кюстера-Гаузера), на третьем — нечувствительность к действию андрогенов (синдром тестикулярной феминизации).
Менструальный цикл
Гипоталамус, гипофиз, яичники и матка — это компоненты репродуктивной системы женщины, которые принимают участие в установлении и регуляции менструального цикла и функционируют с помощью положительных и отрицательных прямых и обратных связей. У плода генетической женского пола на 20-й неделе развития яичники содержат 6-7 млн зародышевых клеток, количество которых уменьшается до 2 млн на момент рождения и до 300000 перед началом пубертатного периода.
Менструальный цикл в норме длится 28 дней (колебания от 21 до 35 дней). Только 15% женщин имеют 28-дневный менструальный цикл. Наиболее нерегулярным менструальный цикл является в течение 2 лет после менархе и 3 лет перед менопаузой (последней менструацией в жизни женщины). Ановуляторные циклы в эти периоды составляют 6-35%.
Менструальный цикл делится на две 14-дневные фазы: I — фолликулярную и II — лютеиновую, характеризующиеся изменениями в яичниках в течение цикла. Эти фазы еще имеют название пролиферативной и секреторной, отражающее синхронные изменения в эндометрии в этот же период времени. Эти циклические изменения происходят в поверхностном, функциональном слое эндометрия (как в его компактном, так и в спонгиозной слое), тогда как базальный слой эндометрия нечувствительным к гормональным стимулов и остается интактным в течение менструального цикла (регенеративная зона).
В течение фолликулярной фазы цикла, выделения ФСГ гипофизом вызывает развитие первичных яичниковых фолликулов. Яичниковые фолликулы продуцируют эстрогены, которые, в свою очередь, стимулируют пролиферацию эндометрия. Под действием ФСГ обычно лишь один из этих фолликулов (доминантный) достигает максимального развития — стадии зрелого (третичного, граафова) фолликула; другие прекращают развитие на разных стадиях (первичные, вторичные фолликулы).
В середине менструального цикла, около 14-го дня, в ответ на достижение максимальной концентрации эстрогенов, синтезируемых гранулезного клетками фолликулов, имеет место пик секреции ЛГ гипофизом. Этот пик ЛГ стимулирует овуляцию — разрыв стенки зрелого фолликула и освобождения яйцеклетки, которая почти сразу попадает в просвет ампулярной части маточной трубы.
После овуляции начинается ІІ, лютеиновая фаза менструального цикла. Доминантный фолликул, в котором состоялась овуляция, накапливает лютеиновый пигмент и развивается в желтое тело. Желтое тело рядом с секрецией эстрогенов начинает продуцировать прогестерон, способствующий секреторным изменениям эндометрия (децидуализация, децидуальные реакции — накопление гликогена, а также рост васкуляризации) для обеспечения имплантации оплодотворенной (фертилизованои) яйцеклетки.
Если оплодотворение не происходит, желтое тело дегенерирует, и уровень прогестерона (и эстрогенов) снижается. При резком уменьшении уровня прогестерона и эстрогенов в эндометрии развивается ишемия и десквамация эпителия функционального слоя — менструация (менструальная фаза).
Фолликулярная фаза
Отмена влияния действия эстрогенов и прогестерона в конце лютеиновой фазы предыдущего менструального цикла приводит к постепенному росту выделения ФСГ гипофизом. В свою очередь, ФСГ стимулирует рост от 5 до 15 примордиальных фолликулов (яйцеклеток, развитие которых остановлен в стадии диплотена в профазе первого мейотического деления, окруженных одним слоем гранулезных клеток), что означает начало I, фолликулярной, фазы нового менструального цикла. Развитие примордиальных (первичных) фолликулов до стадии Диплотена профазы первого мейотического деления не зависит от действия гонадотропинов.
Из этих примордиальных фолликулов обычно только 1 становится доминантным и созревает в преантральный, вторичный фолликул (ооцит, окруженный блестящей зоной с несколькими слоями гранулезных и тека-клеток). Развитие преантральних фолликулов является гонадотропинзависимым.
Селекция доминантного фолликула происходит на 5-7 день менструального цикла. Преантральний фолликул секретирует эстрогены, накапливает фолликулярную жидкость и созревает до стадии овуляторного (третичного, граафова) фолликула. ФСГ отвечает за индукцию синтеза ЛГ-рецепторов и фермента ароматазы, который отвечает за конверсию андрогенов в эстрогены в растущем фолликуле. Эстрогены действуют синергично с ФСГ и увеличивают количество ФСГ-рецепторов и в гранулезных клетках фолликула, а также их митотическую активность.
Фолликул развивается, достигает предовуляторной зрелости путем продукции эстрогенов, которые усиливают его созревание, а также стимулируют образование ФСГ- и ЛГ-рецепторов аутокринным путем. Эстрогены продуцируются «двухклеточным», «двогонадотропиновым путем». Клетки внутренней тека-оболочки фолликула (папка-клетки) в ответ на стимуляцию ЛГ производят андростендион, а гранулезные клетки фолликула под действием ФСГ и с помощью фермента ароматазы конвертируют этот андростендион в эстрадиол.
Синтез андрогенов, которые также конвертируются в эстрогены, стимулирует ЛГ. Андрогены способствуют атрезии недоминантных фолликулов. Андрогены в высоких концентрациях подлежат 5а-редукции в более активные андрогены. Преждевременное увеличение секреции ЛГ также уменьшает митотическую активность гранулезных клеток и способствует дегенеративным изменениям фолликулов.
Повышение уровня циркулирующих эстрогенов по закону центрального отрицательной обратной связи влияет на секрецию ФСГ гипофизом. Это приводит к отмене гонадотропинов поддержки других фолликулов развивающихся. Доминантный фолликул защищен от уменьшения уровня ФСГ вследствие увеличенной концентрации в нем ФСГ-рецепторов. Кроме того, рост васкуляризации внутреннего слоя тека-клеток также способствует большей чувствительности доминантного фолликула к действию ФСГ. Подавляя секрецию гонадотропинов за счет увеличения собственной продукции эстрогенов, доминантный фолликул оптимизирует свое собственное развитие путем прекращения роста других фолликулов.
Овуляция
В конце фолликулярной фазы уровень эстрогенов значительно возрастает и достигает критического (пикового) значения (> 200 пг / мл), что наблюдается в течение около 50 ч, что является триггером для передней доли гипофиза по освобождению максимального количества ЛГ. Этот положительная обратная связь между повышением уровня эстрогенов и ростом концентрации ЛГ усиливается низким уровнем прогестерона.
Овуляция возникает вследствие индуцированного ЛГ разрыва фолликула и освобождения зрелой яйцеклетки примерно через 34-36 ч после начала повышения уровня ЛГ или через 10-12 ч после достижения пика ЛГ. Пик ЛГ инициирует возобновление мейоза в ооците, вызывает лютеинизацию гранулезных клеток фолликула и стимулирует синтез простагландинов и прогестерона, необходимый для разрыва фолликула. Дегенеративные изменения в стенке фолликула могут развиваться вследствие деструкции коллагена, что приводит как пассивное уменьшения, так и разрыв фолликула. Простагландины и лизосомальные энзимы (протеазы) вызывают дегенеративные изменения в стенке фолликула.
Овуляция сопровождается завершением первого мейотического деления с выделением первого полярного тельца. Яйцеклетка обычно попадает в маточную трубу и благодаря движению ресничек ее эпителия продвигается в матку. Этот процесс обычно длится от 3 до 4 дней. Если фертилизация яйцеклетки не происходит в течение 24 ч после овуляции, она дегенерирует.
Лютеиновая фаза
После овуляции начинается лютеиновая фаза цикла. Клетки гранулезы и внутренней тека-оболочки фолликула выстилают его стенку, под действием ЛГ образуют желтое тело. Продолжительность жизни и стероидогенная активность желтого тела зависят от длительной тонической ЛГ-секреции, приводит к увеличению секреции желтым телом прогестерона. Нормальная функция желтого тела требует оптимального преовуляторного развития фолликула (т.е. адекватной ФСГ-стимуляции) и постоянной тонической ЛГ-поддержки.
Желтое тело синтезирует эстрогены и в значительном количестве прогестерон, вызывает дальнейшее развитие желез и секреторные изменения в эндометрии (васкуляризация, накопление гликогена), что являются подготовительными процессами для имплантации оплодотворенной яйцеклетки. Пик секреции прогестерона желтым телом имеет место около 8-го дня после пика ЛГ, что влияет на созревание секреторного эндометрия и супрессии роста фолликулов.
Каждый день лютеиновой фазы сопровождается определенными микроскопическими изменениями желез и стромы эндометрия. Имплантация обычно происходит на 22-23 день менструального цикла, совпадает с максимальной интрацеллюлярной апокринной секреторной активностью клеток эндометрия.
Если происходит фертилизация, развивающийся трофобласт начинает синтезировать хорионический гонадотропин человека (ХГЧ) — гликопротеин, подобный ЛГ, который обеспечивает поддержку функции желтого тела (развитие желтого тела беременности), т.е. стимулирует секрецию им эстрогенов и прогестерона, необходимую для поддержания эндометрия до развития плаценты и начала ее гормонпродуцирующей функции (8-10 нед гестации). Недостаточная функция желтого тела вызывает так называемый дефект лютеиновой фазы цикла (недостаточность лютеиновой фазы), что считается одной из возможных причин прерывания беременности на ранней стадии.
Если фертилизация, а следовательно и вызванный ею синтез ХГЧ не происходят, желтое тело дегенерирует (желтое тело менструации), уровне прогестерона и эстрогенов снижаются, гормональной поддержки эндометрия не происходит, в нем развиваются ишемические изменения и возникает менструация — отторжение функционального слоя эндометрия.