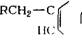алкилсульфонат натрия что это такое
Лако-красочные материалы — производство
Технологии и оборудование для изготовления красок, ЛКМ
АНИОНАКТИВНЫЕ МОЮЩИЕ ВЕЩЕСТВА
Представляют наиболее распространенные моющие вещества, к которым относятся:
1. Алкилкарбонаты (R— COONa)
А) первичные (R — S03Na)
4. Алкиларилсульфонаты (RArS03Na)
Алкилкарбонаты. Представляют собой соли жирных кислот или мыла, которые достаточно подробно описаны выше. Мыла условно можно отнести к синтетическим моющим веществам, учитывая, что сырьем для них служат синтетические жирные кислоты (СЖК).
Алкилсульфаты. Представляют собой натровые соли сульфо — эфиров высших жирных спиртов. В молекуле алкилсульфата сера связана с углеродом через кислород: н О
Различают первичные и вторичные алкилсульфаты. У первичных алкилсульфатов моющая способность возрастает с увеличением количества углеродных атомов в алкильном остатке и достигает оптимума (при температуре до 40° С) у алкилсульфатов с 12—14 атомами углерода. Алкилсульфаты с 16 и более углеродными атомами в цепи очень плохо растворимы в воде (при 20° С) и при взаимодействии с жесткой водой образуют малорастворимые кальциевые соли.
Получение алкилсульфатов. Алкилсульфаты получают суль- фатированием жирных спиртов с последующей нейтрализацией полученного сульфопродукта.
Жирные спирты получают различными способами.
В отличие от других стран, где для производства жирных спиртов, как правило, применяют кокосовое масло и животные жиры, в СССР производство жирных спиртов базируется на продуктах окисления парафина. Кроме того, в связи с расширением добычи кашалотов для производства жирных спиртов используется кашалотовый жир. Производство жирных спиртов из кашалотового жира разработано советскими учеными и проводится на Казанском химическом комбинате имени Вахитова по оригинальной технологии (омыление кашалотового жира под давлением в автоклавах, отгонка с паром образовавшихся жирных спиртов от мыла, конденсация спиртов, разложение мыла). На базе полученных жирных спиртов были синтезированы алкилсульфаты, а затем в 1953 г. впервые изготовлен отечественный синтетический моющий порошок «Новость», одобренный потребителями. В последнее время на одном из комбинатов освоен разработанный группой советских ученых и специалистов метод получения жирных спиртов из кашалотового жира путем гидрогенизации жирных кислот, находящихся в составе восков, и триглицеридов при высоком давлении (300 ат) И температуре 300° С. Применяемый цинково-хромовый катализатор способствует сохранению двойных связей, что обеспечивает максимальное содержание непредельных жирных спиртов в готовом продукте.
Методы производства жирных спиртов в СССР базируются на продуктах окисления парафина.
Метод гидрогенизации жирных кислот. Этот метод получил наибольшее распространение не только в нашей стране, но и за рубежом. Нужная фракция жирных кислот этерифицируется метиловым спиртом по схеме:
RCOOH + СН3ОН——— >- RCOOCH3 + Но О
Полученные метиловые эфиры жирных кислот подвергаются гидрогенизации в автоклавах под давлением 300 ат с применением плавающего катализатора
RCOOCH3 + 2Н2 ————— ► RCH2OH + СН3ОН
Образовавшиеся жирные спирты освобождаются от метилового спирта и катализатора, а затем дистиллируются.
Метод прямого окисления парафиновых углеводородов в присутствии борной кислоты. Этот метод впервые в мировой практике разработан в 1948 г. под руководством проф. Башкирова А. Н.
Сырьем служит синтин или мягкие парафины (фракции 275—320° С). Окисление ведется при температуре 165—170°С; борная кислота, являющаяся катализатором, связывает образующиеся спирты в виде эфиров и предохраняет их от дальнейшего окисления.
По этому методу получают в основном вторичные жирные спирты с распределением гидроксильной группы по всей длине углеводородной цепи.
Метод извлечения жирных спиртов изнеомы — ляемых-П. При окислении парафина до жирных кислот попутно образуются другие кислородсодержащие продукты, в том числе жирные спирты (в основном первичные). В неомы — ляемых-II содержится до 8% жирных спиртов от расходуемого на окисление парафина, их можно извлечь различными способами.
Сульфирование жирных спиртов. Для получения синтетических моющих веществ из жирных спиртов их подвергают сульфированию. При этом образуются не истинные суль — фокислоты, а сульфоэфиры.
Реакция сульфирования в общем виде может быть выражена следующим уравнением:
Группа — S02C1 присоединяется к любому атому углерода по всей длине цепи. Поэтому в результате реакции сульфохлорирования образуется смесь изомеров.
Обработкой едкой щелочью (15—207о-ный раствор) образовавшиеся сульфохлориды переводят в алкилсульфонаты:
Алкилсульфонаты могут быть получены и при помощи сульфо — окисления (открыто Платтом в 1940 г.)
Получающийся при указанных способах готовый продукт получил название «Сульфонат», он используется для приготовления синтетических моющих средств типа «Астра», «Новость», «Синтол». Технология получения алкилсульфонатов сравнительно проста, характеризуется низкими капитальными затратами, а сырьевая база практически неограниченна.
В течение 1961 —1962 гг. в Советском Союзе был разработан синтез и освоено промышленное производство нового синтетического моющего вещества ДНС (динатровая соль сульфоян — тарной кислоты), которое условно можно отнести к алкилсуль — фонатам. Структурная формула ДНС такова: ROCOCHo — СН —COONa
Жирные спирты (С14 — С18) реагируют с малеиновым ангидридом*, а затем обрабатываются бисульфитом натрия. При этом образуется динатровая соль моноалкилсульфоянтарной кислоты **. Процесс протекает по следующей схеме:
Производство ДНС представляет особый интерес для промышленности Советского Союза. В СССР интенсивно развивается производство высших жирных кислот и спиртов, получае-
|| о — очень реакционноспособное соединение.
** Сульфоянтарная кислота НООС—СН2—СН — СООН
Впервые получена Фелингом в 1841 г. сульфированием янтарной кислоты серным ангидридом.
Мых путем окисления твердых и жидких парафинов. Так как при этом получаются в основном вторичные спирты, то степень превращения их в алкилсульфаты при сульфировании серной кислотой не превышает 45—70%.
В отличие от весьма жестких условий сульфирования синтез ДНС осуществляется в мягких условиях с 92—95%-ным выходом продукта и практически не сопровождается побочными реакциями. Моющее действие средств на основе ДНС для хлопчатобумажных, шерстяных и шелковых тканей достаточно высоко.
Как на основе одних ДНС, так и в смеси с другими моющими веществами выпускаются такие моющие средства, как «Новость-С», «Ладога» и др.
Алкиларилсульфонаты. Представляют собой натровые соли алкиларилсульфокислот» общей формулы: R—Ar—S03Na. Алкиларилсульфонаты являются наиболее распространенными моющими веществами. В настоящее время объем мирового производства синтетических моющих веществ превысил 2 млн. т В год. Примерно три четверти из них составляют анионактив — ные вещества, среди которых первое место занимают алкиларилсульфонаты. В нашей стране алкиларилсульфонаты производят в основном в виде алкилбензолсульфонатов (суль- фонолы).
В СССР сульфонол получают двумя способами: хлорным и бесхлорным (сульфонолы нефтяной промышленности).
Сульфонол хлорный производится на основе керосиновой фракции нефти, выкипающей в пределах 200—300° С.
Производство сульфонола складывается из следующих стадий:
А) очистка керосина от ароматических углеводородов путем экстракции последних диэтиленгликолем;
Б) фотохимическое хлорирование очищенного керосина по схеме:
R-CHo———— СН2СН3 + С12 —————- RCH,————— СН2СН2С1 + НС1
В) алкилирование бензола хлорированным керосином в присутствии катализатора — безводного А1С13
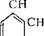
R-CH2 [СГ+Н] С F C I 1-,ю-Я5° у R — С112—С ^jj СН + НС1
Г) сульфирование алкилбензола производится раствором серного ангидрида S03 в жидком сернистом ангидриде S02 при пониженной температуре (10°С), так как процесс сульфирования протекает с большим выделением тепла
Д) нейтрализация полученных алкилбензолсульфокислот раствором каустической соды (20%-ный раствор). Температура нейтрализации не должна превышать 45—55° С.
RCH2— Ci^SGH RCH2—Cif^lCH
е) отделение несульфируемых и упаривание водных растворов сульфонола.
Выпускаемый в настоящее время хлорный сульфонол в виде 30%-ного раствора (по активному веществу) хорошо зарекомендовал себя для производства синтетических моющих порошков.
Сульфонолы нефтяной промышленности (НП)—выпускают нескольких различных видов: НП-1, НП-2, НП-3, БиТ.
Рассмотрим получение сульфонола НП-1 (додецилбензол- сульфоната): С12н25
Исходным сырьем для получения сульфонола НП-1 служат пропилен и бензол. В начале производится полимеризация пропилена на фосфорнокислом катализаторе с образованием доде — цилена (тетраметра пропилена) по схеме:
Условия полимеризации: давление 75—80 ат, температура 180—235° С.
Затем производится алкилирование бензола додециленом в присутствии А1С13 при температуре 55—60° С.
Алкилсульфаты натрия
Описание
Синонимы: Sodium alkyl sulfate, SAS
В целом, алкилсульфаты – класс органических соединений, объединенных наличием общей функциональной группы, обычно имеющих структуру R-O-SO3−. Иными словами алкилсульфаты натрия – это натриевые соли сульфоэфиров высших органических спиртов с различной длиной алкильной цепи. Первичные алкилсульфаты были и остаются одним из преобладающих типов среди синтетических анионных ПАВ. Один из наиболее известных представителей – лаурилсульфат натрия: CH3(CH2)11OSO3Na.
Основной способ получения первичных алкилсульфатов заключается в сульфатировании первичных спиртов с последующей нейтрализацией реакционной массы растворами гидроксидов натрия, аммиака или магния.
Алкилсульфаты натрия это дифильные органические соединения, которые, диссоциируя в воде, образуют анион с длинным углеводородным радикалом – носителем поверхностной активности; катион при этом не является поверхностно-активным.
Алкилсульфаты натрия выпускаются как в виде моносоединений с заданной длиной углеводородного радикала – октилсульфаты, децилсульфаты; так и в виде композиций, включающих радикалы различной длины. Алкилсульфаты натрия – малоопасное вещество. IV класс опасности по ГОСТ 12.1.007–76.
Характеристики
| Наименование | TDS | Химическое описание | Внешний вид при 20оС | Плотность при 20оС, г/см3 | Содержание активной основы, % масс. | рН 3% водного раствора |
|---|---|---|---|---|---|---|
| Syntapon O |  | Октилсульфат натрия | прозрачная желтоватая жидкость | 1,10 | 40,5 ± 0,5 | 9,5 – 11,5 |
| Syntapon OD |  | Алкилсульфат (С8–10) натрия | прозрачная желтоватая жидкость | 1,09 | 43 ± 2 | 9,5 – 11,5 |
| Syntapon NU |  | Алкилсульфат (С9–11) натрия | прозрачная желтоватая жидкость | 1,06 | 37 ± 1 | 8,0 – 10,0 |
| Syntapon DS-P |  | Децилсульфат натрия | прозрачная желтоватая жидкость | 1,02 | 36 ± 1 | 8,0 – 10,0 |
| Syntapon DS |  | Алкилсульфат (С10–12) натрия | прозрачная желтоватая жидкость | 1,02 | 36 ± 1 | 8,0 – 10,0 |
Упаковка:
— Полиэтиленовые бочки вместимостью до 220 литров
— Полимерные емкости вместимостью до 1000 литров или автоцистерны из нержавеющей стали
* По согласованию с потребителем допускается использование других видов тары.
Химия и технология поверхностно-активных веществ и синтетических моющих средств
Анионные ПАВ
Введение
Анионные ПАВ (АПАВ) – это дифильные органические соединения, ко торые, диссоциируя в воде, образуют анион с длинным углеводородным ради калом – носителем поверхностной активности; катион при этом не является по верхностно-активным. К числу основных АПАВ относятся:
— мыла RCOONa, RCOOK;
— алкилсульфаты и алкилфосфаты ROSO3Me, ROPO3Me2;
— алкиларилсульфонаты (чаще всего алкилбензолсульфо наты RC6H4SO3Me);
— алкилсульфонаты и алкилфосфонаты RSO3Me, RPO3Me2;
— алкилсульфосукцинаты
— алкилэтоксисульфаты и алкилэтоксифосфаты
Наибольшее распространение среди анионных ПАВ получили соедине ния, включающие от 10 до 20 атомов углерода в алифатической цепи. Если в алифатической цепи в качестве заместителя содержится бензольное кольцо, то
минимальное число атомов углерода снижается до 8-14. Анионоактивные ПАВ составляют более 60 % всех производимых ПАВ
для СМС. Наибольшее применение нашли натриевые, калиевые, этаноламино вые и аммониевые соли алкилкарбоновых кислот. Кроме вышеперечисленных ПАВ широко применяются сульфаты глицеридов алифатических кислот, на пример, касторового масла и сульфопроизводные моно- и диэтаноламидов али фатических кислот.
Большой интерес представляют соли полуэфиров сульфоянтарной кисло ты – сульфосукцинаты. Сульфосукцинаты служат активной основой туалетных мыл, синтетических кусковых и пастообразных моющих средств, шампуней и пенных препаратов для ванн.
Химия и технология поверхностно-активных веществ и синтетических моющих средств
Анионные ПАВ
Введение
Анионные ПАВ (АПАВ) – это дифильные органические соединения, ко торые, диссоциируя в воде, образуют анион с длинным углеводородным ради калом – носителем поверхностной активности; катион при этом не является по верхностно-активным. К числу основных АПАВ относятся:
— мыла RCOONa, RCOOK;
— алкилсульфаты и алкилфосфаты ROSO3Me, ROPO3Me2;
— алкиларилсульфонаты (чаще всего алкилбензолсульфо наты RC6H4SO3Me);
— алкилсульфонаты и алкилфосфонаты RSO3Me, RPO3Me2;
— алкилсульфосукцинаты
— алкилэтоксисульфаты и алкилэтоксифосфаты
Наибольшее распространение среди анионных ПАВ получили соедине ния, включающие от 10 до 20 атомов углерода в алифатической цепи. Если в алифатической цепи в качестве заместителя содержится бензольное кольцо, то
минимальное число атомов углерода снижается до 8-14. Анионоактивные ПАВ составляют более 60 % всех производимых ПАВ
для СМС. Наибольшее применение нашли натриевые, калиевые, этаноламино вые и аммониевые соли алкилкарбоновых кислот. Кроме вышеперечисленных ПАВ широко применяются сульфаты глицеридов алифатических кислот, на пример, касторового масла и сульфопроизводные моно- и диэтаноламидов али фатических кислот.
Большой интерес представляют соли полуэфиров сульфоянтарной кисло ты – сульфосукцинаты. Сульфосукцинаты служат активной основой туалетных мыл, синтетических кусковых и пастообразных моющих средств, шампуней и пенных препаратов для ванн.
Алкилсульфат/лаурилсульфат натрия
Алкилсульфат натрия (натриевая соль алкилсульфата фракции С12-С14) является водным раствором поверхностно – активных веществ (ПАВ) анионного типа.
Сферы применения алкилсульфата /лаурилсульфата натрия
Алкилсульфаты (лаурилсульфаты натрия) активно используются в качестве компонентов при изготовлении:
Благодаря оптимальному соотношению цены и качества алкилсульфат натрия (ВЖC) С12-С14 является отличным заменителем для аналогов российского и зарубежного производаства: АБСК, Texapon, Hostapur, и т.д.
Физико-химические показатели алкилсульфатов / лаурилсульфата натрия
Нормативное значение показателя
Внешний вид при 20-25 °С
Однородная прозрачная подвижная жидкость от желтого до коричневого цвета без механических примесей
Водородный показатель (рН)
Концентрация, %, не менее
Массовая доля веществ, растворимых в петролейном эфире, %
Алкилсульфат натрия (лаурилсульфат натрия) является малоопасным веществом, относящимся к IV-му классу опасности согласно ГОСТ 12.1.007.
В ходе использования алкилсульфата натрия вторич¬ные опасные соединения не образуются.
Сброс алкилсульфата натрия (лаурилсульфата натрия) в производственные сточные воды допускается при условии разбавления его водой до предельно-допустимой концентрации ПАВ 20 мг/дм³ по активному веществу.
Важно! Работа с алкилсульфатом натрия (лаурилсульфатом натрия) предполагает обязательное использование средств индивидуальной защиты кожи и слизистой оболочки глаз. При контакте вещества с кожей или слизистыми место соприкосновения следует тщательно промыть водой.
Транспортировка и хранение
Хранение алкилсульфатов (лаурилсульфатов натрия) рекомендуется осуществлять при температуре выше 0 °С. Однако в случае неоднократного замерзания и последующего оттаивания вещество не теряет своих первоначальных слов.
Поставки осуществляются в полиэтиленовых канистрах объемом от 5 до 30 л, а также пластиковых или металлических бочках по 200—225 кг.
Срок хранения: 12 месяцев со дня изготовления при соблюдении надлежащих условий транспортировки и хранения.
Согласно классификации ГОСТ 19433 вещество не относится к опасным грузам и может транспортироваться всеми видами транспорта.