амикацин или цефепим что лучше
Цефепим: при каких заболеваниях рекомендуется купить
Антибактериальное средство нового поколения, действенное против патогенов широкого спектра. Применяется по назначению врача в стационарных и амбулаторных условиях короткими курсами, редко вызывает резистентность микробов.
Состав и лекарственная форма
Медикамент имеет единственную фармацевтическую форму — порошок для приготовления внутримышечных и внутривенных инъекций. Лекарства для приема перорально не существует. Сухая смесь содержит активный компонент — цефепима гидрохлорид, который относится к антибактериальным средствам цефалоспоринового класса. Это четвертое поколение веществ, оказывающих более быстрый и долговременный терапевтический эффект.
Микрокристаллический порошок белого цвета расфасован в стеклянные флаконы. Одна доза содержит 0,5 или 1 г. цефалоспорина и стабилизирующие добавки. Перед использованием препарат необходимо разводить дистиллированной водой, физраствором или лидокаином.
Механизм действия
Цефепим, проникая в кровь и мягкие ткани, оказывает выраженное бактерицидное действие: разрушает клеточные мембраны и белки грамположительных, а также грамотрицательных бактерий. Препарат не дает возможности патогенам приспособиться к лекарственному веществу и выработать к нему устойчивость, уничтожая их уже при первом контакте.
Цефепим оказывается эффективным там, где не действуют аминогликозиды и антибиотики других групп. Его назначают при инфицировании стрептококками, клебсиеллами, протеем, клостридиями и другими видами болезнетворной микрофлоры.
Показания к использованию
Лекарственное средство назначают:
при бактериальной пневмонии: средней и тяжелой степени тяжести, если патология вызвана чувствительными к цефалоспоринам микробами;
при фебрильной нейропении;
при инфекционных поражениях почек и воспалениях мочевыводящих путей, протекающих осложненно или без серьезных осложнений;
при кожных инфекциях, а также при воспалениях прилегающих к ним мягких тканей;
при инфекционных процессах органов брюшной полости и малого таза: в составе комплексного лечения, в сочетании с другими антибиотиками.
При необходимости Цефепим применяют в педиатрической практике: с возраста 2 месяцев.
Противопоказания
Отказаться от терапии препаратом необходимо при индивидуальной повышенной чувствительности к его компонентам. Она может проявляться покраснением кожи, пятнами, крапивницей, отечностью покровов и слизистых оболочек, раздражением, усиленным зудом. В тяжелых случаях развивается отек Квинке.
возраст младше 2 месяцев;
язвенная болезнь желудка и язвенный колит в стадии обострения;
тяжелая почечная недостаточность;
хронические нарушения системы кроветворения;
Побочные действия
На фоне использования антибиотика вероятны нежелательные реакции со стороны различных систем организма:
болезненность в месте постановки уколов;
головные боли, головокружения;
функциональные нарушения в работе почек;
тошнота, боли и спазмы в области желудка, запоры, метеоризм;
снижение количества тромбоцитов, лейкопения, снижение свертываемости крови;
аритмические проявления, скачки артериального давления;
физическая слабость, сонливость в дневные часы;
загрудинные и спинные боли.
При резком ухудшении самочувствия вопрос о продолжении лечения обсуждается с медицинским специалистом. При признаках непереносимости препарат отменяют.
Как применять Цефепим
Для приготовления внутривенных раствора содержимое флакона разводят с физиологическим раствором или дектрозой до исчезновения осадка. При внутримышечном введении порошок смешивают с водой для инъекций с содержанием спирта и других добавок. Допускается также соединение антибиотика с раствором лидокаина. Лекарство запрещено соединять в одном шприце или капельной системе с другими антибактериальными средствами.
Однократная доза медикамента составляет от 0,5 до 2 г, в зависимости от вида заболевания.
Внутривенные инфузии и уколы применяют преимущественно при лечении средних и тяжелых форм пневмонии, инфекций мочеполовой системы, фебрильной нейтропении. Начальные суточные дозы при этом максимальны: до 2 г. в сутки. В последующие дни допускается снижать дозировку до 0,5 г.
Внутримышечно Цефепим используют реже, обычно при неосложненных инфекциях внутренних органов, при лечении кожных заболеваний, в педиатрической практике.
Продолжительность курса определяют индивидуально. Для полного подавления инфекционного процесса требуется от 7 до 10 суток. Не допускается самовольное прерывание инъекций, так как это может спровоцировать дальнейшее развитие резистентности микробов и трудности с выбором подходящих медикаментов.
Цефепим несовместим с препаратами, содержащими гепарин. При назначении страдающим нарушениями почек требуется врачебный контроль за физическим состоянием и лабораторными показателями.
Аналоги и стоимость
Аналогичные Цефипиму антибактериальные препараты класса цефалоспоринов четвертого поколения: Максипим, Эфипим, Ладеф, Мовизар, Ценим.
Купить медикамент в аптечных сетях можно по цене от 100 до 200 рублей за один флакон.
Все представленные на сайте материалы предназначены исключительно для образовательных целей и не предназначены для медицинских консультаций, диагностики или лечения. Администрация сайта, редакторы и авторы статей не несут ответственности за любые последствия и убытки, которые могут возникнуть при использовании материалов сайта.
Аминогликозиды с позиций современной практики лечения инфекций дыхательных путей
Появление аминогликозидных антибиотиков ведет свое начало с открытия исследовательской группой Зельмана Ваксмана в 1943 году стрептомицина — первого препарата, активного в отношении Mycobacterium tuberculosis [1].
Появление аминогликозидных антибиотиков ведет свое начало с открытия исследовательской группой Зельмана Ваксмана в 1943 году стрептомицина — первого препарата, активного в отношении Mycobacterium tuberculosis [1]. За столь выдающееся открытие Ваксман в 1952 году был удостоен Нобелевской премии, при вручении которой было отмечено, что «в отличие от открытия пенициллина профессором Александером Флемингом, которое было в значительной степени обусловлено случаем, получение стрептомицина было результатом длительного, систематического и неутомимого труда большой группы ученых».
Впоследствии на основе природных структур, продуцируемых различными представителями актиномицетов (природные антибиотики), и в ряду их полусинтетических производных была разработана большая группа антибактериальных препаратов, которые составили класс аминогликозидов. В настоящее время выделяют три поколения аминогликозидов (табл. 1). К первому поколению относят стрептомицин, неомицин, канамицин и мономицин, применение которых на современном этапе ограничено вследствие их токсичности. Второе поколение составляют гентамицин, тобрамицин, сизомицин и нетилмицин. Амикацин и исепамицин входят в третье поколение аминогликозидов.
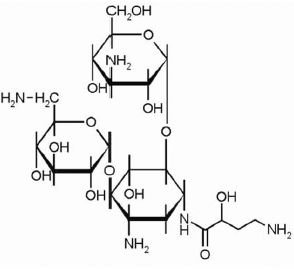
Название данной группы антибиотиков обусловлено молекулярной структурой, в основе которой присутствуют аминосахара, связанные гликозидной связью с агликоновой частью молекулы (рис. 1).
Механизм действия аминогликозидов связан с необратимым угнетением синтеза белка на уровне рибосом у чувствительных к ним микроорганизмов. В отличие от других ингибиторов синтеза белка аминогликозидные антибиотики оказывают не бактериостатическое, а именно бактерицидное действие. Аминогликозиды II и III поколений обладают широким спектром антимикробного действия, в первую очередь, в отношении большинства грамотрицательных микроорганизмов семейства Enterobacteriaceae (Escherichia coli, Proteus spp., Klebsiella spp., Enterobacter spp., Serratia spp. и др.), а также неферментирующих грамотрицательных палочек (Pseudomonas aeruginosa, Acinetobacter spp.) [2, 3, 4]. Аминогликозиды также проявляют свою активность в отношении Staphylococcus aureus, кроме метициллинрезистентных штаммов (MR). Отдельные представители класса различаются между собой по активности и спектру действия. В частности, аминогликозиды I поколения (стрептомицин, канамицин) проявляют наибольшую активность в отношении M. tuberculosis, мономицин обладает эффективностью против некоторых простейших. Все аминогликозиды II и III поколения активны в отношении P. aeruginosa, при этом тобрамицин проявляет наивысшую активность. Сизомицин характеризуется большей активностью, чем гентамицин в отношении Proteus spp., Klebsiella spp., Enterobacter spp. (табл. 2).
Одним из наиболее эффективных аминогликозидов является амикацин, что связано с устойчивостью к действию ферментов, инактивирующих другие аминогликозиды, поэтому антибиотик может оставаться активным в отношении штаммов P. aeruginosa, устойчивых к тобрамицину, гентамицину и нетилмицину [2, 5, 12]. Другой представитель III поколения — изепамицин дополнительно активен в отношении Aeromonas spp., Citrobacter spp., Listeria spp. и Nocardia spp.
Все представители класса аминогликозидов неактивны в отношении S. pneumoniae, S. maltophilia, B. cepacia и анаэробов (Bacteroides spp., Clostridium spp. и др.). Более того, следует помнить, что резистентность S. pneumoniae, S. maltophilia и B. cepacia к аминогликозидам используется при идентификации этих микроорганизмов. Аминогликозиды in vitro активны в отношении шигелл, сальмонелл, легионелл, однако их назначение при данных инфекциях недопустимо, так как они клинически неэффективны в отношении возбудителей, локализованных внутриклеточно [2].
В ряде случаев аминогликозиды оказывают постантибиотический эффект, который зависит от штамма микроорганизма и концентрации препарата в очаге инфекции.
Все аминогликозиды характеризуются практически одинаковой фармакокинетикой (табл. 3). Молекулы антибиотиков являются высокополярными соединениями, в связи с чем плохо растворяются в липидах и при приеме внутрь практически не всасываются из желудочно-кишечного тракта (в системный кровоток поступает менее 2%). Вследствие этого основной путь введения аминогликозидов парентеральный (кроме неомицина). Связывание аминогликозидов с белками крови низкое и колеблется для разных антибиотиков от 0 до 30% (например, тобрамицин практически не связывается с белками). Время достижения Cmax при в/м введении составляет 1–1,5 ч. Аминогликозиды практически не подвергаются биотрансформации, выводятся почками путем клубочковой фильтрации в неизмененном виде, создавая высокие концентрации в моче. Скорость экскреции зависит от возраста, функции почек и сопутствующей патологии пациента (например, при лихорадке она увеличивается, с большой скоростью препарат элиминируется у наркоманов, с меньшей — у беременных, при понижении функции почек скорость экскреции значительно замедляется). Период полувыведения всех аминогликозидов у взрослых с нормальной функцией почек составляет 2–4 ч, при почечной недостаточности период может возрастать до 70 ч и более. Пиковые концентрации аминогликозидов варьируют у различных пациентов и зависят от массы тела, объема жидкости и жировой ткани, состояния пациента. Например, у пациентов с обширными ожогами, асцитом объем распределения аминогликозидов повышен. Наоборот, при дегидратации или мышечной дистрофии он уменьшается.
Аминогликозиды способны создавать высокие концентрации в органах с хорошим кровоснабжением: печени, легких, почках, напротив, низкие концентрации отмечаются в мокроте, бронхиальном секрете, желчи, грудном молоке. Аминогликозиды плохо проходят через гематоэнцефалический барьер, однако при воспалении мозговых оболочек их проницаемость увеличивается.
Учитывая особенности фармакокинетики аминогликозидов, а также потенциальную специфическую токсичность данного класса антибиотиков, необходимо правильно рассчитывать дозу применяемых препаратов. Доза аминогликозидов (не только у детей, но и у взрослых!) должна рассчитываться исходя из массы тела с обязательным учетом индивидуальных особенностей пациента (возраст, функция почек, локализация инфекции).
Факторами, определяющими дозу аминогликозидов, являются [2]:
Дозы у взрослых и детей старше 1 месяца: стрептомицин, канамицин, амикацин по 15–20 мг/кг/сутки в 1–2 введения; гентамицин, тобрамицин — 3–5 мг/кг/сутки в 1–2 введения; нетилмицин — 4–6,5 мг/кг/сутки в 1–2 введения.
Современная практика применения аминогликозидов предусматривает введение препарата 1 раз в сутки, что оправдано как с микробиологической точки зрения (дозозависимый, быстро наступающий бактерицидный эффект; длительный постантибиотический эффект), так и с клинической (меньшая токсичность аминогликозидов при однократном введении при аналогичной эффективности терапии) [2, 3]. В настоящее время однократное в сутки введение аминогликозидов применяется при большинстве показаний (исключение составляют эндокардит и менингит). При однократном введении аминогликозиды лучше всего вводить внутривенно капельно в течение 15–20 мин.
Чрезвычайно важно, что аминогликозиды характеризуются вариабельностью фармакокинетических показателей. При введении одинаковой дозы потенциально токсические уровни в крови (10–14 мкг/мл) для природных аминогликозидов могут быть обнаружены в среднем у 10% больных, концентрации ниже необходимых для адекватной терапии выявляются у 25% больных и более [3]. В этой связи наиболее предпочтительными являются полусинтетические препараты — амикацин и нетилмицин, обладающие наименьшей вариабельностью показателей. Кроме того, данной группе препаратов свойствен узкий коридор безопасности, т. е. незначительный разрыв между эффективным и токсическим уровнем концентраций в крови. В этой связи единственным средством оптимизации лечения аминогликозидами является постоянный фармакокинетический мониторинг, который позволяет исключать создание токсических или субтерапевтических уровней препарата в крови (табл. 4).
При проведении терапевтического мониторинга определяют: 1) пиковую концентрацию аминогликозидов в сыворотке крови — через 60 мин после внутримышечного введения препарата или через 15 мин после окончания внутривенного введения; 2) остаточную концентрацию — перед введением очередной дозы. Установление пиковой концентрации не ниже порогового значения свидетельствует о достаточности используемой дозы аминогликозида, при этом ее высокие уровни не представляют опасности для пациента. Величина остаточной концентрации, превышающая терапевтический уровень, свидетельствует о кумуляции препарата и об опасности развития токсических эффектов. В этом случае снижают суточную дозу или удлиняют интервал между разовыми дозами. При однократном введении всей суточной дозы достаточно определять только остаточную концентрацию [2].
Аминогликозиды относятся к препаратам с низким уровнем общей токсичности. Однако для них характерны специфические нежелательные реакции, а именно ото- и нефротоксичность. Частота развития этих реакций варьирует в зависимости от препарата. В клинических исследованиях было показано, что частота развития нефротоксических явлений при применении нетилмицина составляет 2,8%, амикацина — 8,5%, гентамицина — 11,1% и тобрамицина — 11,5% [9]. Ототоксические реакции наблюдаются у 2,3% пациентов, получавших нетилмицин, у 7,7%, получавших гентамицин, 9,7% — тобрамицин и 13,8% — амикацин [9]. Ототоксичность проявляется как в виде вестибулярных нарушений (чаще при применении стрептомицина, гентамицина, тобрамицина), так и в виде нарушения слуха (амикацин, нетилмицин). Нарушение слуха и поражение преддверно-улиткового нерва могут оказаться необратимыми, вероятность данных реакций возрастает с повышением дозы препарата, при длительных курсах лечения, у больных пожилого возраста и пациентов с исходными нарушениями функции слухового аппарата. Нарушения функции почек при применении аминогликозидов, напротив, чаще всего обратимы. Высокой нефротоксичностью обладает гентамицин, наиболее безопасными препаратами являются амикацин и нетилмицин. В ряде случаев применение аминогликозидов сопровождается нарушением нервно-мышечной проводимости, развитием парестезий, периферических нейропатий.
С точки зрения профилактики развития побочных реакций наибольшее значение имеет отмеченный ранее контроль основных фармакокинетических параметров, которые должны быть ограничены заданными пределами (табл. 3 и 4). Одновременное применение аминогликозидов с другими лекарственными препаратами, выводящимися из организма путем почечной экскреции, также относится к числу факторов риска, влияющих на частоту или степень проявления нежелательных реакций. Аминогликозиды не рекомендуется применять вместе с амфотерицином В, цисплатином, миорелаксантами и ванкомицином.
На протяжении длительного времени аминогликозиды относятся к широко применяемым антибактериальным препаратам и входят в стандарты лечения инфекций различной локализации (табл. 5). На современном этапе практическое значение данной группы антибиотиков, в первую очередь, связано с лечением нозокомиальных инфекций, вызываемых преимущественно грамотрицательными микроорганизмами. Основными показаниями к применению аминогликозидов II и III поколения являются тяжелые инфекции: сепсис, септический эндокардит, остеомиелит, инфекции кожи и мягких тканей, нозокомиальная пневмония, генерализованные формы раневой и ожоговой инфекции, перитонит, послеоперационные гнойные осложнения, инфекции почек и мочеполовых путей и др. В большинстве случаев аминогликозиды назначаются в комбинации с бета-лактамными и антианаэробными антибиотиками. Следует отметить, что в качестве средства эмпирической терапии может служить только амикацин, поскольку к нему сохраняют высокую чувствительность более 70% штаммов грамотрицательных бактерий. Назначение других аминогликозидов рекомендовано после подтверждения чувствительности к гентамицину или конкретному антибиотику выделяемых возбудителей.
Резистентность микроорганизмов к аминогликозидам
К сожалению, более чем полувековое использование аминогликозидов, в том числе по необоснованным показаниям (внебольничные инфекции дыхательных путей и пр.), привело к возникновению и распространению устойчивых к ним штаммов микроорганизмов [10]. В частности, в России уровень резистентности к аминогликозидам, прежде всего к гентамицину, превышает таковой в большинстве других стран [11].
Формирование устойчивости к аминогликозидам обусловлено в первую очередь ферментативной инактивацией антибиотиков путем модификации [11, 12]. Модифицированные молекулы теряют способность связываться с рибосомами и подавлять синтез белка микроорганизмов. Известны три группы аминогликозидмодифицирующих ферментов (АМФ): ацетилтрансферазы (ААС), присоединяющие молекулу уксусной кислоты, фосфортрансферазы (АРН), присоединяющие молекулу фосфорной кислоты, нуклеотидил- или аденилилтрансферазы (ANT), присоединяющие молекулу нуклеотида аденина (табл. 6). В целом именно гентамицин является субстратом для значительно большего количества АМФ, чем другие аминогликозиды II и III поколения, что определяет высокий уровень резистентности к данному антибиотику. Напротив, возможность модифицирования амикацина обуславливает наименьшее среди аминогликозидов количество АМФ, поэтому к нему сохраняют чувствительность ряд бактерий, резистентных к гентамицину, нетилмицину и другим препаратам этой группы.
Согласно данным по антибиотикорезистентности в России за период 2002–2004 гг., чрезвычайно высокая резистентность нозокомиальных штаммов P. aeruginosa и Klebsiella pneumoniae наблюдалась к гентамицину, составляя 74,9% и 76,5% соответственно — рис. 2, рис. 3 [13]. Наиболее активен в отношении данных возбудителей амикацин, к которому нечувствительны до 35,8% штаммов K. pneumoniae и 42,9% P. aeruginosa.
В другом же исследовании (Micromax), проведенном в стационарах Москвы, Смоленска и Екатеринбурга частота выделения нечувствительных к амикацину штаммов P. aeruginosa и K. pneumoniae составила 11% и 10,8% соответственно [14]. В этой связи чрезвычайно важно руководствоваться именно локальными данными по антибиотикорезистентности возбудителей.
Применение аминогликозидов в лечении инфекций дыхательных путей
В связи с тем, что аминогликозиды не обладают активностью в отношении основного возбудителя внебольничных инфекций дыхательных путей — S. pneumoniae, их нельзя использовать для лечения внебольничной пневмонии (как в амбулаторной, так и стационарной практике) и других внебольничных инфекций верхних и нижних отделов респираторного тракта. Пожалуй, единственной клинической ситуацией, оправдывающей назначение аминогликозидов, является тяжелая внебольничная пневмония, вызванная P. aeruginosa. В данном случае применяются цефтазидим, цефепим, цефоперазон/сульбактам, тикарциллин/клавуланат, пиперациллин/тазобактам, карбапенемы (меропенем, имипенем) или ципрофлоксацин либо в режиме монотерапии или комбинации с аминогликозидами II–III поколения (предпочтительным является применение амикацина) [15].
Абсцесс легкого и эмпиема плевры
Потенциальными возбудителями абсцесса легкого являются анаэробные микроорганизмы — Fusobacterium nucleatum, Peptostreptococcus spp., Bacteroides spp. либо ассоциации анаэробных и аэробных бактерий (в первую очередь, представители семейства Enterobacteriacea — K. pneumoniae и K. оxytoca) [16]. Российские эксперты в качестве препаратов выбора рекомендуют применение ингибиторозащищенных аминопенициллинов (амоксициллин/клавуланат, ампициллин/сульбактам) либо цефоперазон/сульбактама. При отсутствии этих антибиотиков либо их неэффективности могут использоваться карбапенемы, ингибиторозащищенные пенициллины (тикарциллин/клавуланат, пиперациллин/тазобактам) либо комбинации клиндамицина с аминогликозидами II и III поколения [17].
В этиологии эмпиемы плевры ведущую роль занимают грамотрицательные бактерии (15–32%) и анаэробы (5–19%). На долю S. aureus приходится от 7 до 15% случаев, S. pneumoniae выделяется у 5–7% больных, еще реже встречается H. influenzae. В 20–25% случаев обнаруживают микробные ассоциации, прежде всего, анаэробов и аэробов, представленных грамотрицательными бактериями [18]. Антибактериальная терапия должна, по возможности, проводится целенаправленно, т. е. с учетом данных микробиологического исследования содержимого плевральной полости. При острой постпневмонической эмпиеме плевры, вызванной S. pneumoniae и S. pyogenes, в качестве препаратов выбора используются цефалоспорины ІІ–ІV поколений в режиме монотерапии. Альтернативой им являются линкосамиды или ванкомицин. При стафилококковой острой постпневмонической эмпиеме применяют оксациллин либо цефазолин, в качестве альтернативы рассматриваются линкосамиды, фузидиевая кислота, ванкомицин и линезолид. В случае острой постпневмонической эмпиемы плевры, вызванной Haemophilus influenzae, препаратами выбора являются цефалоспорины III или IV поколения. Альтернативой им являются «защищенные» аминопенициллины (амоксициллин/клавуланат, ампициллин/сульбактам) или фторхинолоны.
В этиологии подострой и хронической эмпиемы плевры ведущую роль занимают анаэробные стрептококки, бактероиды, часто в ассоциации с микроорганизмами семейства Enterobacteriaceae. Препаратами первой линии в данном случае являются «защищенные» аминопенициллины — амоксициллин/клавуланат или ампициллин/сульбактам. В качестве препаратов альтернативы рекомендуются линкосамид в сочетании с аминогликозидом II или III поколения, либо цефалоспорины II–IV генерации, либо карбапенемы (имипенем, меропенем), либо тикарциллин/клавуланат или пиперациллин/тазобактам [17]. При эмпиеме плевры, как правило, без хирургического вмешательства невозможно добиться излечения пациента, и в большинстве случаев требуется торакотомическое дренирование, реже применяется торакоскопия и декортикация.
Нозокомиальная пневмония
Нозокомиальная пневмония (НП) занимает второе место среди всех нозокомиальных инфекций (13–18%) и является самой частой инфекцией (≥ 45%) в отделениях реанимации и интенсивной терапии (ОРИТ) [19, 23]. НП развивается в среднем у 0,5–1% всех госпитализированных больных и у 10–20% госпитализированных в ОРИТ. Особая категория НП у пациентов, находящихся на искусственной вентиляции легких (вентиляторассоциированная пневмония — ВАП), развивается у 9–27% от общего числа интубированных. По показателю смертности НП лидирует среди нозокомиальных инфекций, вызывая летальные исходы в среднем от 30 до 70% пациентов [20, 21].
НП наиболее часто вызывается аэробными грамотрицательными микроорганизмами — P. aeruginosa, E. coli, K. pneumoniae и Acinetobacter spp. (рис. 4). В последнее время отмечается увеличение частоты обнаружения S. aureus, в том числе МR (MRSA) [21]. Большинство случаев НП имеет полимикробную этиологию [22]. Частота встречаемости полирезистентных возбудителей зависит от популяции пациентов (чаще всего у больных с тяжелыми хроническими заболеваниями, факторами риска развития пневмонии и поздним развитием пневмонии > 5 дней), стационара и типа отделения, что свидетельствует о крайней необходимости получения локальных данных.
При выборе антибиотиков для эмпирической антибактериальной терапии НП необходимо ориентироваться в первую очередь на локальные данные по антибиотикорезистентности возбудителей. Необходимо помнить, что эти данные нуждаются в периодическом обновлении, так как устойчивость бактерий может изменяться с течением времени в зависимости от структуры и частоты использования антибиотиков.
В настоящее время рекомендован подход к антибиотикотерапии НП в зависимости от сроков развития заболевания. При ранней НП (≤ 5 дней), развившейся у пациентов без факторов риска, применяют цефалоспорины III и IV поколения, амоксициллин/клавуланат, левофлоксацин, моксифлоксацин, ципрофлоксацин и эртапенем в режиме монотерапии.
Напротив, у пациентов с поздней (> 5 дней) НП или при наличии факторов риска полирезистентных возбудителей рекомендована комбинированная терапия — антисинегнойный цефалоспорин или карбапенем или цефоперазон/сульбактам в сочетании с амикацином или фторхинолоном с синегнойной активностью.
Аминогликозиды также применяются в комбинации с карбапенемом при НП установленной этиологии, в частности, вызванной E. coli, K. pneumoniae, другими грамотрицательными микро-
организмами (Enterobacter spp., Morganella spp., Serratia spp.), P. aeruginosa или Acinetobacer spp. (табл. 7).
Традиционная длительность терапии НП составляет 14–21 день, однако современная тактика ведения пациентов с ВП предусматривает сокращение длительности антибиотикотерапии до 7 дней в случае эффективной начальной эмпирической терапии [21]. При использовании аминогликозидов для комбинированной эмпирической терапии, их применение может быть прекращено через 5–7 дней у пациентов с клинической эффективностью лечения.
В заключение необходимо еще раз отметить, что применение аминогликозидов для лечения внебольничных инфекций дыхательных путей недопустимо, при внутрибольничных инфекциях аминогликозиды (нетилмицин, амикацин) должны использоваться только лишь в определенных клинических ситуациях и только в комбинации с другими антибактериальными препаратами.