антиандрогены что это для мужчин
Антиандрогенная терапия: за и против
В соответствие с данными статьи, опубликованной в июньском номере журнала New England Journal of Medicine, длительная супрессия андрогенов у больных местно распространенным раком предстательной железы, получающих лучевую терапию, имеет преимущества по показателям выживаемости по сравнению с андрогенной супресссией коротким курсом.
В соответствии с данными статьи, опубликованной в июньском номере журнала New England Journal of Medicine, длительная супрессия андрогенов у больных местнораспространенным раком предстательной железы, получающих лучевую терапию, имеет преимущества по показателям выживаемости по сравнению с андрогенной супресссией коротким курсом.
По данным исследования, в котором участвовали больные раком предстательной железы стадии Т2с и более, супрессия андрогенов в течение 3х лет позволяет добиться лучших показателей выживаемости, чем прием антиандрогенов в течение 6 месяцев.
Что также является важным, не было отмечено повышения риска смертельных сердечно-сосудистых осложнений при пролонгированном курсе антиандрогенной терапии, в отличие от предыдущего подобного исследования.
Таким образом, исследователи рекоммендуют сочетать лучевую терапию с длительным приемом антиандрогенов больным местнораспространенным раком предстательной железы (со стадией Т2с и более по классификации TNM)».
Однако антиандрогенная терапия также имеет достаточно широкий спектр побочных эффектов, которые могут значительно сказываться на качестве жизни пациентов. Необходимость проведения более длительных курсов лечения и расширения показаний к её использованию вызывает сомнения у многих специалистов. Так, доктор Вильям Дейл из Чикагского Университета пишет в статье Journal of Clinical Oncology: «Становится очевидным злоупотребление использованием антиандрогенной терапии при лечении рака простаты». Так же считает доктор Альбертсен из Университета при Connecticut Health Center, о чем пишет в статье New England Journal of Medicine. И доктор Дейл, и доктор Альбертсен отмечают, что применение антиандрогенной терапии у мужчин с диагнозом метастатического рака простаты, а также в сочетании с лучевой терапий при лечении местнораспространённого заболевания, действительно, увеличивает выживаемость, однако данные преимущества представляются сомнительными при других стадиях заболевания.
Таким образом, антиандрогенная терапия является эффективным, но достаточно токсичным методом лечения, требующим дальнейшего изучения. При её назначении врач-онколог должен принять в расчёт как её потенциальную пользу для пациента, так и влияние на качество жизни и возможное развитие осложнений. Каждый случай должен рассматриваться индивидуально с учётом стадии заболевания, возраста, наличия негативных или благоприятных прогностических факторов. В настоящее время есть наиболее чёткие показания для её назначения больным метастатическим раком простаты, молодым пациентам с агрессивными формами заболевания, а также в сочетании с лучевой терапией при его местнораспространённых формах.
Антагонисты мужских половых гормонов (антиандрогены)
Смотри также диане, нилутамид, проскар, серпенс, флутамид.
ЦИПРОТЕРОН (Cyproterone)
Синонимы: Андрокур, Андрокурдепо, Ципроиеторонацетат.
Показания к применению. У мужчин: контроль полового влечения в случае сексуальных отклонений. У женщин: тяжелые явления андрогенизации (пояштение мужских черт). У детей: идиопатическая (неясного происхождения) преждевременная половая зрелость.
Способ применения и дозы. Мужчинамс патологически измененным половым поведением и повышенным половым влечением назначают по 1 таблетке 2 раза в день, реже по 2 таблетки 2 раза в день или временно по 2 таблетке 3 раза в день. Ципротерон-депо вводят внутримышечно во 3 мл (1 ампула) каждые 10-14 дней. При необходимости доза препарата может быть увеличена до 6 мл (2 ампулы) каждые 10-14 дней. При такой дозировке предпочтительно введение по 3 мл (1 ампула) в каждую ягодицу. В случае достижения удовлетворительного терапевтического эффекта доза препарата может быть снижена, с одновременным и постепенным увеличением временных интервалов между инъекциями. Обычно курс лечения продолжается несколько месяцев. При необходимости лечение препаратом сочетают с психотерапевтическими мероприятиями.
Женщинам препарат назначают только внутрь в комбинации с препаратом диане-35. Детям препарат назначают только внутрь по специальным схемам.
Условия хранения. Список Б. В сухом месте.
Заместительная гормональная терапия для мужчин с возрастным андрогенным дефицитом
Специализация: урология, андрология
Синдром возрастного андрогенодефицита у мужчин — это нарушение биохимического баланса, возникающее в зрелом возрасте по причине недостаточности андрогенов в сыворотке крови, нередко сопровождающейся снижением чувствительности организма к андрогенам. Как правило, это приводит к значительному ухудшению качества жизни и неблагоприятно сказывается на функциях практически всех систем организма. Естественно, что огромный интерес вызывают вопросы терапии андрогенного дефицита, поскольку именно она ставит сложную задачу перед врачом-клиницистом: выбрать из широкого арсенала методов и препаратов гормональной терапии наиболее оптимальный, сочетающий в себе качество, эффективность, а также удобство в применении.
В настоящее время врачи-урологи и андрологи наиболее часто применяют заместительную терапию тестостероном. Данный метод позволяет решить целый ряд задач: снизить симптомы возрастного андрогенодефицита путем повышения либидо, общей сексуальной удовлетворенности, уменьшить выраженность либо полностью ликвидировать вегетососудистые и психические расстройства. Кроме того, если заместительная терапия тестостероном применяется более 1 года, у пациентов наблюдается повышение плотности костной массы, снижение выраженности висцерального ожирения, а также нарастание мышечной массы. Также после длительного курса лечения нормализуются лабораторные параметры: наблюдается повышение уровня гемоглобина или количества эритроцитов, снижение уровня ЛПОНП (липопротеинов очень низкой плотности) и ЛПНП (липопротеинов низкой плотности) при неизмененном уровне ЛПВП (липопротеинов высокой плотности). Многие авторы считают, что такого эффекта можно достичь, добившись восстановления концентрации тестостерона в крови до нормального уровня (10–35 нмоль/л). Следует также учитывать, что *17α-алкилированные препараты тестостерона флуоксиместеролон и метилтестостерон обладают выраженной гепатотоксичностью, оказывая токсическое и канцерогенное влияние на печень, а также отрицательно воздействуют на липидный спектр крови (резкое повышение уровня атерогенных и снижение уровня антиатерогенных липопротеидов). Поэтому применение этих производных тестостерона в клинической практике было прекращено.
В настоящее время из пероральных препаратов предпочтение отдается тестостерону ундеканоату (Андриол). Указанный эфир тестостерона не подвергается первичному печеночному метаболизму, так как всасывается в лимфатическую систему, минуя печень. После гидролиза тестостерона ундеканоата в лимфатической системе в системный кровоток поступает тестостерон, который оказывает лечебное действие как сам по себе, так и через свои основные метаболиты – дигидротестостерон (ДГТ) и эстрадиол, обусловливающие полный спектр андрогенной активности тестостерона. Таким образом, тестостерона ундеканоат сохраняет свою активность при пероральном применении. Вместе с этим, минуя систему воротной вены и прохождение через печень, тестостерона ундеканоат не оказывает гепатотоксического и гепатоканцерогенного действия. Период полувыведения препарата из плазмы составляет 3–4 часа. В связи с этим режимом дозировки тестостерона ундеканоата является 2-кратный прием в течение суток, это не всегда удобно для пациентов. Исходя из собственного опыта, мы считаем, что Андриол является достаточно мягким препаратом и помогает только в случаях начальных и минимальных проявлений возрастного андрогенного дефицита.
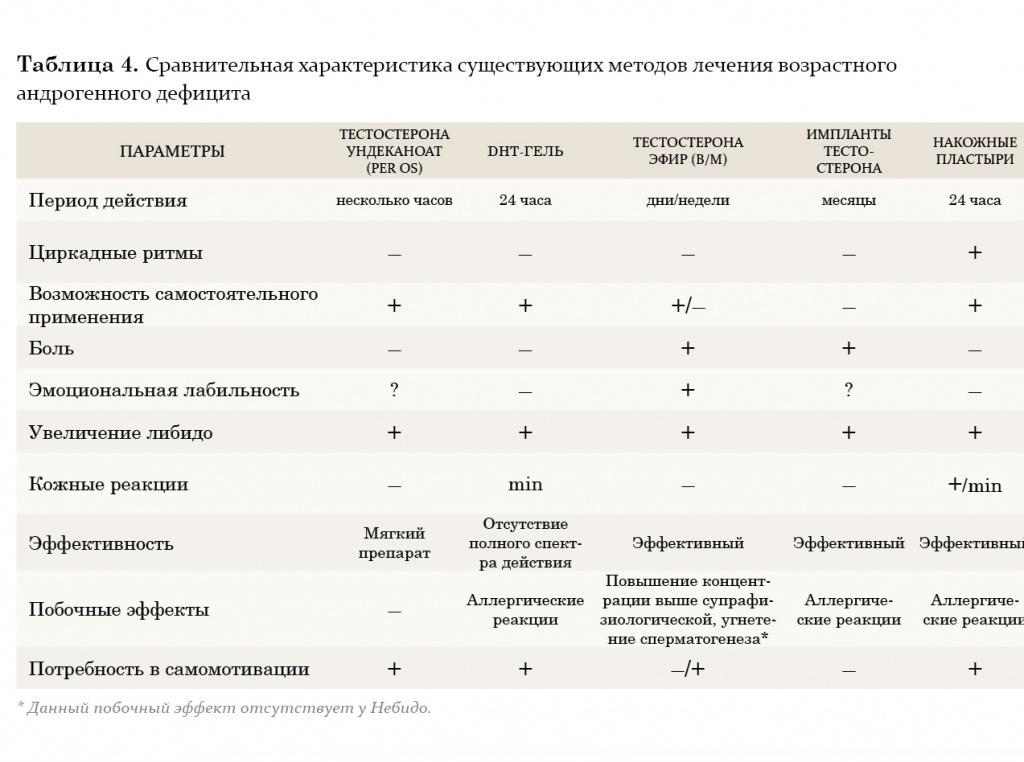
Внутримышечные инъекции пролонгированных эфиров тестостерона также являются широко применяемым методом заместительной терапии у мужчин с гипогонадизмом. Два наиболее известных эфира тестостерона – тестостерона ципионат и тестостерона энантат, имеют похожую фармакокинетику. При внутримышечном введении этих препаратов создается депо, из которого препарат высвобождается в кровеносное русло. В течение первых 2–3 дней после введения уровень тестостерона повышается до супрафизиологических цифр, а затем медленно снижается на протяжении последующих 2 недель до субнормальных значений. Положительной стороной этих препаратов является длительность терапевтического действия. Тем не менее резкие изменения в уровне тестостерона, зачастую ощущаемые самим пациентом в виде подъемов и снижения либидо, общего самочувствия, эмоционального статуса, являются нежелательными качествами данных препаратов. В связи с этим большие надежды возлагаются на новый препарат Небидо (Шеринг), фармакокинетика которого значительно отличается от других эфиров тестостерона. Небидо представляет собой тестостерона ундеканоат и является препаратом, не обладающим пиком повышения концентрации.
На протяжении двух последних десятилетий большое внимание уделяется исследованию преимуществ трансдермального применения препаратов тестостерона. Мошоночные пластыри обладают эффективным действием, и некоторые пациенты считают их наиболее удобным методом лечения. Накожные пластыри наиболее хорошо воспринимаются пациентами и дают эффективный уровень тестостерона в сыворотке крови. Тем не менее существуют некоторые различия между этими двумя разновидностями пластырей относительно их аллергогенного потенциала: при применении накожных пластырей отмечается гораздо большая частота возникновения аллергических реакций и раздражения кожи, чем при применении мошоночных пластырей.
Гель тестостерона обладает всеми преимуществами пластырей и не вызывает развития кожных реакций. Единственный его недостаток заключается в наличии возможности контакта геля с партнершей и недостаточном количестве долговременных исследований по его применению.
Трансдермальный путь введения тестостерона позволяет избежать его первичного метаболизма в печени и инактивации, как это происходит при применении пероральных андрогенных препаратов, а также позволяет имитировать циркадные ритмы высвобождения физиологического немодифицированного тестостерона и его естественных метаболитов, эстрадиола и ДГТ. К тому же терапию с использованием пластырей и геля в случае необходимости можно легко прервать. К положительным моментам этого метода лечения также относится низкий риск возникновения лекарственной зависимости.
Европейский препарат 5-α-дигидротестостерон-гель (ДГТ) хотя и признан эффективным, однако неизвестно, оказывает ли изолированное применение неароматизированного андрогена, каким является ДГТ, такое же действие, как тестостерон, в связи с тем, что метаболиты тестостерона включают эстрадиол. По мнению многих авторов, применение препарата не рекомендуется, так как ДГТ вследствие невозможности превращения в эстрадиол не обладает полным спектром терапевтических свойств тестостерона (например, влиянием на костную ткань и сердечно-сосудистую систему).
Некоторые из препаратов заместительной терапии, такие как тестостерона ундеканоат, ДГТ-гель и мошоночные пластыри, вызывают существенное увеличение концентрации ДГТ в сыворотке крови. ДГТ известен как главный андроген простаты, и в связи с этим проводилось много дискуссий по поводу способности его вызывать заболевания предстательной железы. Однако, несмотря на эти предположения, в последнее 10-летие не зафиксировано данных в пользу увеличения частоты возникновения патологии простаты при назначении препаратов ДГТ.
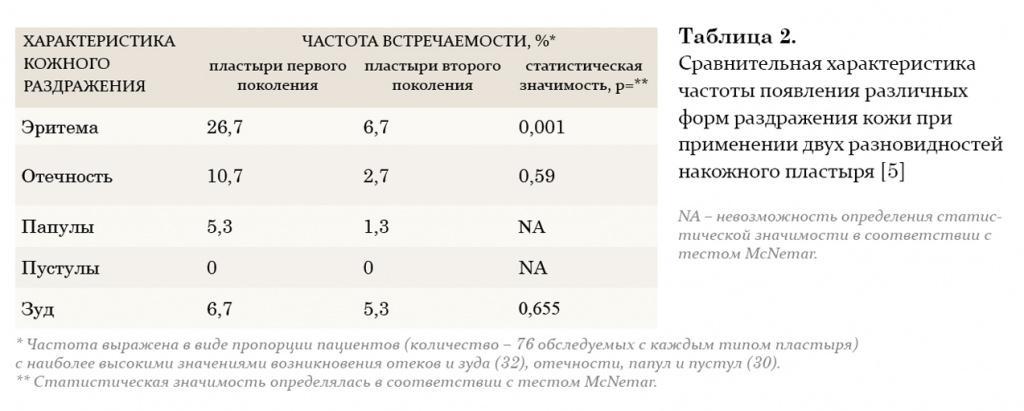
Таким образом, существует множество препаратов заместительной андрогенотерапии, однако все они имеют те или иные побочные эффекты, а также обладают угнетающим действием на сперматогенез. В последнее время появляется все больше работ, демонстрирующих вторичный характер возрастного андрогенного дефицита. Согласно материалам ВОЗ, получены данные о сохранении секретирующей функции клетками Лейдига у пожилых мужчин, что позволило ученым предложить принципиально новый подход в лечении возрастного андрогенного дефицита, основанный на стимуляции синтеза эндогенного тестостерона.
Однако не стоит забывать, что наряду с абсолютными противопоказаниями для заместительной терапии андрогенами (рак грудной и предстательной желез) существуют и дополнительные (доброкачественная гиперплазия предстательной железы с выраженной обструкцией, пролактинома, полицитемия). К относительным противопоказаниям относятся нарушения сна в виде апноэ, обструктивные заболевания легких, интенсивное курение.
К побочным эффектам андрогенов относятся усиление ночного апноэ, полицитемия, гинекомастия, приапизм, задержка жидкости, повышение АД, отеки, увеличение размеров простаты, торможение сперматогенеза.
То есть сегодня существуют методы лечения возрастного андрогенного дефицита, которые можно разделить на две группы, принципиально различающиеся по механизму действия:
заместительная терапия экзогенными андрогенными препаратами; терапия, стимулирующая синтез эндогенного тестостерона.
Таким образом, можно сказать, что оптимального для всех средства для лечения возрастного андрогенного дефицита у мужчин не существует. И к выбору препарата следует подходить строго индивидуально, учитывая возраст пациента, индекс массы тела, необходимость сохранения сперматогенеза, показатели гематокрита и сопутствующие заболевания.
Антиандрогены против андрогенов: в лечении выпадения волос.

Одной из причин андрогенетической алопеции считается повышенная чувствительность рецепторов к андрогенам. И это не последняя «претензия» к андрогенам. Как известно мужские гормоны стимулируют избыточный рост волос в андрогензависимых зонах, провоцируют угревые высыпания, выпадение волос, нарушение менструального цикла. Повышение уровня андрогенов может повлечь за собой ожирение, артериальную гипертензию, нарушения углеводного и липидного обменов.
Не тяжело догадаться, что первым пунктом в лечении данных отклонений будет антиандрогенная терапия. Но оправдано ли и безопасно такое лечение? Может пришло время посмотреть по-новому на тактику лечения. Такую возможность нам дают результаты научных исследований и клинический опыт современных институтов и клиник.
Если врач сталкивается с истинной гиперандрогенией, в данном случае антиандрогенная терапия необходима. Когда мы можем столкнуться с истиной гиперандрогенией?
Она может быть овариального или надпочечникового генеза, а так же иметь функциональный или опухолевый генез. Синдром поликистозных яичников относится к функциональной овариальной гиперандрогении. К функциональной надпочечниковой гиперандрогении относятся неклассическая форма врожденной дисфункция коры надпочечников, опухолевые заболевания, болезнь Иценко-Кушинга, гиперпролактинемия.

210 женщинам из 463 был поставлен диагноз «выпадение волос по женскому типу». Но синдром поликистозных яичников был выявлен только у 4 пациенток, депрессия была у 18 пациенток. Так как теория том, что в основе развития андрогенетической алопеции лежат андрогены не столь очевидна, все чаще андрогенетическую алопецию предпочитают называть «выпадение волос по женскому типу».
Но исключать индивидуальную чувствительность волосяных фолликулов к нормальному уровню тестостерона как причину и механизм развития выпадения волос невозможно и неправильно.
Еще один интересный факт. У пациентов с синдромом нечувствительности к андрогенам или дефицитом 5-α редуктазы с невозможностью превращения тестостерона в дигидротестостерон развивается «выпадение волос по женскому типу» или как прежде называли андрогенетическая алопеция, но как видите без участия андрогенов.
Опубликованные в 2012 году Глазов Р. Л. И соавт. результаты, не менее удивляют, среди 285 женщин, которые имели дефицит тестостерона, 76 из них жаловались на истончение волос на голове.
При проведении терапия тестостероном 48 из них говорили о улучшения состояния волос. Ткачев Владислав Петрович, к.м.н., врач дерматолог, трихолог поделился собственным опытом, что из 29 пациентов фертильного возраста с диагнозом «выпадение волос по женскому типу» уровень общего тестостерона в пределах нормы у 9 (31 %), а избыток у 1 (3, 4%), значение тестостерона ниже нормы было у 19 пациентов.
В лечении андрогенетической алопеции предусмотрено использование контрацептивных препаратов с ципротероном (Диане 35), верошпирон (спиронолактоном), флутамидом. Хотя реальные показания к назначению этих препаратов имеются лишь у небольшого процента пациентов. К тому же данные препараты повышают уровень депрессии, которая уже имеется у большого количества женщин страдающих поредением волос.
После приема антиандрогенов многие женщины действительно отмечают приостановление выпадения волос, ускорение роста волос и со временем увеличение густоты волос.
Что же происходит с женским организмом при подавлении андрогенов?
Рецепторы к андрогенам у женщин находится в кровеносных сосудах, сердце, легких, молочных железах, в головном и спинном мозге, мочевом пузыре, уретре, матке, яичниках, влагалище, мышечной и жировой ткани, коже, костной ткани, периферических нервах.
После длительного приема антиандрогенов могут возникнуть:
По данным Гончарова Н.П. и соавторов еще ряд факторов могут повлиять на уровне тестостерона:
Если врач трихолог столкнулся с истиной гиперандрогенией, то тут без антиандрогенов не обойтись. Слепо назначать системную терапию антиандрогенами только по факту наличия у женщин с типовым поредением волос нерационально. Ведь патогенез андрогенетической алопеции (выпадение волос по женскому типу) не ограничен только повышенной чувствительностью рецепторов волосяных фолликулов к андрогенам.
Правильно будет использование этих препаратов в виде наружных средств, для минимизации побочных эффектов.
Также вы можете записаться на консультацию трихолога в косметологии МедЭстет в Виннице.
Литература Журнал Трихология 3/2016
С уважением врач-трихолог Яковлева Леся
Гормональное лечение рака предстательной железы
Рецензент материала
Профессор Капранов С.А. — Доктор медицинских наук, дважды Лауреат Государственных Премий Правительства Российской Федерации в области науки и техники, Лауреат Премии Ленинского Комсомола, автор более 350 научных работ по медицине, 7 монографий, и 10 патентов на изобретения по медицине, за 30 лет личного опыта провел более чем 10 000 различных эндоваскулярных операций
Рак простаты – один из самых акутальныхвопросов современной онкомедицины. Ключевая проблема заключается в том, что по уровню летальности злокачественные образования, формирующиеся на предстательной железе, занимают 2-3 место среди прочих видов онкологии. План лечения рака предстательной железы определяет исключительно профильный специалист. Часто обращаются к гормональной разновидности медикаментозной терапии. Подробнее о нюансах и особенностях гормонального лечения рака предстательной железы узнайте из этой статьи.
Причины появления опухолей
Однозначного ответа о том, каковы причины, по которым формируется рак предстательной железы, до сих пор не существует. Можно выделить массу провоцирующих факторов, которые статистически имеют место в жизни мужчин, страдающих от онкологии с такой локализацией. В этот перечень входит:
Внимание! Рекомендуется не только отказаться от животных жиров, но и насытить свой ежедневный рацион соей, фитоэстрогенами, изофлавоноидами, токоферолом, селеном и каротиноидами.
Показания к гормональному лечению
Не всегда гормональная терапия рака простаты является действенным методом. Дать корректное назначение может только лечащий врач, имеющий полное представление о клинической картине ведомого пациента. Востребована гормонотерапия среди мужчин, чей возраст превышает 67-70 лет. Также прибегают к гормональному типу лечения на следующих стадиях развития образования:
Статистически наибольшая эффективность у лечения рака простаты при помощи радикальной простатэктомии с полным иссечением предстательной железы. Однако оперативные процедуры не всегда возможны, как и альтернативная им терапия (химическая, лучевая). Фактически гормонотерапией пользуются как методом, который, если и не помогает излечить рак простаты, то хотя бы продлевает жизнь пациенту.
Разновидности гормонотерапии
Ранее лечение рака простаты посредством гормонального контроля заключалось в проведении двусторонней орхиэктомии (удаление яичек) – это позволяло снизить уровень тестостерона в организме (считается, что именно переизбыток этого гормона в организме является одной из причин рака предстательной железы). Современная онкомедицина исключает необходимость операции, т.к. можно использовать специальные медикаменты, понижающие уровень тестостерона до необходимого в целях лечения.
В здоровом мужском организме содержание тестостерона составляет от 300 до 1000 нг/дл. Медикаментозно этот уровень может быть понижен до 50 нг/дл, но зачастую медики стремятся к минимально возможному уровню гормона – 20-30 нг/дл. Рассмотрим подробнее, какие виды гормональных препаратов используются при лечении поражения простаты.
Агонисты ЛГРГ
Освобождающий лютеинизирующий гормон (ЛГРГ) – это пептидный гормон, направляющий химическую реакцию к мозговым клеткам, вызывая продукцию тестостерона. Агонисты данного гормона отвечают за блокировку его функций, соответственно предотвращая выработку тестостерона половой системой.
Данные медикаментозный вариант лечения является одним из самых распространенных и востребованных при борьбе с раком предстательной железы. Выпускается необходимый препарат не в таблеточном, а в жидком ампульном виде для введения через мышечные или жировые ткани, поскольку пептиды растворяются в ЖКТ, не достигая цели.
Введение препарата осуществляется раз в месяц, либо для его автоматической подачи в организм используется специальный имплантат, вводимый под кожу. В этом случае вещество поступает в организм медленно, а установленный элемент заменяется раз в полгода или год.
Стоит отметить, что в первые 3-4 недели после первичного введения агонистов ЛГРГ уровень тестостерона возрастает, вызывая обострение симптоматики рака предстательной железы. При сильном болевом синдроме или выявлении активного роста опухоли за пределы простаты врач может назначить вспомогательный курс антиандрогенов. Со временем дискомфорт и плохое самочувствие уйдут, а уровень тестостерона начнет снижаться, что и требуется для эффективного лечения.
Побочные эффекты от гормонотерапии с использованием агонистов ЛГРГ:
Крайне популярно при терапии рака с помощью агонистов ЛГРГ использовать схему дискретного дозирования. Суть такого лечения заключается в периодической приостановке введения препаратов и последующем возобновлении. Статистика показывает, что выраженность побочных эффектов при таком подходе уменьшается. Однако преимущества и эффективность такой терапии не изучены до конца.
Антагонисты ЛГРГ
В сравнении с агонистами данный вид препаратов используется крайне редко. На данный момент является изученной и производимой лишь одна форма такого медикамента для гормонотерапии – дегареликс (отечественный вариант – «Фирмагон»). В онкомедицине к нему обращаются преимущественно на 3-4 стадии развития рака предстательной железы с метастазированием в костную ткань. Медикамент позволяет предотвратить компрессию спинного мозга, вызываемую сдавливанием опухолью.
Антагонист ЛГРГ не повышает уровень тестостерона, а симптоматика, которой сопровождается рак простаты, блокируется. Первичная доза составляет 2 шприца по 120 мг, а потом 80 мг через 1 месяц. В дальнейшем процедура повторяется раз в месяц.
Зачастую побочные эффекты такой гормонотерапии:
Случаев передозировки препаратом не выявлено.
Антиандрогены
Это препараты периферического действия, которые блокируют продукцию мужских гормонов надпочечниками. Стоит отметить, что действующие компоненты антиандрогенов вызывают минимум побочных эффектов в сравнении с другими препаратами, используемыми при лечении посредством гормонотерапии. Однако эффективность данных средств снижается, если рак предстательной железы начинает распространяться в ближайшие органы и ткани.
Первичный эффект от использования в сочетании с агонистами ЛГРГ – это сильнейшее увеличение уровня тестостерона в организме, что приводит к росту предстательной железы в размерах и усложнению мочеиспускательного процесса. Если рак простаты метастазировал в костную ткань, то использование антиандрогенов усиливает болевой синдром в костях, повышает риск получения травмы, перелома или ущемления нервных окончаний.
Если же проводить гормонотерапию попеременно, сначала используя антиандрогенные медикаменты, а затем переходя на агонисты ЛГРГ, то количество побочных эффектов уменьшится. Как показывает практика, если от использования антиандрогенов нет эффекта, то временное прекращение лечения способствует улучшению самочувствия пациента. Медицинская терминология определяет для такого состояния название «андрогенное отторжение».
Эстрогены
Синтетически выведенный гормон эстроген (он является сугубо женским) может быть использован в гормонотерапии при лечении у мужчин рака предстательной железы. Снижение уровня тестостерона в этом случае происходит за счет принудительного выделения лютеинизирующего вещества гипоталамусом. Даже при допустимой дозировке в 3-5 мг эстрогеносодержащие препараты провоцируют образование хронических патологий сердечно-сосудистой системы, а также увеличивают риск сердечного приступа.
В качестве защитной меры для организма пациента в процессе лечения медики снижают дозировку до суточного приёма в 1 мг. Но при этом уже через 6-12 месяцев тестостерон вновь начинает накапливаться в организме, что сводит борьбу с раком предстательной железы на нет, если положительный эффект от проводимого лечения не был достигнут ранее.
Орхиэктомия
Если всё же врач прибегает к использованию орхиэктомии, то проводится оперативное вмешательство с иссечением яичек. На их место для сохранения эстетичности в мошонку могут быть помещены искусственные заменители (имплантаты). Подобная операция эффективно уменьшает уровень тестостерона в организме. Вся процедура занимает около 1,5 часа и небольшого реабилитационного периода вплоть до снятия швов со сделанных ранее надрезов. При всей радикальности операции у неё те же побочные эффекты, что и агонистов ЛГРГ.
Однако, как уже было сказано ранее, оперативное вмешательство – это не безальтернативный вариант. Современные медикаментозные подходы к лечению поражения предстательной железы достаточно эффективны. От них отказываются в случае нехватки финансов или продолжительного отсутствия положительных результатов. Также орхиэктомия назначается пожилым пациентам, которые не могут посещать медкабинет с целью проведения гормональной терапии (введения препаратов по графику).
Сочетанная блокировка андрогенов
Гормональная терапия при раке, проводимая по этому принципу, заключается в одновременном приёме медикаментов, воздействующих на мозговую активность и периферически на функционал надпочечников. Тестостерон не только перестаёт вырабатываться, но и прекращает действовать непосредственно в простате. Однако количество побочных эффектов от такого метода лечения превышает его положительные качества. Выраженными проявлениями зачастую являются: отсутствие сексуального желания, импотенция, понос, тошнота, дисфункция печени.
Общие побочные эффекты гормональной терапии
Помимо того, что у конкретных методов имеются собственные недостатки, стоит указать на те проявления, которые могут формироваться при приёме любых медикаментов. К ним относятся:
Однако столь широкий перечень побочных эффектов проявляется в полном объеме крайне редко. Грамотно спланированный процесс лечения, построенный на использовании оптимальных медикаментозных средств, имеет предельно высокую эффективность и даёт положительные результаты в борьбе со злокачественной опухолью. Однако полного выздоровления посредством терапии добиться крайне сложно, если быть точнее, то она должна применяться в комплексе с другими современными методами лечения.
Зачастую гормональную терапию используют для замедления интенсивности развития онкологического образования. Она необходима для контроля над онкологической патологией и сохранения привычного режима жизнедеятельности пациента. С помощью терапии можно повышать эффективность других методов, либо просто продлевать срок жизни для мужчины, чей клинический случай является бесперспективным в ракурсе полного выздоровления.
Прогноз и оценка эффективности метода
Когда онкологическое поражение только диагностируется, прогноз может быть рассчитан исходя из результатов дифференцирования выявленного новообразования (злокачественное или доброкачественное) и определения стадии его развития. Для мужчин с опухолью М1 (1-2 стадия) уровень выживаемости составляет от 28 до 53 месяцев. Для малой доли пациентов (7%), прошедших курс терапии при раке простаты, он составляет более 10 лет.
Важно! «Уровень выживаемости» – это не термин, который становится приговором. Это срок, который прошел с момента прохождения лечебного курса конкретным пациентом. По истечению данного срока он был снят с учета, потому в историю болезни записывается обозримый период жизни.
Прогнозировать перспективы развития опухоли и лечебного воздействия на неё можно, основываясь на следующие показатели:
В случае местно-распространенного развития рака выживаемость составляет более 10 лет.
Именно уровень ПСА является контрольным значением. Нормальным уровнем его понижения спустя 1,5-2 месяца после того, как было начато гормональное лечение рака предстательной железы, является значение в 1/10 нг/мл. Однако и при уровне в 5/10 нг/мл можно рассчитывать на благоприятный прогноз. Помимо контроля за уровнем ПСА многое зависит от агрессивности злокачественного образования и схематики воздействия метастазов на организм пациента.
Профилактические меры
Завершение лечебного курса – это не последняя стадия борьбы с заболеванием. В случае со злокачественными опухолями необходимо предотвращать возможный рецидив, контролируя каждый свой шаг вне стен медицинского учреждения. К набору профилактических мероприятий, которые назначаются мужчинам, прошедшим один из вышеперечисленных лечебных курсов, относятся:
Мужчина также должен быть ограждён от стресса и нервного перенапряжения. Осторожность в целях предотвращения механических повреждений также должна стать ключевым принципом жизнедеятельности.
Обращение в Центр эндоваскулярной хирургии
Медицинский центр профессора Капранова – это профильное учреждение, где помощь может получить любой онкобольной. Обращение к нашим специалистам гарантирует вам качественную диагностику с точным дифференцированием и определением стадии развития опухоли. Врачи центра находят индивидуальный подход к каждому пациенту, формируя оптимальный план лечебных курсов. При этом хирургическое вмешательство не назначается никогда, если существует возможность альтернативного подхода к борьбе с раковым образованием.
Изучите внимательно наш сайт, ознакомившись с ключевыми особенностями работы центра. Прочитайте и другие статьи, чтобы узнать о методах онкомедицины. Имейте представление о наших возможностях. Многое о нас можно узнать из отзывов других пациентов, прошедших лечебные курсы у медиков центра. Можно оставить собственный комментарий, если у вас уже сложилось впечатление о нас.
Ответственность и профессионализм – это лишь малая часть достоинств наших врачей и медперсонала. Всем обратившимся гарантируются выгодные условия и комфорт пребывания в центре. Будьте здоровы, а мы вам в этом поможем, исходя из особенностей и потребностей каждого пациента!
Основные направления деятельности центра эндоваскулярной хирургии а также другие популярные материалы:
Эмболизация маточных артерий в гинекологии
ЭМА в Москве
Эмболизация сосудов аденомы простаты

