антифосфолипидным синдромом что это
Антифосфолипидный синдром
МКБ-10
Общие сведения
Антифосфолипидный синдром (АФС) – комплекс нарушений, вызванных аутоиммунной реакцией к фосфолипидным структурам, присутствующим на клеточных мембранах. Заболевание было детально описано английским ревматологом Hughes в 1986 году. Данные об истинной распространенности антифосфолипидного синдрома отсутствуют; известно, что незначительные уровни АТ к фосфолипидам в сыворотке крови обнаруживаются у 2-4% практически здоровых лиц, а высокие титры – у 0,2%. Антифосфолипидный синдром в 5 раз чаще диагностируется среди женщин молодого возраста (20-40 лет), хотя заболеванием могут страдать мужчины и дети (в т. ч. новорожденные). Как мультидисциплинарная проблема, антифосфолипидный синдром (АФС) привлекает внимание специалистов в области клинической ревматологии, акушерства и гинекологии, кардиологии.
Причины
Основополагающие причины развития антифосфолипидного синдрома неизвестны. Между тем, изучены и определены факторы, предрасполагающие к повышению уровня антител к фосфолипидам. Так, высокий титр антифосфолипидных антител наблюдается на фоне:
Имеются сведения о генетической предрасположенности к повышенному синтезу антител к фосфолипидам у лиц-носителей антигенов HLA DR4, DR7, DRw53 и у родственников больных антифосфолипидным синдромом.
Патогенез
В зависимости от структуры и иммуногенности различают «нейтральные» (фосфатидилхолин, фосфатидилэтаноламин) и «отрицательно заряженные» (кардиолипин, фосфатидилсерин, фосфатидилинозитол) фосфолипиды. К классу антифосфолипидных антител, вступающих в реакцию с фосфолипидами, относятся волчаночный антикоагулянт, Ат к кардиолипину, бета2-гликопротеин-1-кофакторзависимые антифосфолипиды и др. Взаимодействуя с фосфолипидами мембран клеток эндотелия сосудов, тромбоцитов, нейтрофилов, антитела вызывают нарушение гемостаза, выражающиеся в склонности к гиперкоагуляции. В целом иммунобиологические механизмы развития антифосфолипидного синдрома требуют дальнейшего изучения и уточнения.
Классификация
С учетом этиопатогенеза и течения различают следующие клинико-лабораторные варианты антифосфолипидного синдрома:
Симптомы
Согласно современным взглядам, антифосфолипидный синдром представляет собой аутоиммунную тромботическую васкулопатию. При АФС поражение может затрагивать сосуды различного калибра и локализации (капилляры, крупные венозные и артериальные стволы), что обусловливает чрезвычайно разнообразный спектр клинических проявлений, включающий венозные и артериальные тромбозы, акушерскую патологию, неврологические, сердечно-сосудистые, кожные нарушения, тромбоцитопению.
Наиболее частым и типичным признаком антифосфолипидного синдрома являются рецидивирующие венозные тромбозы: тромбоз поверхностных и глубоких вен нижних конечностей, печеночных вен, воротной вены печени, вен сетчатки. У больных с антифосфолипидным синдромом могут возникать повторные эпизоды ТЭЛА, легочная гипертензия, синдром верхней полой вены, синдром Бадда-Киари, надпочечниковая недостаточность.
Венозные тромбозы при антифосфолипидном синдроме развиваются в 2 раза чаще артериальных. Среди последних преобладают тромбозы церебральных артерий, приводящие к транзиторным ишемическим атакам и ишемическому инсульту. Прочие неврологические нарушения могут включать мигрень, гиперкинезы, судорожный синдром, нейросенсорную тугоухость, ишемическую нейропатию зрительного нерва, поперечный миелит, деменцию, психические нарушения.
Поражение сердечно-сосудистой системы при антифосфолипидном синдроме сопровождается развитием инфаркта миокарда, внутрисердечного тромбоза, ишемической кардиомиопатии, артериальной гипертензии. Довольно часто отмечается поражение клапанов сердца – от незначительной регургитации, выявляемой с помощью ЭхоКГ, до митрального, аортального, трикуспидального стеноза или недостаточности. В рамках диагностики антифосфолипидного синдрома с сердечными проявлениями требуется проведение дифференциальной диагностики с инфекционным эндокардитом, миксомой сердца.
У женщин АФС часто выявляется в связи с акушерской патологией: повторным самопроизвольным прерыванием беременности в различные сроки, задержкой внутриутробного развития плода, фетоплацентарной недостаточностью, гестозом, хронической гипоксией плода, преждевременными родами. При ведении беременности у женщин с антифосфолипидным синдромом акушер-гинеколог должен учитывать все возможные риски.
Диагностика
Учитывая полиорганность поражения, диагностика и лечение антифосфолипидного синдрома требуют объединения усилий врачей различных специальностей: ревматологов, кардиологов, неврологов, акушеров-гинекологов и др. Антифосфолипидный синдром диагностируется на основании клинических (сосудистый тромбоз, отягощенный акушерский анамнез) и лабораторных данных. Диагноз считается достоверным при сочетании, по меньшей мере, одного основного клинического и лабораторного критерия:
Дифференциально-диагностические мероприятия должны быть направлены на исключение:
Лечение антифосфолипидного синдрома
Основной целью терапии антифосфолипидного синдрома служит предотвращение тромбоэмболических осложнений. Режимные моменты предусматривают умеренную физическую активность, отказ от долгого нахождения в неподвижном состоянии, занятий травматичными видами спорта и длительных авиаперелетов. Женщинам с антифосфолипидным синдромом не следует назначать пероральные контрацептивы, а перед планированием беременности необходимо обязательно обратиться к акушеру-гинекологу. Беременным пациенткам в течение всего периода гестации показан прием малых доз глюкокортикоидов и антиагрегантов, введение иммуноглобулина, инъекции антикоагулянтов под контролем показателей гемостазиограммы.
Медикаментозная терапия при антифосфолипидном синдроме может включать назначение непрямых антикоагулянтов, прямых антикоагулянтов, антиагрегантов. Профилактическая антикоагулянтная или антиагрегантная терапия большинству больных с антифосфолипидным синдромом проводится длительно, а иногда пожизненно. При катастрофической форме антифосфолипидного синдрома показано назначение высоких доз глюкокортикоидов и антикоагулянтов, проведение сеансов плазмафереза, переливание свежезамороженной плазмы и т. д.
Прогноз
Своевременная диагностика и профилактическая терапия позволяют избежать развития и рецидивирования тромбозов, а также надеяться на благоприятный исход беременности и родов. При вторичном антифосфолипидном синдроме важным представляется контроль за течением основной патологии, профилактика инфекций. Прогностически неблагоприятными факторами служат сочетание антифосфолипидного синдрома с СКВ, тромбоцитопения, быстрое нарастание титра Ат к кардиолипину, стойкая артериальная гипертензия. Все пациенты с диагнозом «антифосфолипидный синдром» должны находиться под наблюдением ревматолога с периодическим контролем серологических маркеров заболевания и показателей гемостазиограммы.
Антифосфолипидный синдром в Москве
Антифосфолипидный синдром (АФС) — это аутоиммунное заболевание, в основе которого лежит синтез антифосфолипидных антител. Данное исследование представляет собой объемный анализ, позволяющий выявить патологию с высокой вероятностью. Тест включает в себя выявление больших групп антител, которые встречаются при АФС.
Что входит в комплекс
Приём и исследование биоматериала
Когда нужно сдавать анализ Антифосфолипидный синдром?
Диагностика и дифференциация антифосфолипидного синдрома.
Подробное описание исследования
Одним из механизмов иммунной защиты в норме является выработка антител — иммуноглобулинов, Ig, — которые относятся к гамма-глобулиновой фракции белков сыворотки крови. По своей природе антитела представляют собой гликопротеиды — молекулы, содержащие углевод и белок, — и делятся на пять классов: IgA, IgM, IgG, IgE, IgD. Они различаются по структуре и выполняемым функциям, но имеют схожее строение. В случае, когда иммуноглобулины реагируют на молекулы собственного организма, их называют аутоантителами.
Антифосфолипидный синдром (АФС) — это аутоиммунное заболевание, которое включает в себя рецидивирующие тромбозы, акушерскую патологию. В основе АФС лежит синтез антифосфолипидных антител и их стимулирующим тромбообразование действием. Данные иммуноглобулины бывают нескольких типов.
Антифосфолипидный синдром является одним из видов приобретенных тромбофилий. Тромбофилиями называют состояния, при которых развиваются тромбозы кровеносных сосудов. При АФС тромбы возникают как в венозном русле, так и в артериальном и могут повторяться (рецидивировать) в 70-80% в одном и том же месте. Тромбозы глубоких вен опасны высоким риском развития эмболии — закупорки — легочных сосудов.
Также при антифосфолипидном синдроме может отмечаться тромбоцитопения. Тромбоцитопенией называют состояние, при котором количество тромбоцитов в крови составляет менее 150 × 109/л. Люди с тромбоцитопенией имеют повышенный риск развития кровотечений и увеличения их длительности. На коже могут появляться многочисленные мелкие пурпурные точки, в связи с чем болезнь называют тромбоцитопенической пурпурой.
Выделяют первичный и вторичный АФС. Первый диагностируют, когда не известна причина, вызывающая повышение содержания антифосфолипидных антител. Второй же выделяют, когда известно основное заболевание, которое является причиной увеличения образования данных иммуноглобулинов и часто связано с хронической стимуляцией иммунной системы. Основными четырьмя группами причин стимуляции являются:
К повышению концентрации антифосфолипидных антител приводит ряд препаратов, в том числе фенотиазины и другие средства, вызывающие лекарственную волчанку: хлорпромазин, гидралазин, фенитоин, прокаинамид и хинилин.
Антифосфолипидные антитела повышаются как при вирусных, так и при бактериальных инфекциях. Однако при них повышение является транзиторным — кратковременным — и их появление следует отличать от АФС.
Акушерская патология при АФС связана с невынашиванием беременности. Выкидыш, обусловленный повышенной концентрацией антифосфолипидных антител, вероятен на любом сроке, но чаще происходит во втором или в третьем триместре. Гибель плода является следствием тромбообразования в мелких сосудах плаценты, из-за чего последняя перестаёт выполнять свои функции и дальнейшее протекание беременности становится невозможным.
Комплексное исследование на АФС включает в себя следующие группы антифосфолипидных антител:
Кардиолипин — это фосфолипид, который входит в состав биологических мембран, а именно обнаруживается в мембране митохондрий, одной из структур клеток, где участвует в обменных процессах. К кардиолипину при антифосфолипидном синдроме вырабатываются иммуноглобулины, поэтому их определение с назначением соответствующего анализа является одним из основных моментов в правильной постановке диагноза.
Данные аутоантитела направлены на поражение основных компонентов биологических мембран клеток человека. Такими компонентами являются фосфолипиды. Из этих молекул больше всего АТ вырабатываются к фосфатидилсерину, который находится на внутренней поверхности тромбоцитов и на мембранах клеток внутреннего слоя сосудов (эндотелия). Фосфатидилсерин принимает активное участие в формировании кровяного сгустка (тромба), а при выработке АТ к этой молекуле происходит неадекватное тромбообразование.
Волчаночный антикоагулянт (ВА).
ВА — это группа антител к фосфолипидам, также увеличивающим риск тромбообразования. Впервые выделен у пациентов с системной красной волчанкой, однако в настоящее время входит в один из критериев определения антифосфолипидного синдрома.
Антитела к бета-2 гликопротеину.
Данные АТ являются одним из главных маркеров АФС. Их выявление при подозрении на АФС рекомендовано российскими и зарубежными клиническими рекомендациями. Иммуноглобулины к бета-2 гликопротеину часто ассоциированы с вторичным антифосфолипидным синдромом на фоне системной красной волчанки.
Антитела к протромбину.
Протромбин представляет собой белок, участвующий в процессах свертывания крови. АТ к нему, напрямую способствуют развитию симптомов АФС.
Данный анализ с высокой степенью вероятности может определить наличие АФС, широко применяется в клинической практике, доступен по цене и не имеет абсолютных медицинских противопоказаний. Сдавать для исследования необходимо венозную кровь.
Подробное описание исследований, референсные значения представлены на страницах с описаниями отдельных исследований.
Антифосфолипидный синдром в Ботлих
Антифосфолипидный синдром (АФС) — это аутоиммунное заболевание, в основе которого лежит синтез антифосфолипидных антител. Данное исследование представляет собой объемный анализ, позволяющий выявить патологию с высокой вероятностью. Тест включает в себя выявление больших групп антител, которые встречаются при АФС.
Что входит в комплекс
Приём и исследование биоматериала
Когда нужно сдавать анализ Антифосфолипидный синдром?
Диагностика и дифференциация антифосфолипидного синдрома.
Подробное описание исследования
Одним из механизмов иммунной защиты в норме является выработка антител — иммуноглобулинов, Ig, — которые относятся к гамма-глобулиновой фракции белков сыворотки крови. По своей природе антитела представляют собой гликопротеиды — молекулы, содержащие углевод и белок, — и делятся на пять классов: IgA, IgM, IgG, IgE, IgD. Они различаются по структуре и выполняемым функциям, но имеют схожее строение. В случае, когда иммуноглобулины реагируют на молекулы собственного организма, их называют аутоантителами.
Антифосфолипидный синдром (АФС) — это аутоиммунное заболевание, которое включает в себя рецидивирующие тромбозы, акушерскую патологию. В основе АФС лежит синтез антифосфолипидных антител и их стимулирующим тромбообразование действием. Данные иммуноглобулины бывают нескольких типов.
Антифосфолипидный синдром является одним из видов приобретенных тромбофилий. Тромбофилиями называют состояния, при которых развиваются тромбозы кровеносных сосудов. При АФС тромбы возникают как в венозном русле, так и в артериальном и могут повторяться (рецидивировать) в 70-80% в одном и том же месте. Тромбозы глубоких вен опасны высоким риском развития эмболии — закупорки — легочных сосудов.
Также при антифосфолипидном синдроме может отмечаться тромбоцитопения. Тромбоцитопенией называют состояние, при котором количество тромбоцитов в крови составляет менее 150 × 109/л. Люди с тромбоцитопенией имеют повышенный риск развития кровотечений и увеличения их длительности. На коже могут появляться многочисленные мелкие пурпурные точки, в связи с чем болезнь называют тромбоцитопенической пурпурой.
Выделяют первичный и вторичный АФС. Первый диагностируют, когда не известна причина, вызывающая повышение содержания антифосфолипидных антител. Второй же выделяют, когда известно основное заболевание, которое является причиной увеличения образования данных иммуноглобулинов и часто связано с хронической стимуляцией иммунной системы. Основными четырьмя группами причин стимуляции являются:
К повышению концентрации антифосфолипидных антител приводит ряд препаратов, в том числе фенотиазины и другие средства, вызывающие лекарственную волчанку: хлорпромазин, гидралазин, фенитоин, прокаинамид и хинилин.
Антифосфолипидные антитела повышаются как при вирусных, так и при бактериальных инфекциях. Однако при них повышение является транзиторным — кратковременным — и их появление следует отличать от АФС.
Акушерская патология при АФС связана с невынашиванием беременности. Выкидыш, обусловленный повышенной концентрацией антифосфолипидных антител, вероятен на любом сроке, но чаще происходит во втором или в третьем триместре. Гибель плода является следствием тромбообразования в мелких сосудах плаценты, из-за чего последняя перестаёт выполнять свои функции и дальнейшее протекание беременности становится невозможным.
Комплексное исследование на АФС включает в себя следующие группы антифосфолипидных антител:
Кардиолипин — это фосфолипид, который входит в состав биологических мембран, а именно обнаруживается в мембране митохондрий, одной из структур клеток, где участвует в обменных процессах. К кардиолипину при антифосфолипидном синдроме вырабатываются иммуноглобулины, поэтому их определение с назначением соответствующего анализа является одним из основных моментов в правильной постановке диагноза.
Данные аутоантитела направлены на поражение основных компонентов биологических мембран клеток человека. Такими компонентами являются фосфолипиды. Из этих молекул больше всего АТ вырабатываются к фосфатидилсерину, который находится на внутренней поверхности тромбоцитов и на мембранах клеток внутреннего слоя сосудов (эндотелия). Фосфатидилсерин принимает активное участие в формировании кровяного сгустка (тромба), а при выработке АТ к этой молекуле происходит неадекватное тромбообразование.
Волчаночный антикоагулянт (ВА).
ВА — это группа антител к фосфолипидам, также увеличивающим риск тромбообразования. Впервые выделен у пациентов с системной красной волчанкой, однако в настоящее время входит в один из критериев определения антифосфолипидного синдрома.
Антитела к бета-2 гликопротеину.
Данные АТ являются одним из главных маркеров АФС. Их выявление при подозрении на АФС рекомендовано российскими и зарубежными клиническими рекомендациями. Иммуноглобулины к бета-2 гликопротеину часто ассоциированы с вторичным антифосфолипидным синдромом на фоне системной красной волчанки.
Антитела к протромбину.
Протромбин представляет собой белок, участвующий в процессах свертывания крови. АТ к нему, напрямую способствуют развитию симптомов АФС.
Данный анализ с высокой степенью вероятности может определить наличие АФС, широко применяется в клинической практике, доступен по цене и не имеет абсолютных медицинских противопоказаний. Сдавать для исследования необходимо венозную кровь.
Подробное описание исследований, референсные значения представлены на страницах с описаниями отдельных исследований.
Профилактика и лечение антифосфолипидного синдрома: современные рекомендации и перспективы
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
ГУ Институт ревматологии РАМН, Москва
ГУ Институт ревматологии РАМН, Москва
А нтифосфолипидный синдром (АФС) – клинико–лабораторный симптомокомплекс, характеризующийся венозными и артериальными тромбозами, патологией беременности и некоторыми другими реже встречающимися клиническими проявлениями и лабораторными нарушениями, патогенетически связанными с синтезом антифосфолипидных антител (аФЛ) [1,2].
Профилактика и лечение АФС – сложная и недостаточно разработанная проблема. Это объясняется неоднородностью патогенетических механизмов, лежащих в основе АФС, отсутствием достоверных клинических и лабораторных показателей, позволяющих прогнозировать риск рецидивов тромбоза. В настоящее время не существует общепринятых международных стандартов тактики ведения пациентов с различными формами АФС, а предлагаемые рекомендации основаны главным образом на результатах «открытых» испытаний или ретроспективного анализа исходов заболевания [3–11]. Недостаточно изучены подходы к профилактике и лечению атеросклеротического поражения сосудов, нередко развивающегося у пациентов с АФС [12,3]. Поскольку «специфические» методы лечения иммунопатологических нарушений, лежащих в основе АФС, не разработаны, ведение пациентов с АФС (как и с другими тромбофилиями) основано на применении антикоагулянтных (антагонисты витамина К, гепарин) и антиагрегантных препаратов – ацетилсалициловая кислота (АСК). Характерная особенность АФС – высокий риск повторных тромбозов. Поэтому большинство пациентов вынуждены принимать антиагрегантные и/или антикоагулянтные препараты в течение длительного времени, а иногда и пожизненно.
Полагают, что риск развития (и рецидивирования) тромбозов при АФС можно снизить путем исключения потенциально контролируемых «факторов риска», но истинная эффективность этих рекомендаций не известна. Факторы риска, которые необходимо учитывать при разработке тактики ведения пациентов, представлены в таблице 1.
Учитывая определенную связь между увеличением титров аФЛ и риском развития тромбозов в общей популяции, полагают, что стойкое увеличение уровня аФЛ (даже в отсутствие клинических признаков АФС) является основанием для профилактического назначения низких доз АСК [14]. Недавно были опубликованы данные двух ретроспективных исследований, посвященных оценке эффективности АСК [15,16]. В одном исследовании изучалось 65 женщин с акушерской патологией, связанной с АФС. В течение 8 лет наблюдения тромботические нарушения развились только у 3 (10%) из 31 женщин, получавших АСК, и у 20 (59%) из 34 женщин, не получавших АСК [15]. В другом исследовании, включавшем 77 пациентов с АФС или без тромбозов, но с положительными результатами определения аФЛ, было показано, что прием АСК четко ассоциируется с более низкой частотой развития тромбозов [16].
Учитывая определенную связь между увеличением титров аФЛ и риском развития тромбозов в общей популяции, полагают, что стойкое увеличение уровня аФЛ (даже в отсутствие клинических признаков АФС) является основанием для профилактического назначения низких доз АСК [14]. Недавно были опубликованы данные двух ретроспективных исследований, посвященных оценке эффективности АСК [15,16]. В одном исследовании изучалось 65 женщин с акушерской патологией, связанной с АФС. В течение 8 лет наблюдения тромботические нарушения развились только у 3 (10%) из 31 женщин, получавших АСК, и у 20 (59%) из 34 женщин, не получавших АСК [15]. В другом исследовании, включавшем 77 пациентов с АФС или без тромбозов, но с положительными результатами определения аФЛ, было показано, что прием АСК четко ассоциируется с более низкой частотой развития тромбозов [16].
Существенный профилактический эффект, по крайней мере, при вторичном АФС, связанный с системной красной волчанкой (СКВ), могут оказать аминохинолиновые (антималярийные) препараты (гидроксихлорохин) [17]. Наряду с противовоспалительным гидроксихлорохин обладает определенными антитромботическим (подавляют аггрегацию и адгезию тромбоцитов, уменьшают размер тромба) и гиполипидемическим эффектами. Применение гидроксихлорохина, несомненно, показано всем аФЛ–позитивным пациентам с СКВ [18].
Лечение антагонистами витамина К (варфарин) безусловно, более эффективный, но менее безопасный (по сравнению с АСК) метод профилактики венозных и артериальных тромбозов при АФС [3–11,19,20]. Напомним, что применение антагонистов витамина К–антикоагулянтов требует тщательного клинического (геморрагические осложнения) и лабораторного (определение протромбинового времени) контроля. Для стандартизации результатов этого теста следует оценивать параметр «международное нормализованное отношение» (МНО), который учитывает влияние используемого в тесте тромбопластина на величину протромбинового времени.
Схема лечения варфарином при АФС такая же, как и при других тромбофилиях, и заключается в назначении «насыщающей» дозы (5 мг/день) в течение первых 2–х дней, а затем в подборе оптимальной дозы препарата, ориентируясь на «целевое» МНО. Следует помнить, что у лиц пожилого возраста для достижения того же уровня антикоагуляции следует использовать более низкие дозы варфарина, чем у молодых [21].
Особое значение имеет вопрос об интенсивности и длительности антикоагуляции. Известно, что увеличение МНО с 2–3 до 3,1–4,0 ассоциируется с возрастанием частоты тяжелых геморррагических осложнений (интракраниальные геморрагии или геморрагии, приводящие к летальному исходу, требующие переливания крови или госпитализации) [22]. Напомним, что к факторам риска геморрагических осложнений на фоне лечения варфарином относятся:
В общей популяции пациентов с венозными тромбозами отмена варфарина ассоциируется с одинаковой (5–10%) частотой рецидивирования тромбозов независимо от длительности предшествующего лечения варфарином (6, 12 и 24 мес.) [23]. Однако, как уже отмечалось, для АФС характерен высокий риск рецидивирования тромбозов. Поэтому пациентам с АФС и венозными тромбозами лечение варфарином должно проводиться более длительно (>12 мес), чем пациентам без АФС (3–6 мес).
Одна группа авторов при риске рецидивирования тромбозов (включая ишемический инсульт) у пациентов АФС рекомендует интенсивную антикоагуляцию варфарином, позволяющую поддерживать МНО на уровне >3,1 [24]. В то же время другие авторы указывают на эффективность (особенно при венозных тромбозах) среднего уровня антикоагуляции, позволяющего поддерживать МНО на уровне 2,0–3,0 [25]. M.A. Cronwther и соавт. [25] провели рандомизированное двойное слепое контролируемое исследование, в котором сравнивалась эффективность и безопасность умеренной интенсивной (МНО 2–3) и высокоинтенсивной (МНО 3.1–4) антикоагуляции варфарином при АФС. В исследование было включено 114 пациентов с высоким/умеренным уровнем аФЛ и по крайней мере одним эпизодом тромбоза (венозного и артериального) в анамнезе; длительность лечения составила 2,7 года. За период наблюдения рецидивы тромбозов имели место у 6 из 56 (10,7%) пациентов, получавших высокоинтенсивную терапию, и у 2 из 58 (3,4%) получавших умеренно интенсивную терапию варфарином. Интересно, что частота тяжелых кровотечений в сравниваемых группах была примерно одинаковой (у 3 пациентов, которым проводили интенсивную антикоагуляцию, и у 4 – умеренную).
Таким образом, в настоящее время наиболее аргументировано использование варфарина в средних дозах (МНО 2,0–3,0) у пациентов с первым эпизодом венозного тромбоза в отсутствие других факторов риска рецидивирования тромбоэмболических осложнений, в то время как у пациентов с рецидивами тромбозов в анамнезе, вероятно, более оправдана интенсивная антикоагуляция (МНО >3,0).
Специального обсуждения заслуживает вопрос о применении варфарина у пациентов с АФС и ишемическим инсультом [19]. Это связано с тем, что по данным многочисленных контролируемых исследований варфарин не имеет преимуществ перед АСК в отношении профилактики рецидивов инсульта в общей популяции пациентов с мозговыми инсультами и часто вызывает тяжелые интракраниальные кровотечения [26,27]. Однако, по мнению многих авторов, при АФС риск повторных мозговых тромбозов выше, чем риск кровотечений [28,29]. При этом риск кровотечений на фоне интенсивной антикоагуляции при АФС может быть в определенной степени компенсирован тем, что пациенты с этим синдромом, как правило, молодого возраста [28]. По данным G. Ruiz–Irastorza и соавт. [28], у пациентов с АФС на фоне лечения варфарином частота «больших» кровотечений составила 6 случаев на 100 пациентов–год, ни в одном случае не было фатальных кровотечений, а интракраниальные геморрагии имели место только у 1 пациента. При этом рецидивы тромбозов развивались главным образом у пациентов, у которых наблюдалась недостаточная антикоагуляция (МНО 4,0) в отсутствие кровотечений рекомендуется временно отменить варфарин до того момента, когда значение МНО вернется к желаемому уровню [33]. Более быстро нормализации МНО можно достигнуть путем введения небольших доз витамина К: 1 мг перорально (позволяет снизить риск по крайней мере «малых» кровотечений) или 0,5 мг внутривенно. Следует избегать назначения высоких доз витамина К, так как это может привести к длительной (в течение нескольких дней) резистентности к антагонистам витамина К. Подкожные инъекции витамина К не рекомендуются из–за выраженной вариабильности абсорбции. В случае гиперкоагуляции, сопровождающейся «большими» кровотечениями, введения только витамина К недостаточно, так как полный эффект развивается только через 12–24 часа после введения. В этом случае рекомендуется введение свежезамороженной плазмы или, что более предпочтительно, концентрата протромбинового комплекса.
Общие рекомендации, касающиеся профилактики тромбозов у пациентов с АФС, суммированы в таблице 2.
Центральное место в лечении острых тромботических осложнений при АФС занимают прямые антикогулянты – гепарин и особенно препараты низкомолекулярного гепарина [34]. Тактика применения прямых антикоагулянтов у пациентов с АФС не отличается от общепринятой:
Центральное место в лечении острых тромботических осложнений при АФС занимают прямые антикогулянты – гепарин и особенно препараты низкомолекулярного гепарина [34]. Тактика применения прямых антикоагулянтов у пациентов с АФС не отличается от общепринятой:
1. Определить базальный уровень АЧТВ, протромбиновое время и общий анализ крови.
2. Подтвердить отсутствие противопоказаний для гепаринотерапии.
3. Ввести внутривенно 5000 МЕ гепарина.
4. Решить вопрос о тактике гепаринотерапии.
Начать непрерывную внутривенную инфузию нефракционированного гепарина – 18 МЕ/кг/час (в среднем 30000/24 часа мужчине 70 кг веса):
– определять АЧТВ каждые 6 часов в течение первых 24 часов, затем ежедневно;
– поддерживать АЧТВ на уровне 1.5–2.5;
– продолжать инфузии в течение 5–7 дней.
Подкожное введение гепарина: начать с дозы 17500 МЕ каждые 12 часов (или 250 МЕ/кг каждые 12 часов).
5. Каждый день определять уровень тромбоцитов из–за возможности развития тромбоцитопении.
6. Если больные до этого не получали варфарин, то его следует назначить в течение первых 24–48 часов от начала гепаринотерапии.
7. Продолжить лечение гепарином по крайней мере в течение 4–5 дней после назначения варфарина. У пациентов с массивным илеофеморальным тромбозом или легочной тромбоэмболией лечение гепарином проводится в течение не менее 10 дней.
8. Прекратить введение гепарина при достижении МНО > 2 в течение 48 часов.
У пациентов с факторами риска рецидивирования тромбозов в течение длительного времени должна проводиться интенсивная профилактика с использованием низкомолекулярного гепарина.
Катастрофический антифосфолипидный синдром
Прогноз катастрофического АФС во многом зависит от того, насколько рано поставлен диагноз и начата «агрессивная» терапия. Для лечения «катастрофического» АФС используется весь арсенал методов интенсивной и противовоспалительной терапии, применяемый для лечения критических состояний при ревматических болезнях (рис. 1) [35,36].
Рис. 1. Алгоритм лечения АФС
Эффективность терапии в определенной степени зависит от возможности устранить факторы, провоцирующие его развитие (например, подавление инфекции и/или активности основного заболевания). При подозрении на наличие инфекции следует незамедлительно назначать антибактериальную терапию, а при развитии гангрены конечностей проводить ампутацию. Важное значение имеет «неспецифическая» интенсивная терапия, например, гемодиализ у пациентов с быстро развивающейся почечной недостаточностью, вентиляция легких, введение инотропных препаратов и др.
Проведение интенсивной терапии глюкокортикоидами направлено не на лечение самих «тромботических» нарушений, а определяется необходимостью курирования синдрома «системного воспалительного ответа». Напомним, что синдром системного воспалительного ответа характеризуется диффузным воспалением сосудистого эндотелия, связанным с гиперпродукцией ФНО- a и ИЛ–1. Целый ряд клинических проявлений АФС, связанных как с тромбозом мелких сосудов, так и распространенным некрозом (например, дыхательный дистресс–синдром у взрослых и др.), являются показаниями для назначения высоких доз глюкокортикоидов. Обычно рекомендуется проведение пульс–терапии по стандартной схеме (1000 мг метилпреднизолона в день в течение 3–5 дней) с последующим назначением высоких доз глюкокортикоидов (1–2 мг/кг/день) перорально. Следует еще раз подчеркнуть, что сами по себе глюкокортикоиды не влияют на риск развития повторных тромбозов.
Внутривенный иммуноглобулин вводится в дозе 0,4 г/кг в течение 4–5 дней и особенно эффективен при наличии тромбоцитопении. Следует, однако, помнить, что внутривенный иммуноглобулин может вызывать нарушение функции почек, особенно у лиц пожилого возраста, получавших нефротоксические препараты.
«Катастрофический» АФС является единственным абсолютным показанием для проведения сеансов плазмафереза (рекомендуется удаление 2–3 литров плазмы в течение 3–5 дней) у пациентов АФС, которые следует сочетать с максимально интенсивной антикоагулянтной терапией, использованием для замещения свежезамороженной плазмы, а при наличии показаний – с проведением пульс–терапии ГК и циклофосфамидом. Плазмаферез – метод выбора при тромботической тромбоцитопенической пурпуре и тромботической микроангиопатической гемолитической анемии, нередко осложняющей КАФС.
Циклофосфамид (0,5–1,0 г в сутки) в определенной степени показан при развитии катастрофического АФС на фоне обострения СКВ и для предотвращения синдрома «рикошета» после проведения сеансов плазмафереза.
Данные, касающиеся возможности применения антицитокинов (например, ингибитора ФНО- a ), отсутствуют. Теоретическим основанием для их применения являются данные о существенном повышении уровня ФНО- a при АФС, в том числе катастрофическом АФС. Вероятно, введение инфликсимаба может быть потенциально показано пациентом с синдромом системного воспалительного ответа на фоне АФС.
Стандартом профилактики рецидивирующих потерь плода (а также венозных и артериальных тромбозов в послеродовом периоде) при АФС является применение низких доз АСК (81 мг/сут) в сочетании с нефракционированным гепарином или низкомолекулярным гепарином [37–39] в течение всего периода беременности и по крайней мере в течение 6 мес. после родов (табл. 3).
Основными недостатками гепарина являются различная биодоступность при подкожном введении и его неспецифическое связывание с белками плазмы (АТ III и факторы коагуляции), тромбоцитарными белками (например, тромбоцитарный фактор 4) и ЭК. При этом некоторые гепарин–связывающие белки относятся к белкам острой фазы воспаления, концентрация которых существенно увеличивается на фоне воспаления. Наконец, еще одно ограничение гепаринотерапии – снижение способности гепарина инактивировать тромбин, находящийся в комплексе с фибрином и фактор Xa, связанный с активированными тромбоцитами в образующемся тромбе. Поэтому гепарин не оказывает влияния на рост тромба, а после прекращения гепаринотерапии может наблюдаться «рикошетное» усиление коагуляции.
Препараты низкомолекулярного гепарина обладают преимуществами перед нефракционированным гепарином при лечении венозных тромбозов и акушерской патологии у пациентов АФС и почти полностью вытеснили последний [37] (табл. 4).
Недавно было проведено рандомизированное исследование, в котором сравнивалась эффективность низкомолекулярного гепарина в сочетании с АСК и внутривенным иммуноглобулином [40]. В исследование было включено 30 женщин с 3 и более спонтанными абортами в анамнезе. У женщин, получавших гепарин и АСК, число успешных родов (84%) было выше, чем у женщин, получавших внутривенный иммуноглобулин (57%).
При родоразрешении кесаревым сечением введение низкомолекулярных гепаринов отменяется за 2–3 дня и возобновляется в послеродовом периоде с последующим переходом на прием непрямых антикоагулянтов. Лечение АСК и гепарином позволяет снизить риск венозных и артериальных тромбозов, которые нередко развиваются у пациентов с АФС на фоне и после беременности [41].
Необходимо иметь в виду, что длительная терапия гепарином беременных женщин может приводить к развитию остеопороза, осложняющегося переломами костей скелета. Для уменьшения потери костной массы необходимо рекомендовать прием карбоната кальция (1500 мг) в сочетании с витамином D. Лечение низкомолекулярным гепарином реже приводит к остеопорозу, чем лечение нефракционированным гепарином. Одним из ограничений для применения низкомолекулярного гепарина является опасность развития эпидуральной гематомы при проведении регионарной анестезии. Поэтому, если предполагаются преждевременные роды, лечение низкомолекулярным гепарином следует прекратить не позже, чем на 36–й неделе беременности.
Использование непрямых антикоагулянтов при беременности в принципе противопоказано, так как приводит к варфариновой эмбриопатии, характеризующейся нарушением роста эпифизов и гипоплазией носовой перегородки, а также неврологическими нарушениями. Однако по данным недавно проведенного исследования назначение варфарина между 15 и 34 неделями беременности пациенткам с АФС (n=14) не ассоциировалось с тератогенным эффектом [101], а частота успешных родов (86%) была такая же, как и у женщин, принимавших низкие дозы АСК и низкомолекулярный гепарин (87%). Эти данные позволяют предположить, что в некоторых случаях у пациенток, нуждающихся в активной антикоагулянтной терапии (но не переносящих лечение гепарином) или имеющих тяжелые системные тромбозы (инсульт и др.), возможно назначение варфарина в сроки от 14 до 34 недели беременности. У пациенток, которым проводится искусственное зачатие или индукция овуляции, необходимо заменить варфарин на гепарин. Гепарин следует отменить за 12–24 часа до проведения операции, а через 6–8 часов возобновить терапию.
Лечение средними/высокими дозами глюкокортикоидов (ГК), популярное в 80–х годах, в настоящее время практически не применяется из–за побочных эффектов как у матери, так и у плода и отсутствия доказательств их эффективности. Более того, глюкокортикоидная терапия приводит к развитию тяжелых побочных эффектов, включая преждевременный разрыв мембраны, преждевременные роды, задержку роста плода, инфекции, преэклампсию, диабет, остеопению и остеонекроз. Однако перед родами отменять ГК у женщин, получавших их во время беременности, не следует, а во время родов им необходимо дополнительно вводить внутривенно ГК, для того чтобы избежать надпочечниковой недостаточности. Применение ГК оправдано при вторичном АФС (в сочетании с СКВ) и направлено на лечение основного заболевания. Лишь в некоторых случаях у пациенток, у которых невынашивание беременности не удается преодолеть на фоне стандартной терапии низкими дозами АСК и гепарином (а также внутривенным иммуноглобулином), возможно назначение преднизолона (20–40 мг/сут).
Применение внутривенного иммуноглобулина (0,4 г/кг в течение 5 дней каждый мес.) не имеет преимуществ перед стандартным лечением АСК и гепарином и показано только при неэффективности «стандартной» терапии АСК и гепарином [42–44]. Имеется несколько предварительных сообщений об определенной эффективности плазмафереза, однако в настоящее время этот метод используется крайне редко.
Следует подчеркнуть, что выявление аФЛ не влияет на исходы беременности у женщин, которым проводилось искусственное оплодотворение.
В таблице 5 перечислены общие рекомендации по ведению пациенток с АФС.
При соблюдении представленных рекомендаций удается увеличить частоту успешных родов у женщин с двумя и более эпизодами потери плода в анамнезе до 70–80%. Следует, однако, подчеркнуть, что даже в случае успешных родов у пациенток с АФС отмечается увеличение частоты преэкслампсии, задержки роста плода, преждевременных родов и других форм акушерской патологии. Дети у женщин с АФС, как правило, рождаются здоровыми, без признаков нарушения физического и нейропсихического развития, тромбозов и др., по крайней мере, в течение 5 лет наблюдения.
Умеренная тромбоцитопения, нередко наблюдающаяся у пациентов с АФС, не требует специального лечения. При вторичном АФС в рамках СКВ, тромбоцитопения обычно хорошо контролируется ГК, аминохинолиновыми препаратами, а в резистентных случаях – низкими дозами АСК.
Тактика лечения резистентной тяжелой тромбоцитопении ( 3 ), создающей угрозу кровотечений, до конца не разработана. Этим пациентам, наряду с применением ГК в высоких дозах, целесообразно назначение внутривенного иммуноглобулина. Имеются данные об определенной эффективности препарата даназол (слабый андроген) или дапсон.
В случае неэффективности высоких доз ГК методом «выбора» является спленэктомия [45], причем у подавляющего большинства пациентов отмечена стойкая нормализация уровня тромбоцитов.
Периоперационное ведение пациентов с АФС
У пациентов с АФС имеет место существенное увеличение риска тромбозов (особенно после операций на сосудах и клапанах сердца) [46] и нередко развитие катастрофического АФС. В целом пациенты АФС составляют группу очень высокого риска развития венозных тромбоэмболических осложнений в послеоперационном периоде [47].
Разработаны стандарты антикоагулянтной терапии для группы «высокого риска», к которой относятся пациенты АФС (табл. 6). Следует, однако, подчеркнуть, что эти рекомендации специально не апробировались при АФС.
По мнению D. Erkan и соавт. [47], пациентам с АФС необходимо проводить более интенсивную антикоагулянтную терапию и свести к минимуму время, в течение которого антикоагулянтная терапия приостанавливается. У пациентов, которые в течение длительного времени применяли варфарин, препарат следует назначить сразу после операции при отсутствии хирургических противопоказаний. Лечение гепарином следует продолжить до стабилизации МНО на терапевтическом уровне.
В случае необходимости ургентных операций у пациентов с АФС, получающих варфарин, следует перелить свежезамороженную плазму (содержит все факторы свертывания, в том числе витамин К, дефицит которого развивается на фоне приема варфарина). Пациентам с тромбоцитопений ( 9 /Л) или кровоточивостью следует назначать ГК и/или внутривенный иммуноглобулин. Переливание тромбоцитарной массы, как правило, не эффективно и может увеличивать риск развития тромбозов.
Общие рекомендации по ведению пациентов с АФС до, после и во время операции:
2. Во время операции
3. Назначение антикоагулянтов
4. Больные с трансплантированной почкой
Атеросклероз и артериальная гипертензия
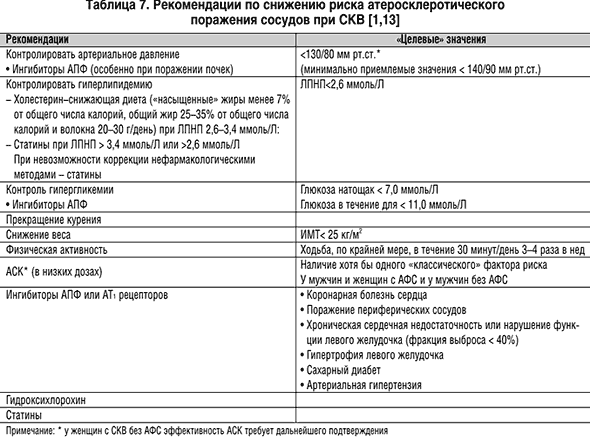
Учитывая высокий риск атеросклеротического поражения сосудов при СКВ, и особенно при АФС, профилактика атеротромботических нарушений (как и при сахарном диабете) показана практически всем пациентам [12,13] (табл. 7).
Для лечения сопутствующей артериальной гипертензии и сердечной недостаточности при АФС, вероятно, наиболее оправдано использование ингибиторов АПФ. Доказано, что терапия данными препаратами улучшает исход у пациентов с гипертонией, застойной сердечной недостаточностью и ИБС.
Перспективы фармакотерапии АФС
Очевидно, что высокий риск развития коронарной болезни сердца при АФС уже сам по себе является веским основанием для широкого применения статинов у пациентов с этими заболеваниями. Однако учитывая данные об иммунных механизмах патогенеза атеротромбоза при СКВ и АФС, применение статинов при этих патологических состояниях имеет очень важные дополнительные патогенетические и клинические обоснования [48,49]. Известно также, что статины оказывают профилактические действие не только в отношении ИМ, но и других сосудистых осложнений – инсульта и даже тромбоза глубоких вен голени, которые являются наиболее характерными клиническими проявлениями АФС.
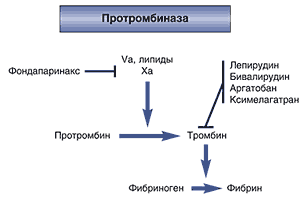
Хотя эффективность антикоагулянтов и ингибиторов аггрегации тромбоцитов при АФС не вызывает сомнения, практическое использование этих препаратов имеет свои ограничения из–за недостаточно высокой эффективности, токсичности (или того и другого). Для «стандартных» антикоагулянтов характерно узкое «терапевтическое окно» (трудность достигнуть адекватной антикоагуляции без риска развития кровотечений), а также выраженная вариабельность терапевтического ответа у отдельных пациентов, что диктует необходимость тщательного лабораторного мониторинга. Все это вместе взятое послужило мощным стимулом для разработки новых антитромботических агентов [50–52]. К ним относятся как уже широко применяющиеся в клинической практике тиоперидиновые ингибиторы АФД рецепторов (тиклопедин и клопидогрел) и ингибиторы тромбоцитарных (GPIIb/IIIa) рецепторов, так и новые антикоагулянты – прямые ингибиторы тромбина, ингибиторы фактора X, ингибиторы тканевого фактора (ТФ), рекомбинантный активированный белок С и др. (табл. 8 и рис. 2).
Рис. 2. Механизмы действия новых антикоагулянтов
В последние годы благодаря расшифровке структуры антигенов, которые являются мишенями для аФЛ, созданы реальные предпосылки для разработки «патогенетической» терапии этого заболевания. Одно из таких принципиально новых направлений фармакотерапии АФС, как аутоиммунной тромбофилии, связано с возможностью индукции специфической В–клеточной толерантности к потенциальным аутоантигенам, индуцирующим синтез «патогенных» аФЛ. Таким «патогенным» типом аутоантител при АФС могут быть антитела к b 2–гликопротеину (ГП)–I.
Свойствами b 2–ГП–I «толерагена» обладает препарат LJP 1082. Он представляет собой рекомбинантную тетравалентную молекулу, состоящую из 4–х копий домена 1 b 2–ГП–I человека (соединены полиэтиленгликольными мостиками), в котором присутствует, как полагают, основной В–клеточный «аутоэпитоп» этого антигена [53]. Полагают, что LJP 1082 обладает способностью связываться с b 2–ГПI–специфическими В–лимфоцитами и в отсутствие Т–клеточного сигнала индуцировать анергию или апоптоз В–клеток, синтезирующих антитела к b 2–ГПI. Недавно было проведено несколько клинических испытаний (в рамках I/II фаз) [54,55], в которых продемонстрирована высокая безопасность и переносимость лечения этим препаратом.
1. Levine J, Branch DW, Rauch J. The antiphospholipid syndrome. N Engl J Med 2002; 346: 752–763
2. Алекберова ЗС, Насонов ЕЛ., Решетняк ТМ., Раденска–Лоповок СГ. Антифосфолипидный синдром: 15 лет изучения в России В кн: Избранные лекции по клинической ревматологии. Москва, Медицина. Под редакцией В.А.Насоновой, Н.В.Бунчука 2001, 132–148.
3. Cuadrado, MJ. Treatment and monitoring of patients with antiphospholipid antibodies and thrombotic history (Hughes syndrome). Curr Rheumatol Rep 2002; 4:392
4. Roubeu RAS. Treatment of the antiphospholipid syndrome. Curr Opin Rheumatol 2002; 14: 238–242
5. Ruiz–Irastorza G, Khamashta MA, Hughes GRV. Antiagregant and anticoagulant therapy in systemic lupus erythematosus and Hughes dyndrome. Lupus 2001;10: 241–245.
6. Derksen R.H,M., de Groot Ph G., Nieuwenhuis H,K,M Christiaens G,C.M.L. How to treat women with antiphospholipid antibodies in pregnancy. Ann. Rheum. Dis., 2001; 60: 1–3
7. Lockwood C.J., Schur P.H. Monitoring and treatment of pregnant women with the antiphospholipid antibody syndrome. UpToDate 2002; 10, No,2
8. Berman BL, Schur PH, Kaplan AA. Prognosis and therapy of the antiphospholipid antibody syndrome. UpToDate 2004; 11.3
9. Roubey RAS. New approaches to prevention of thrombosis in the antiphospholipid syndrome: hopes, trials, and tribulations. Arthritis Rheum 2003; 48: 3004–3008.
10. Насонов Е.Л. Современные подходы к профилактике и лечению антифосфолипидного синдрома. Терапевт архив 2003;5:83–88.
11. Petri M. Evidence–based management of thrombosis in the antiphospholipid antibody syndrome. Curr Rheumatol Report 2003; 5: 370–373.
12. Salmon JE, Roman MJ. Accelerated atherosclerosis in systemic lupus erythematosus: implication for patients management. Curr Opin Rheumatol 2001; 13: 341–344
13. Wajed J, Ahmad Y, Durrington PN, Bruce IN. Prevention of cardiovascular disease in systemic lupus erythematosus – proposed guidelines for risk factor management. Rheumatology 2004; 43: 7–12
14. Alarcon–Segovia D, Boffa MC, Branch W, et al. Prophylaxis of the antiphospholipid syndrome: a consensus report. Lupus 2003; 12: 499–503.
15. Erkan D, Merrill JT, Yazici Y et al. High Thrombosis rate after fetal loss in antiphospholipid syndrome: effective prophylaxis with aspirin. Arthr Rheum 2001; 44: 1466–1469.
16. Erkan D, Yazici Y, Peterson MG et al. A cross–sectional study of clinical thrombotic risk factors and preventive treatment in antiphospholipid syndrome. Rheumatology (Oxford) 2002; 41: 924–929.
17. Насонов Е.Л., Иванова М.М. Антималярийные (аминохинолиновые) препараты: новые фармакологические свойства и перспективы клинического применения Клин. фармакол. терапия 1998, 3:65–68.
18. Yoon KH. Sufficient evidence to consider hydroxychloroquine as an adjunct therapy in antiphospholipid antibody (Hughes`) syndrome. J. Rheumatol., 2002; 29; 1574–1575.
19. Meroni PL, Moia M, Derksen RHWM, et al. Venous thromboembolism in the antiphospholipid syndrome: management guidelines for second prophylaxis. Lupus 2003; 12: 504–507.
20. Brey RL, Chapman J, Levine SR et al. Stroke and the antiphospholipid syndrome: consensus meeting Taormina 2002. Lupus 2003; 12: 508–513.
21. Valentini KA, Hull RD. Clinical use of warfarin. UpToDate 2003; 12.1
22. Hirsh J, Fuster V, Ansell J, Halperin JL. American Heart Association/American College of Cardiology Foundation Guide to warfarin therapy. Circulation 2003; 107; 1692–1711.
23. van Dongen CJJ, Vink R, Hutten BA Buller HR, Prins MH. The incidence of recurrent venous thromboembolism after treatment with vitamin K antagonists in relation to time since first events. A meta–analysis. Arch Intern Med 2003; 163: 1285–1293.
24. Ruiz–Irastorza G, Khamashta MA, Caetellino G, Hughes GRV. Systemic lupus erythematosus. Lancet 2001; 357: 1027–1032.
25. Crowther MA, Ginsberg JS, Julian J, et al. A comparison of two intensities of warfarin for the prevention of recurrent thrombosis in patients with the antiphospholipid antibody syndrome. New Engl J Med 2003; 349: 1133–1138.
26. Adam HP. Emergent use of anticoagulantion for treatment of patients with ischemic stroke. Stroke 2002; 33: 856–861.
27. Sandercock P, Gubitz G, Foley P, Counsell C. antiplatelet therapy for acute ischemic stroke. Cochrane Database Syst Rev 2003; CD00029
28. Ruiz–Irastorza G, Khamashta M, Hunt B et al. Bleeding and recurrent thrombosis in definite antiphospholipid syndrome. Analysis of a series of 66 patients with oral anticoagulation to a target international normalization ratio of 3.5. Arch Untern Med, 2002; 162: 1164–1169.
29. Moll, S, Ortel, TL. Monitoring warfarin therapy in patients with lupus anticoagulants. Ann Intern Med 1997; 127:177.
30. Robert, A, Le Querrec, A, Delahousse, B, et al. Control of oral anticoagulation in patients with the antiphospholipid syndrome – Influence of the lupus anticoagulant on international normalized ratio. Thromb Haemost 1998; 80:99.
31. Tripodi, A, Chantarangkul, V, Clerici, M, et al. Laboratory control of oral anticoagulant treatment by the INR system in patients with the antiphospholipid syndrome and lupus anticoagulant. Results of a collaborative study involving nine commercial thromboplastins. Br J Haematol 2001; 115: 672.
32. Решетняк ТМ, Широкова ИЕ, Кондратьева ДВЮ и соавт. Варфарин в комплексной терапии антифосфолипидного синдрома: предварительные результаты. Науно–практическая ревматология 2003; 3: 37–41.
33. Shulman S. Care of patients receiving long–term anticoagulant therapy. New Engl J Med 2003; 349: 675–683.
34. Weitz J.I. Low–molecular–weight heparins. New Engl J Med 1997; 337: 688–698.
35. Aherson RA, Cervera R, de Groot P, Erkan D, et al. Catastrophic antiphospholipid syndrome (CAPS): International consensus statement on classifacation criteria and treatment guidelanes. Lupus 2003; 12: 530–544.
36. Erkan D, Cervra R, Asherson RA. Catastrophic antiphospholipid syndrome; where do we stand. Arthritis Rheum 2003; 48: 3320–327.
37. Lockwood CJ, Schur PH. Monitoring and treatment of