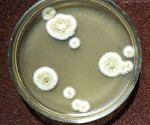
антитела к аспергиллам что это
Антитела к аспергиллусу IgG, Aspergillus lgG п/кол.
Описание
Антитела к аспергиллусу IgG, Aspergillus lgG полуколичественный — выявление антител IgG, которые вырабатываются иммунной системой в ответ на инфицирование возбудителем гриба рода аспергилл (Aspergillus), а также являются показателем текущей или не выявленной ранее инфекции.
Аспергиллёз — инфекционное заболевание, вызываемое различными видами плесневых грибов рода Aspergillus, протекающее с преимущественным поражением бронхолёгочной системы. Аспергиллы могут обнаруживаться и у здоровых людей.
Механизм заражения — аэрогенный (при вдыхании спор грибка), фекально-оральный (при употреблении продуктов питания, обсеменённых грибком), а также через слизистые оболочки и повреждённые кожные покровы.
Причина аспергиллёза — пыль и не ответственное отношение к уборке помещений.
Зачастую заболевание развивается у лиц с ослабленным иммунитетом при вдыхании большого количества спор аспергилл с пылью.
Клиническая картина при аспергиллёзе
Формы аспергиллёза:
Антитела при аспергиллёзе
В ответ на инфицирование, иммунной системой вырабатываются обеспечивающие иммунный ответ специфические иммуноглобулины (антитела). Антитела IgG выявляются в крови уже на ранней стадии заражения.
Исследование антител класса IgG необходимо проводить в динамике. Нарастание уровня концентрации антител IgG свидетельствует о текущем заболевании. При хронических формах заболевания IgG сохраняются в крови на протяжении длительного времени.
Интерпретация результатов
Единицы измерения: УЕ*
Положительный результат будет сопровождаться дополнительным комментарием с указанием коэффициента позитивности пробы (КП*):
Аспергиллез IgG (кач.) в Москве
Выявление антител класса IgG, специфичных к возбудителю инфекционного заболевания аспергиллез — плесневым грибам рода Aspergillus. Эти антитела являются маркерами заболевания, начиная с ранних стадий, а также протекающего хронически. Анализ назначается для раннего выявления аспергиллеза, который при отсутствии лечения может переходить в тяжелые стадии, иногда со смертельным исходом.
Приём и исследование биоматериала
Когда нужно сдавать анализ Аспергиллез IgG (кач.)?
Подробное описание исследования
Грибковые инфекции, вызываемые Aspergillus, — аспергиллезы — очень разнообразны. Они варьируются от подобного аллергии заболевания до чрезвычайно серьезной, генерализованной (затрагивающей много органов и систем) инфекции, приводящей иногда к смертельному исходу. Тяжесть аспергиллеза зависит от нескольких факторов, наиболее важным из которых является состояние иммунной системы человека.
Аллергический бронхолегочный аспергиллез (АБЛА)
Это аллергическое заболевание, которое довольно часто встречается у пациентов с астмой: по оценкам, 20% астматиков могут заразиться этой патологией в какой-то момент своей жизни. АБЛА также часто встречается у пациентов с муковисцидозом. Симптомы аналогичны классическим симптомам астмы: приступы плохого самочувствия, кашля и хрипов. У некоторых пациентов отхаркивают коричневатые слизистые пробки. При отсутствии лечения АБЛА может привести к необратимому повреждению легких (фиброзу).
Аспергиллома
При этом заболевании аспергиллы размножаются в полости легкого, образовавшейся в результате перенесенного заболевания, такого как туберкулез или саркоидоз. Споры в полости прорастают, образуя внутри нее мицелиальный (образованный слоем грибка) шар. По мере роста внутри легких грибок выделяет токсичные и аллергические вещества, ухудшающие состояние пациента.
Заболевание может остаться незамеченным, особенно на ранних стадиях. Похудение, хронический кашель и усталость — классические симптомы поздних стадий грибковой инфекции. Кровохарканье (кашель с кровью) встречается у 50-80% больных.
Аспергиллярный синусит
Это заболевание локализуется в носовых пазухах. У пациентов со здоровой иммунной системой оно приводит к хроническим головным болям, дискомфорту в области лица и заложенности носа. Дренажа носовых пазух обычно бывает достаточно для излечения. Если грибок поселился глубоко в носовых пазухах, необходима операция в сочетании с противогрибковым лечением. Если у пациентов нарушена иммунная система (например, лейкоз или у реципиентов трансплантата костного мозга), аспергиллярный синусит может перейти в инвазивный аспергиллез. Симптомы включают жар, лицевую боль, насморк и головную боль.
Инвазивный аспергиллез
Большое количество пациентов с нарушениями иммунитета умирают от этой инфекции. Шансы на выживание увеличиваются, если диагноз поставлен на ранней стадии. Пациенты с риском инвазивного аспергиллеза — это люди со сниженной иммунной защитой, в частности пациенты перенесшие трансплантацию костного мозга, пациенты, проходящие лечение рака, у которых мало белых кровяных телец, пациенты с тяжелыми ожогами или СПИДом. Пациенты с инвазивным аспергиллезом обычно испытывают лихорадку и легочные симптомы (кашель, боль в груди, недомогание и затрудненное дыхание), которые не проходят при лечении антибиотиками. Грибок может распространяться через кровь в мозг и другие органы, например, в глаза, сердце, почки и кожу.
Аспергиллы могут размножаться в пище и таким образом попадать в организм человека. Возможно попадание возбудителя через поврежденную кожу. Однако чаще всего споры грибов попадают в организм человека при вдыхании, так как они легко распространяются по воздуху. Аспергиллезу подвержены в основном люди с ослабленным иммунитетом, страдающие другими легочными заболеваниями либо тяжелыми болезнями, такими как рак, СПИД.
При аспергиллёзе для предотвращения серьезных осложнений крайне важна ранняя диагностика. Иммуноглобулины класса G (IgG) обнаруживаются, начиная с ранней фазы инфекции. Этот тип антител сохраняется у человека значительно дольше, чем иммуноглобулины других классов (IgА и IgЕ). Возрастающие во времени титры IgG свидетельствуют об активном заболевании. При хроническом аспергиллезе IgG могут находиться в крови продолжительное время — от года и более. Низкие титры IgG свидетельствуют либо о ранней стадии заболевания, либо о заболевании, перенесенном в прошлом.
Антитела к аспергиллам что это
Выявление в крови специфических антител класса IgG, которые вырабатываются в ответ на инфекцию, вызванную грибом рода аспергилл (Aspergillus fumigatus).
Аспергиллез, черная гниль.
Иммуноферментный анализ (ИФА).
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
Общая информация об исследовании
Грибы рода Aspergillus вызывают тяжелое заболевание – аспергиллез. При этом локализация патологического процесса может быть весьма разнообразна. В первую очередь аспергилл поражает бронхолегочную систему, это самый распространенный вариант микоза легких.
Аспергиллы продуцируют ферменты (протеолитический, сахаролитический, липолитический и др.) и эндотоксины. Выделение различных типов токсинов (альфа-токсина, глиотоксина и др.) в окружающую среду и в организм человека при прогрессировании заболевания также является характерной чертой Aspergillus fumigatus.
Соединения, синтезируемые аспергиллом (в том числе сериновые и аспарагиновые протеазы, металлопротеиназы, дипептидилпептидазы и фосфолипазы и др.), являются сильными аллергенами. В результате аллергической реакции на них или при развитии инфекционного процесса могут поражаться и другие органы – придаточные пазухи носа, гортань, трахея и бронхи – с возможным распространением инфекции в кожу, в желудочно-кишечный тракт, головной мозг, сердце. Известно, что аспергиллы являются причиной аллергического бронхолегочного аспергиллеза, хронического некротического легочного аспергиллеза, могут вызывать бронхиальную астму, экзогенный аллергический альвеолит.
Заразиться можно, употребив пищу, пораженную аспергиллами, при вдыхании грибковых спор, а также при их попадании на поверхность раны. Способствуют заражению болезни, ослабляющие иммунитет, а также определенная сфера деятельности человека, например работа с голубями, которые являются переносчиком заболевания.
Кроме того, к факторам, повышающим риск инфицирования аспергиллезом, относят:
Самые распространенные из них – это нейтропения и использование кортикостероидов.
При инфицировании в организме запускаются защитные механизмы – иммунный ответ, – и в результате происходит выработка специфических антител, чье действие направлено на обезвреживание и гибель возбудителя. В силу особенностей Aspergillus fumigatus устранить патоген за счет собственных ресурсов организму не удается, поэтому чаще всего требуется серьезное и длительное лечение.
Антитела IgG могут быть обнаружены уже в раннюю фазу заражения. Они присутствуют у человека значительно дольше, чем антитела других классов (IgА и IgЕ), и могут выявляться в сыворотке через 12 месяцев и более после первого контакта с антигенами возбудителя. Для острого периода характерны нарастающие или высокие титры антител IgG. При хронических формах заболевания IgG могут обнаруживаться в течение более длительного периода.
Для уверенной постановки диагноза при поражениях бронхов и легких необходимо учитывать:
Подтверждением диагноза служит выявление самого возбудителя из различных биоматериалов (из мокроты, материала, взятого из бронхов, биоптатов пораженных органов). По клиническим и рентгенологическим данным аспергиллез дифференцируют с другими микозами (нокардиозом, гистоплазмозом, кандидозом), а также с туберкулезом легких, абсцессами легких, новообразованиями, хроническим бронхитом.
Для чего используется исследование?
Когда назначается исследование?
Что означают результаты?
Что может влиять на результат?
Перекрестная реакция на другого возбудителя или аллерген (например, на продукты, в процессе изготовления которых применялись ферментационные процессы).
Кто назначает исследование?
Врач общей практики, терапевт, пульмонолог, фтизиатр, инфекционист, оториноларинголог.
Аспергиллез
МКБ-10
Общие сведения
Причины аспергиллеза
Возбудителями аспергиллеза у человека могут выступать следующие виды плесневых грибков рода Aspergillus: A. flavus, A. Niger, A. Fumigatus, A. nidulans. A. terreus, A. clavatus. Аспергиллы являются аэробами и гетеротрофами; способны расти при температуре до 50°С, длительно сохраняться при высушивании и замораживании. В окружающей среде аспергиллы распространены повсеместно – в почве, воздухе, воде. Благоприятные условия для роста и размножения аспергилл имеются в вентиляционных и душевых системах, кондиционерах и увлажнителях воздуха, старых вещах и книгах, сырых стенах и потолках, длительно хранящихся пищевых продуктах, сельскохозяйственных и комнатных растениях и др.
Заражение аспергиллезом чаще всего происходит ингаляционным путем при вдыхании частиц пыли, содержащих мицелий гриба. Наибольшему риску возникновения заболевания подвержены сельскохозяйственные рабочие, работники бумагопрядильных и ткацких предприятий, мукомолы, а также заводчики голубей, поскольку голуби, чаще других птиц, болеют аспергиллезом. Возникновению грибковой инфекции способствует инфицирование при проведении инвазивных процедур: бронхоскопии, пункции околоносовых пазух, эндоскопической биопсии и др. Не исключен контактный путь передачи аспергиллеза через поврежденные кожные покровы и слизистые оболочки. Также возможно алиментарное инфицирование при употреблении контаминированных аспергиллами продуктов питания (например, куриного мяса).
Кроме экзогенного инфицирования аспергиллами, известны случаи аутозаражения (при активации грибков, обитающих на коже, слизистой зева и дыхательных путей) и трансплацентарного инфицирования. К факторам риска заболеваемости аспергиллезом относятся иммунодефициты любого генеза, хронические заболевания дыхательной системы (ХОБЛ, туберкулез, бронхоэктатическая болезнь, бронхиальная астма и др.), сахарный диабет, дисбактериоз, ожоговые травмы; прием антибиотиков, кортикостероидов и цитостатиков, проведение лучевой терапии. Нередки случаи развития микозов смешанной этиологии, вызываемых различными видами грибков – аспергиллами, кандида, актиномицетами.
Классификация аспергиллеза
Таким образом, в зависимости от путей распространения грибковой инфекции различают эндогенный (аутоинфекцию), экзогенный (с воздушно-капельным и алиментарным путем передачи) и трансплацентарный аспергиллез (с вертикальным путем заражения).
По локализации патологического процесса выделяют следующие формы аспергиллеза: бронхолегочную (в т. ч. аспергиллез легких), ЛОР-органов, кожную, глазную, костную, септическую (генерализованную) и пр. На первичное поражение респираторного тракта и легких приходится около 90% всех случаев аспергиллеза; придаточных пазух носа – 5%. Вовлечение остальных органов диагностируются менее чем у 5% больных; диссеминация аспергиллеза развивается примерно в 30% случаев, преимущественно, у ослабленных лиц с отягощенным преморбидным фоном.
Симптомы аспергиллеза
У больных с сопутствующими заболеваниями дыхательной системы (легочным фиброзом, эмфиземой, кистами, абсцессом легкого, саркоидозом, туберкулезом, гипоплазией, гистоплазмозом) нередко формируется аспергиллома легких – инкапсулированный очаг, содержащий гифы гриба, фибрин, слизь и клеточные элементы. Гибель пациентов с аспергилломой может наступить в результате легочного кровотечения или асфиксии.
Аспергиллез ЛОР-органов может протекать в виде наружного или среднего отита, ринита, синусита, тонзиллита, фарингита. При аспергиллезном отите вначале возникает гиперемия, шелушение и зуд кожи наружного слухового прохода. С течением времени слуховой проход заполняется рыхлой сероватой массой, содержащей нити и споры гриба. Возможно распространение аспергиллеза на барабанную перепонку, сопровождающееся резкими колющими болями в ухе. Описаны поражения верхнечелюстных и клиновидных пазух, решетчатой кости, переход грибковой инвазии на орбиты. Глазной аспергиллез может принимать форму конъюнктивита, язвенного блефарита, узелкового кератита, дакриоцистита, блефаромейбомита, панофтальмита. Нередки осложнения в виде глубоких язв роговицы, увеита, глаукомы, потери зрения.
Аспергиллез кожи характеризуется появлением эритемы, инфильтрации, коричневатых чешуек, умеренного зуда. В случае развития онихомикоза возникает деформация ногтевых пластин, изменение цвета на темно-желтый или коричневато-зеленоватый, крошение ногтей. Аспергиллез ЖКТ протекает под видом эрозивного гастрита или энтероколита: для него типичны запах плесени изо рта, тошнота, рвота, диарея.
Генерализованная форма аспергиллеза развивается при гематогенной диссеминации аспергилл из первичного очага в различные органы и ткани. При данной форме заболевания возникают аспергиллезный эндокардит, менингит, энцефалит; абсцессы головного мозга, почек, печени, миокарда; поражение костей, ЖКТ, ЛОР-органов; аспергиллезный сепсис. Летальность от септической формы аспергиллеза очень высока.
Диагностика аспергиллеза
В зависимости от формы микоза пациенты направляются на консультацию к специалисту соответствующего профиля: пульмонологу, отоларингологу, офтальмологу, микологу. В процессе диагностики аспергиллеза большое внимание уделяется анамнезу, в т. ч. профессиональному, наличию хронической легочной патологии и иммунодефицита. При подозрении на бронхолегочную форму аспергиллеза проводится рентгенография и КТ легких, бронхоскопия с забором мокроты, бронхоальвеолярный лаваж.
Основу диагностики аспергиллеза составляет комплекс лабораторных исследований, материалом для которых могут служить мокрота, промывные воды из бронхов, соскобы с гладкой кожи и ногтей, отделяемое из пазух носа и наружного слухового прохода, отпечатки с поверхности роговицы, кал и пр. Аспергиллы могут быть обнаружены с помощью микроскопии, культурального исследования, ПЦР, серологических реакций (ИФА, РСК, РИА). Возможно проведение кожно-аллергических проб с антигенами аспергилл.
Дифференциальная диагностика аспергиллеза легких проводится с воспалительными заболеваниями респираторного тракта вирусной или бактериальной этиологии, саркоидозом, кандидозом, туберкулезом легких, муковисцидозом, опухолями легких и др. Аспергиллез кожи и ногтей имеет сходство с эпидермофитией, рубромикозом, сифилисом, туберкулезом, актиномикозом.
Лечение аспергиллеза
При аспергилломе легких показана хирургическая тактика – экономная резекция легкого или лобэктомия. В процессе лечения любой формы аспергиллеза необходимо проведение стимулирующей и иммунокорригирующей терапии.
Прогноз и профилактика аспергиллеза
Наиболее благоприятное течение отмечается при аспергиллезе кожи и слизистых оболочек. Летальность от легочных форм микоза составляет 20-35%, а у лиц с иммунодефицитом – до 50%. Септическая форма аспергиллеза имеет неблагоприятный прогноз. К мерам, позволяющим предупредить заражение аспергиллезом, относятся мероприятия по улучшению санитарно-гигиенических условий: борьба с пылью на производстве, ношение работниками мельниц, зернохранилищ, овощехранилищ, ткацких предприятий индивидуальных средств защиты (респираторов), улучшение вентиляции цехов и складов, регулярное микологическое обследование лиц из групп риска.
Антитела к аспергиллам что это
Clinical Infections Diseases 2000; 30:676-709
David A. Stevens, Virginia L. Kan, Marc A. Judson, Vicki A. Morrison, Stephen Dummer, David W. Denning, John E. Bennett, Thomas J. Walsh, Thomas F. Patterson, George A. Pan key
Практические рекомендации по лечению аспергиллеза
Аспергиллез имеет различные клинические проявления. В данном руководстве рассматриваются три основных заболевания: инвазивный аспергиллез с вовлечением различных органов и систем (в частности с поражением легких), легочная аспергиллема и аллергический бронхолегочный аспергиллез. Приведенные здесь рекомендации тщательно отобраны, но все же за читателем остается право более детально изучить соответствующие вопросы в оригинальных статьях, посвященных данной теме.
Инвазивный аспергиллез
Учитывая высокую летальность заболевания у больных с иммунной недостаточностью, особенно важны быстрая диагностика и немедленное начало лечения уже при одном подозрении на инвазивный аспергиллез (BIII). При быстром прогрессировании болезни в самом начале необходимо внутривенное введение противогрибковых средств (BIII). Наибольший опыт накоплен в отношении амфотерицина В деоксихолата, который применяется в максимально переносимых дозах (1-1,5 мг/кг/сут) даже при умеренном повышении в крови уровня креатинина (BIII). У пациентов с нарушенной функцией почек или с нефротоксичностью, развившейся при применении амфотерицина деоксихолата, показаны жировые производные амфотерицина (АII). Итраконазол может служить альтернативой амфотерицину у части пациентов, у которых возможны пероральный прием, хорошая всасываемость (о чем судят по уровню препарата в крови) и исключена возможность взаимодействия с другими лекарствами (ВII). Пероральный итраконазол также показан для продолжения терапии у больных, которые ответили на начальную внутривенную терапию (СIII). Лечение должно продолжаться и после разрешения болезни, а также при наличии факторов, предрасполагающих к развитию аспергиллеза (BIII). В определенных ситуациях может использоваться адъювантная терапия, в частности хирургическое лечение, химио- и иммунотерапия (СIII).
Аспергиллема
В отношении аспергиллемы до настоящего времени не разработана оптимальная тактика лечения. Терапия, в основном, направлена на предупреждение жизнеугрожающего легочного кровотечения. Определяющим может быть хирургическое удаление аспергиллемы, но из-за серьезных осложнений оно применяется у пациентов высокого риска, например, с жизнеугрожающим легочным кровотечением, а также у больных с саркоидозом, иммунологическими нарушениями и при нарастании уровня специфических IgG к аспергилле (СIII). Пациенты, подлежащие оперативному вмешательству, должны иметь удовлетворительные показатели дыхательной функции. Эмболизация бронхиальных артерий может использоваться как временная процедура у больных с легочным кровотечением. При этом также может оказаться полезным эндобронхиальное и внутриполостное введение противогрибковых средств. Так как большинство аспергиллем не является причиной жизнеугрожающего легочного кровотечения, необходимо тщательно взвесить риск и стоимость хирургического лечения в сравнении с предполагаемым клиническим эффектом.
Аллергический бронхолегочный аспергиллез (АБЛА)
Несмотря на отсутствие рандомизированных исследований, имеющиеся данные подтверждают целесообразность применения кортикостероидов при обострении АБЛА (АII). Нет единого мнения насчет оптимальной дозы и длительности терапии, однако по существующим на данный момент данным рекомендуется начальная доза 0,5 мг/кг/сут преднизолона. Снижение дозы рассматривается индивидуально в зависимости от течения заболевания (BIII). При этом одних клинических симптомов может быть недостаточно для принятия такого решения, так как значительное повреждение легких может протекать асимптоматично. Повышение сывороточного уровня IgЕ, новые или прогрессирующие старые инфильтраты в легких, ухудшение спирометрических показателей говорят о необходимости применения кортикостероидов (ВII). Повторяющиеся приступы бронхиальной астмы у больных АБЛА предполагают постоянную кортикостероидную терапию (BIII). Применение итраконазола может способствовать снижению дозы кортикостероидов (ВII).
Таблица1
Категории обоснованности рекомендаций по терапии заболеваний, вызываемых Aspergillus
Так как число заболеваний, вызванных аспергиллой, растет, необходимо проведение рандомизированных сравнительных исследований. Имеющиеся рекомендации представляют собой компромисс и консенсус между теми, кто изучает эти заболевания. Рекомендации составлены на основании опубликованных работ и собственного опыта, включая отдельные случаи, открытые и некоторые сравнительные исследования.
Грибы рода Aspergillus представляют собой широко распространенный сапрофит. Наиболее частым видом, вызывающим заболевания, является Aspergillus fumigatus, за ним следует Aspergillus flavus. Также доказана патогенная роль Aspergillus amstelodami, Aspergillus avenaceus, Aspergillus candidus, Aspergillus cameus, Aspergillus caesiellus, Aspergillus clavatus, Aspergillus glaucus, Aspergillus granulosus, Aspergillus nidulans, Aspergillus niger, Aspergillus oryzae, Aspergitius quadrilineatus, Aspergillus restrictus, Aspergillus sydowi, Aspergillus terreus, Aspergillus ustus и Aspergillus versicolor. Частота и относительная значимость этих инфекций возрастает во всех развитых странах. Это возможно связано с увеличением продолжительности жизни (а, следовательно, и числа) пациентов с иммунными нарушениями при СПИДе, злокачественных опухолях, интенсивной цитотоксической терапии, трансплантациях органов, с одной стороны, а также с улучшением результатов лечения и профилактики кандидозов, с другой стороны.
Данные рекомендации созданы с целью предложить адекватное и эффективное лечение трех основных заболеваний, вызываемых грибами рода Aspergillus. К ним относятся инвазивный аспергиллез, АБЛА и аспергиллема. Эти рекомендации рассматриваются как общие и могут быть модифицированы в конкретных клинических ситуациях. Они основываются на научных публикациях и документально подтвержденной информации и в большей мере касаются терапии. Однако рекомендации не претендуют на всеобъемлющую полноту. Категории обоснованности рекомендаций и качества доказательств представлены в таблицах 1 и 2. Профилактика и эмпирическая терапия инвазивного аспергиллеза у пациентов с нейтропенией рассматривались в предыдущих публикациях [1] и поэтому в этой статье не обсуждаются.
Общие и конкретные комментарии, касающиеся противогрибковых средств, были даны в предыдущих публикациях данной серии. Препараты, доступные сегодня для лечения аспергиллеза, включают известный в клинике более 40 лет амфотерицин В в форме деоксихолата 3, три жировые формы амфотерицина В <5-12] и итраконазол-триазольное соединение в пероральной и внутривенной формах 13. Наибольший опыт накоплен в отношении лечения аспергиллеза деоксихолатом амфотерицина В и хирургическими методами. Сейчас активно рассматриваются новые подходы в терапии, особенно у пациентов с быстро прогрессирующим аспергиллезом.
Итраконазол взаимодействует со многими лекарственными веществами, что особенно важно у больных с высоким риском развития аспергиллеза, одновременно получающих другие препараты. У таких пациентов часто обнаруживается гипохлоргидрия и/или энтеропатия как результат основного заболевания. Поэтому при использовании перорального итраконазола необходимо убедиться в адекватной всасываемости по уровню препарата в сыворотке крови (ВII). Предпочтение следует отдавать пероральной суспензии итраконазола на основе циклодекстрина, так как ее всасываемость лучше по сравнению с капсулированным итраконазолом 22. Хотя уже доступна внутривенная форма препарата, данных о ее клиническом использовании очень мало.
При инвазивном аспергиллезе многие врачи рекомендуют применять максимальные дозы препаратов. Например, для амфотерицина В деоксихолата это составляет 1-1,5 мг/кг/сут, для жировых производных амфотерицина >= 5 мг/кг/сут и > =400 мг/сут для итраконазола (BIII). Повышение уровня креатинина в крови не редко наблюдается при применении амфотерицина В деоксихолата, и опытные клиницисты обычно не изменяют дозу препарата, так как нефротоксичность в этом случае невелика.
Таблица 2
Степень качества доказательств рекомендаций по противогрибковой терапии заболеваний, вызываемых Aspergillus
доказано по крайней мере в одном рандомизированном контролируемом исследовании
Инвазивный аспергиллез. Инвазивный аспергиллез легких.
Прогрессирующее течение заболевания и его устойчивость к лечению частично объясняется способностью возбудителя к быстрому росту и инвазии кровеносных сосудов.
Высев аспергиллы при бактериологическом исследовании материала, полученного из дыхательных путей (мокрота, смывы из носа и др.), у иммунокомпетентного пациента обычно является свидетельством колонизации, тогда как у иммунокомпрометированного может указывать на инвазивный аспергиллез. У больных лейкозом или после трансплантации костного мозга высев грибов в 80-90% случаев свидетельствует о течении аспергиллеза [31, 32]. При рентгенографическом исследовании в поздних стадиях заболевания можно обнаружить характерные клиновидные участки затемнения или полости сопряженные с плеврой [33, 341. На компьютерной томограмме в начале заболевания можно увидеть «ореол» (участок разрежения, вокруг нодулярного дефекта легочной ткани), что, по сути, является отеком или кровоизлиянием вокруг ишемического очага. По мере прогрессирования на томограмме становится различим «полумесяц», образованный воздушной полостью вокруг легочного узла и обусловленный сокращением некротизированной ткани. Эти рентгенологические симптомы помогают в диагностике и позволяют судить о протяженности поражения тканей, однако нужно учитывать, что схожие признаки обнаруживаются при других инфекциях [35]. Наиболее полно изменения на компьютерных томограммах были изучены у пациентов, находящихся в состоянии нейтропении после трансплантации костного мозга. Как правило, изменения на томограммах предшествуют таковым на рентгеновских снимках, поэтому компьютерная томография (КГ) должна включаться в диагностический поиск при подозрении на инвазивный аспергиллез. При этом спиральная КГ и КГ с высоким разрешением имеют преимущество перед обычной компьютерной томографией. Бронхоальвеолярный лаваж с цитологическим и бактериологическим исследованиями и/или определением антигена является высокоспецифичным методом исследования с высокой диагностической ценностью в отношении инвазивного аспергиллеза у иммунокомпрометированных больных [36, 37] (BII). Трансбронхиальная или щеточная биопсии часто дают ложноотрицательные результаты (СIII). Если имеются эндобронхиальные очаги, может оказаться полезной их биопсия.
Терапия
Врачи не всегда располагают убедительными доказательствами инвазивного аспергиллеза легких. Несмотря на это приходиться назначать лечение, основываясь только на предположении о данном заболевании, особенно у тяжелых больных и у пациентов с иммунологическими нарушениями. Необходимы исследования по определению диагностического алгоритма в случае, если эмпирическая терапия уже начата.
Оптимальная длительность терапии не определена. Она зависит от распространенности процесса, ответа не лечение, наличия фоновых заболеваний и иммунного статуса. Можно считать разумным продолжение терапии с целью полной эрадикации возбудителя после исчезновения клинических и рентгенологических проявлений, отрицательных бактериологических посевов и уменьшения обратимых предрасполагающих состояний (BIII). Длительность лечения диктуется клиническим ответом, а не предполагаемой кумулятивной дозой. Лечение следует продолжать на фоне химиотерапии. У больных, перенесших грибковую инфекцию, даже при кажущемся отсутствии ее симптомов рационально возобновление противогрибкового лечения на период химиотерапии. Ответ на проводимые меры у таких больных во многом зависит от таких факторов как наличие нейтропении, функции нейтрофилов, выраженность иммуносупрессии, функционирование трансплантата, а также от распространенности аспергиллеза до начала лечения.
Предпочтение следует отдавать внутривенному пути введения, по крайней мере, вначале и у тяжелых больных, так как при этом обеспечено полное поступление препарата в организм (BIII). Амфотерицин В 2 является стандартом в лечении инвазивного аспергиллеза, особенно в тяжелых и жизнеугрожающих случаях. Общий ответ на терапию составляет 37% (от 14% до 83%) [51]. (Данные варьируют в зависимости от фонового заболевания, объема поражения, наличия нейтропении или иммунодефицита, определения понятия «ответ на терапию», продолжительности наблюдения и других факторов). Как показано в корреляционном анализе при исследовании других грибковых заболеваний [52] более благоприятный исход наблюдается при наличии чувствительности возбудителя к препаратам in vitro. Жировые производные амфотерицина fi показаны при развитии у больных инвазивным аспергиллезом нефротоксичности при применении обычного амфотерицина 7 (AII). Они также могут использоваться в начале лечения при нарушенных почечных функциях или одновременном приеме других нефротоксических препаратов. Предыдущие исследования жировых производных амфотерицина были открытыми или в них использовался исторический контроль. Пока еще нет окончательных результатов рандомизированных проспективных исследований, касающихся сравнения эффективности и режимов дозирования амфотерицина В и его жировых производных при инвазивном аспергиллезе. Опыты на животных показали, что для достижения одинакового терапевтического эффекта доза последних должна быть выше, чем доза деоксихолата амфотерицина В. Однако имеется исследование, в котором эти результаты ставятся под сомнение [53].
Применение итраконазола в терапии инвазивного аспергиллеза изучалось в двух исследованиях [13, 14]. Полный ответ и значительное улучшение наблюдался в 39% и 63% случаев соответственно. Эти данные сопоставимы с результатами более ранних наблюдений 18. Частота рецидивов заболевания может быть выше у иммунокомпрометированных пациентов [13]. Пероральная форма является альтернативой амфотерицину у пациентов, которые тщательно соблюдают медицинские рекомендации, одновременно не принимают медикаменты, взаимодействующие с итраконазолом, и у которых не нарушено всасывание препарата из ЖКТ. Логичным представляется использование внутривенного амфотерицина В на начальном этапе лечения и, по крайней мере, до того, как удастся остановить прогрессирование, с последующим переходом на пероральный прием итраконазола (СIII).
Комбинированное применение амфотерицина В с азольными соединениями, флюцитозином и рифампицином имеет преимущество при исследовании in vitro и на животных моделях, хотя была показана возможность их антагонистического взаимодействия [55, 56]. Сообщалось об определенном успехе использования данных комбинаций в отдельных случаях, однако их роль и эффективность в терапии инвазивного аспергиллеза окончательно не определены. К тому же флюцитозин может усугублять миелосупрессию у пациентов с нейтропенией. Поддержание нетоксичного уровня этого препарата в крови при одновременном использовании амфотерицина В затруднен, так как последний может нарушать выделительную функцию почек и, тем самым, тормозить экскрецию флюцитозина. Рифампицин, являясь индуктором печеночных ферментов, может значительно влиять на фармакокинетику других препаратов, особенно у пациентов после трансплантации костного мозга, которые получают глюкокортикоиды, циклоспорин или такролимус. Это свойство рифампицина также исключает возможность использования итраконазола [193].
В некоторых случаях инвазивного аспергиллеза легких с успехом применяется хирургическое иссечение очага [57]. Некоторые клиницисты подчеркивают необходимость как можно более раннего хирургического вмешательства при центрально расположенном очаге (вблизи средостения), так как при этом существует опасность массивного легочного кровотечения [58]. В настоящее время изучаются дополнительные возможности профилактики и лечении инвазивного аспергиллеза при нейтропении или у иммунокомпрометированных пациентов [59]. Изучается эффективность трансфузий гранулоцитов [60, 61], применения колониестимулирующих факторов (гранулоцитарный колоние-стимулирующий фактор, макрофагальный колониестимулирующий фактор, гранулоцитарно-макрофагальный колониестимулирующий фактор) 63, интерферона у [66]. На настоящий момент нет рекомендаций по рутинному использованию данных методов (СIII), так как не доказано увеличение выживаемости при их использовании.
Терапевтические подходы при других инвазивных и неинвазивных локализациях аспергиллеза
Аспергиллезная инфекция с локализацией вне легких встречается реже. Проспективные клинические исследования, посвященные результатам ее лечения, отсутствуют за исключением небольших наблюдений. В этой связи, представленные здесь рекомендации по лечению основаны на отдельных сообщениях или данных, касающихся легочного аспергиллеза.
Аспергиллез придаточных пазух носа
Хронический субклинический инвазивный аспергиллез придаточных пазух носа наблюдается у иммунокомпетентных пациентов в регионах с высоким содержанием грибковых спор в окружающей среде, например, в Судане, Саудовской Аравии, других тропических и пустынных областях, а также у больных сахарным диабетом независимо от региона. В данных случаях наиболее частым возбудителем является A. flavus, тогда как у иммунокомпрометированных пациентов чаще выделяется A. fumigatus. Этот вид аспергиллеза протекает длительно (до нескольких лет), имеет прогрессирующий характер с тенденцией к распространению на близлежащие ткани: решетчатый синус, глазницу, с последующим развитием остеомиелита костей черепа и внутричерепных структур 74. Также как при остром инвазивном аспергиллезе у иммунокомпетентных больных в большинстве случаев помогает хирургическая санация и дренирование [75] (BIII). Роль противогрибковой терапии здесь вторична (СIII). Следует, однако, отметить, что нередко возникают рецидивы заболевания.
Иногда аспергиллез придаточных пазух проявляется в виде шаровидного грибкового образования или мицетомы, которые не проявляют признаков инвазии и ограничиваются единственной пазухой в течение месяцев или лет. Лечение включает в себя хирургическое удаление грибкового образования с целью обеспечить дренаж пазухи. Роль системной противогрибковой терапии в этом случае не определена. Прогноз заболевания очень хороший.
Аспергиллез гортани, трахеи и бронхов
Имеются сообщения о возникновении аспергиллеза гортани, трахеи и бронхов у пациентов с нарушениями иммунитета при лимфопролиферативных заболеваниях, СПИДе, трансплантации солидных органов, длительной терапии кортикостероидами 79. Локализованная аспергиллезная инфекция, ограниченная местом анастомоза, была описана у некоторых пациентов после трансплантации сердца и легких [84]. У больных СПИДом с лихорадкой, кашлем и отдышкой встречаются очаги грибкового поражения в виде язв и налетов [79]. Эпиглотит аспергиллезной этиологии встречается крайне редко [85].
Во всех этих случаях основой лечения является системная противогрибковая терапия. В качестве дополнительной терапии может применяться амфотерицинВ в виде ингаляций, однако эффективность данного метода не доказана [86]. Сообщалось о нескольких случаях аспергиллеза гортани, в которых успешно применялись хирургические методы (выскабливание или удаление очага) в дополнение к системной противогрибковой терапии. При возникновении некротизирующего аспергиллеза бронхов с наличием грибковых масс в трахее может оказаться необходимым удаление с помощью бронхоскопии, так как противогрибковые препараты слабо проникают в их толщу.
Аспергиллез уха
Описаны как инвазивный, так и неинвазивный (сапрофитный) аспергиллез уха. Аспергиллы могут колонизировать серные пробки в наружном слуховом проходе без развития инфекции. Однако у больных СПИДом и острым лейкозом может наблюдаться инвазивный аспергиллез наружного слухового прохода [4, 80, 81, 87, 88]. Аспергиллезный отит может сопровождаться аспергиллезным мастоидитом.
Системная противогрибковая терапия необходима у иммунокомпрометированных пациентов [89] (Bill). В более легких случаях (без инвазии тканей), а также у пациентов без иммунных нарушений возможно проведение местной терапии, включая удаление серных образований (BIII). Препараты для местного лечения включают крезилат, медицинский спирт, нистатин (мазь или порошок), амфотерицин В 3% раствор для наружного применения, борная кислота, тимол, генциан виолет, йодохлоргидроксиквин (порошок, лосьон), 5-фторцитозин (мазь), нитрофунгин, клотримазол и кетоконазол [90]. Обычно требуется длительная терапия.
Аспергиллез глаза
Существует несколько механизмов развития аспергиллезного эндофтальмита: прямая инокуляция возбудителя при травме, вследствие хирургических вмешательств, таких как удаление катаракты, гематогенное распространение, наиболее часто встречающееся у иммунокомпрометированных пациентов, наркоманов и больных аспергиллезным эндокардитом [91]. В этих случаях диагноз подтверждается исследованием мазков и бактериологическими посевами стекловидного тела и внутриглазной жидкости. Системное лечение амфотерицином В и итраконазолом обычно неэффективно вследствие слабого проникновения этих препаратов в стекловидное тело и жидкие среды глаза [90]. Поэтому амфотерицин В (доза 10 мкг) применяется в виде инъекций в стекловидное тело (B), обычно после pars plana витрэктомии. Уровень флюцитозина составляет 20-30% от уровня этого препарата в крови; имеется небольшой опыт его применения при глазных инфекциях. Витрэктомия с орошением амфотерицином В или введением его внутрь стекловидного тела может оказаться необходимым для диагностики и лечения заболевания 95 (BIII).
Другие проявления аспергиллезной инфекции глаза встречаются реже. Абсцессы склеры лечатся хирургически с местным назначением амфотерицина В [96, 97]. До конца не ясна необходимость в этих случаях системной противогрибковой терапии. При поражении роговицы применяются различные методы, включая наложение «оллагеновых пленок, импрегнированных 0,5% амфотерицином В, 0,15%-1% раствор амфотерицина В в виде глазных капель, глазные ванночки с амфотерицином В, местное применение 1% клотримазола 5% пимарицина, 1% миконазола или 2% кетоконазола 98. Пероральный итраконазол также может быть полезен в случае поверхностного поражения, так как он проникает в глубокие слои роговицы [101]. Хирургическое вмешательство может потребоваться в случае прогрессирования заболевания, несмотря на медикаментозное лечение или при угрозе перфорации. Хирургические методы включают выскабливание, пластинчатую кератотомию, формирование конъюнктивальной складки над участком изъязвления (с целью предохранения разрыва глаза), подсадку роговицы. При возникновении злокачественной глаукомы для восстановления оттока внутриглазной жидкости необходимо проведение иридэктомии, удаление хрусталика или передняя витрэктомия [102].
Аспергиллез ЦНС
Аспергиллез ЦНС может проявляться единичными или множественными абсцессами головного мозга, менингитом, эпидуральным абсцессом или субарахноидальным кровотечением [103]. По литературным данным смертность при этом заболевании превышает 90% [4].
Аспергиллезный менингит встречается редко. Имеются сообщения о случаях менингита у наркоманов, больных диабетом, туберкулезом, при нейтропении или у пациентов, находящихся на длительной терапии кортикостероидами. Заболевание может быть следствием распространение аспергиллеза околоносовых пазух, осложнением интратекального введения антибиотиков или хирургического вмешательства на клиновидной кости [112]. Иногда причину аспергиллезного менингита выявить не удается. В ходе лечения можно проводить повторные определения аспергиллезного антигена в спинномозговой жидкости [113]. Амфотерицин В [4], итраконазол [114] и вориконазол [113] для лечения менингита используются системно и интратекально (например, через резервуар Оммайя). В некоторых случаях может потребоваться удаление пораженных тканей [115].
Эпидуральные абсцессы аспергиллезной этиологии как правило вторичны и являются распространением инфекции по протяжению, например, при поражении тел позвонков. Для лечения эпидуральных абсцессов применяется хирургическое дренирование и системная терапия (BIII).
Аспергиллез костей
Аспергиллез кожи
Аспергиллез кожи обычно возникает у пациентов со значительными иммунными нарушениями вследствие диссеминации возбудителя из первичного очага, как правило, легких. Отсевы могут быть как единичными, так и множественными, обычно безболезненны, чаще локализуются на конечностях. Первоначально они выглядят как эритематозные папулы, которые затем превращаются в пустулы с развитием изъязвления с приподнятыми краями и черной корочкой [128,129]. Хотя последнее характерно для аспергиллезного поражения кожи, данные элементы не являются патогномоничными и для исключения других возбудителей, вызывающих сходную картину, требуется биопсия с бактериологическим исследованием биоптата (АIII). Наиболее частыми возбудителями аспергиллеза кожи являются A. fumigatus, A. flavus и A. terreus. Имеются сообщения, что Aspergillus chevalieri вызывает поражение кожи в виде эритематозных, гиперкератозных и везикулопапулезных элементов [130].
Биопсия кожных очагов инфекции крайне важна для постановки правильного диагноза. Основным в лечении является применение, как правило, успешное, системной противогрибковой терапии (BIII). В случае неконтролируемой местной инфекции при нейтропении может потребоваться хирургическое лечение [131]. Если инфекция локализуется в месте постановки венозного катетера, необходимо его удаление [129]. Аспергиллез ожоговых ран и посттравматическая инфекция мягких тканей лучше всего поддаются лечению хирургическими методами в сочетании с системной противогрибковой терапией. В терапии онихомикозов используется пероральный итраконазол с или без местного применения 8% циклопирокса в виде лака для ногтей [15, 132, 133].
Эндокардит, перикардит и миокардит аспергиллезной этиологии
Имеются сообщения о первичных и вторичных клапанных эндокардитах аспергиллезной этиологии [94], которые иногда являются признаком диссеминированного аспергиллеза. Возбудитель редко высевается из крови [30]. При этом заболевании на клапанах часто возникают массивные, но хрупкие вегетации, которые могут становиться причиной эмболических осложнений. Плохое проникновение амфотерицина В в клапанные вегетации и высокий риск эмболии диктуют необходимость раннего хирургического вмешательства с протезированием клапанов, особенно при вторичном клапанном эндокардите [94, 134]. Оправдано назначение амфотерицина в периоперационном период. В отдельных случаях может с успехом применяться комбинация амфотерицина В и флюцитозина без хирургического лечения [135].
Перикардит является редким осложнением диссеминированного аспергиллеза 136. Он может быть следствием гематогенного распространения возбудителя, вскрытия абсцесса миокарда или переходом инфекции со стороны легких. Клинически перикардит проявляется в виде загрудинных болей, одышки или аритмией. В диагностике может оказаться полезным определение антигена в перикардиальной жидкости. У трети больных перикардит осложняется тампонадой сердца. Также описаны случаи констриктивного перикардита и пневмоперикарда. Лечение состоит из системной противогрибковой терапии (СIII) и дренажа полости перикарда, включая, по возможности, перикардэктомию [4]. Миокардит встречается как изолированно, так и вместе с перикардитом 141.
Аспергиллез мочеполового тракта
Аспергиллезная инфекция мочеполового тракта обычно возникает вследствие гематогенного распространения. Вовлечение почечной паренхимы характерно для иммунокомпрометированных пациентов, например, при лейкозе или хроническом гранулематозе, а также для наркоманов. Больные сахарным диабетом и наркоманы имеют повышенный риск инфекции с поражением почечной лоханки. Образование грибкового шара наблюдается при некрозе почечных сосочков, а также может встречаться при абсцессе простаты [144]. При аспергиллезе паренхиматозных органов применяется системная противогрибковая терапия. Для лечения абсцессов и грибковых шаров показано хирургическое удаление. Терапия может быть малоэффективной из-за низкой концентрации итраконазола и полиенов в моче. При инфекция почек, уретры и простаты системно используется амфотерицин В или его липосомальные производные [145]. Применение флюцитозина также может оказаться эффективным из-за его способности достигать высокой концентрации в моче. Местное орошение амфотерицином В используется при инфекции мочевого пузыря и почечной лоханки.
Внутрибрюшной аспергиллез
Аспергиллезный перитонит возникает как осложнение хронического перитонеального диализа 147. Для эрадикации возбудителя необходимо удаление диализного катетера [4]. Проводиться противогрибковая терапия с использованием амфотерицина В и итраконазола внутрибрюшинно и системно [90,146].
Поражение аспергиллой висцеральных органов наиболее часто наблюдается при диссеминации инфекции. Среди органов желудочно-кишечного тракта пищевод вовлекается чаще, чем толстый и тонкий кишечник [4, 104]. Изъязвления в пораженных органах могут стать причиной некрозов и перфораций [149]. Несмотря на проведение системной терапии, исход заболевания плохой.
Аспергиллез лимфатических узлов
Аспергиллы могут вызывать первичную гранулематозную инфекцию лимфоузлов [150]. В случае неудовлетворительного ответа на системную противогрибковую терапию для эрадикации возбудителя показано хирургическое удаление пораженного узла.
Аспергиллема легких
Аспергиллема легких определяется как находящийся в полости легкого или бронхоэктазе конгломерат переплетенных аспергиллезных гиф, покрытый фибрином, слизью и клеточными элементами [151]. Обычно больной имеет фоновое заболевание (фиброкистозный саркоидоз, кавернозный туберкулез, гистоплазмоз, буллезную эмфизему или фиброз легких) [152]. Диагноз аспергиллемы обычно ставится клинически без проведения биопсии легких. Рентгенографические признаки имеют огромное значение в постановке предварительного диагноза. На снимке аспергиллема легких выглядит как круглое образование, иногда подвижное, расположенное внутри сферической или овальной капсулы и отделенное от стенки этой капсулы воздушной прослойкой различной формы и размера. По интенсивности затемнения при рентгенографии аспергиллема соответствует жидкости [153]. При периферическом расположении характерно утолщение плевры. Диагноз обычно ставится при наличии вышеописанных рентгенологических признаков и положительной реакции преципитации (при аспергиллеме это исследование обладает >95% чувствительностью) [153, 154]. Следует помнить, что пациенты, получающие кортикостероиды могут быть серонегативны.
Несмотря на то, что аспергиллема часто рассматривается как доброкачественная сапрофитная колонизация, при аспергиллезе легких трудно провести границу между колонизацией и инвазией тканей 151. Инвазивный аспергиллез легких может развиваться из аспергиллемы [155] и при этом часто бывает фатальным. Описана хроническая некротизирующая форма аспергиллезной инфекции [156] с развитием общих симптомов (лихорадка, потеря веса и др.), присутствием аспергиллемы на рентгенограмме и признаками инвазии ткани легкого при исследовании биоптата.
Общепризнанным методом лечения является хирургическое удаление аспергиллемы [152]. Однако это может сопровождаться серьезными, вплоть до летального исхода, осложнениями 162. Из-за высокой васкуляризации тканей резекция легкого опасна. К тому же возможно постоперационное развитие аспергиллезной инфекции в образованной полости. Смертность от операции превышает 7% [167]. Нередки серьезные послеоперационные осложнения, такие как формирование бронхоплеврального свища и кровотечение. Аспергиллема чаще развивается у пациентов с неблагоприятным преморбидным фоном и нарушенными легочными функциями, что еще больше повышает риск хирургической операции [167]. У многих больных приходиться отказываться от выполнения резекции вследствие неудовлетворительных показателей функций легких. Таким образом, хирургическое удаление аспергиллемы, по-видимому, должно проводиться только у пациентов с массивным легочным кровохарканьем и адекватными легочными функциями [167], а также рассматриваться в качестве возможного метода лечения при саркоидозе, у иммунокомпрометированных больных и при повышении титра специфических аспергиллезных IgG (CIII). Непредсказуемое течение заболевания делает принятие решения об операции особенно трудным.
Эмболизация бронхиальных артерий (ЭБА) у пациентов с кровохарканьем применяется для окклюзии кровоточащих сосудов [168]. Иногда производят эмболизацию Других сосудов, поддерживающих кровотечение. К сожалению, эта процедура обычно не приносит успеха или оказывает лишь временный эффект. После ее проведения пациент должен лежать неподвижно в течение 3-4 часов. Вследствие коллатерального кровообращения кровотечение часто возобновляется; повторные эмболизации, как правило, безуспешны [169, 170]. Таким образом, ЭБА может рассматриваться как временная мера при жизнеугрожающем кровотечении у пациентов, которые подлежат более эффективной терапии после стабилизации состояния (BIII).
Дополнительные методы лечения аспергиллемы включают лучевую терапию [171], внутриполостное или эндобронхиальное введение [167, 172-174] и мелкодисперсную ингаляцию противогрибковых средств [167], и системную противогрибковую терапию [17, 18, 175-178]. Такие симптомы как лихорадка и кашель могут быть частично обусловлены сопутствующей инфекцией, вызванной другим возбудителем, или проявлением аллергии. Уменьшение симптоматики наблюдалось у больных с признаками аллергии (эозинофилия, повышение уровня IgE, положительный скарификационный тест на аспергиллу и др.), которым проводилась системная терапия кортикостероидами [179]; однако следует учитывать то, что такая терапия увеличивает риск грибковой инвазии и диссеминации [154], и/или усугубляет течение нераспознанной сопутствующей инфекции. Некоторые из исследований заслуживают отдельного комментария. Внутривенное введение амфотерицина В не более эффективно, чем рутинный бронхиальный лаваж [175]. Особенно впечатляющими были результаты одного исследования [173], в котором для лечения аспергиллемы использовались внутриполостные и эндобронхиальные инстилляции амфотерицина В: у 12 из 14 пациентов наблюдалось разрешение заболевания или клиническое улучшение. Этот метод трудновыполним у больных с нарушенными дыхательными функциями. Об использовании итраконазола сообщалось в ряде исследований [17, 18, 176-178]. Эти исследования были по большей части ретроспективными, не слепыми и неконтролируемыми. Дозировка и продолжительность терапии итраконазолом не стандартизированы. Тем не менее, результаты исследований говорят об эффективности итраконазола в лечении аспергиллемы (BIII).
АБЛА
В Соединенных Штатах АБЛА наблюдается у 7-14% больных бронхиальной астмой, постоянно получающих лечение кортикостероидами [182]. У многих пациентов с муковисцидозом отмечается колонизация дыхательных путей аспергиллами и примерно у 7% этих больных развивается АБЛА [183]; к тому же у них имеется повышенный риск развития инвазивного аспергиллеза после трансплантации легких.
Типичным рентгенологическим признаком АБЛА являются непостоянные одно- или двухсторонние участки уплотнения в легких, преимущественно в верхних отделах [184]. Данная картина обусловлена обструкцией бронхов слизистыми пробками. Бронх, заполненный слизью, на рентгенограмме дает затемнение в виде ленты или пальца перчатки [182]. Такие тени характерны для заболевания; они могут меняться после откашливания слизистой пробки. Также на снимках могут наблюдаться кольцевидные или параллельные тени («трамвайные рельсы»), которые представляют собой воспаленные бронхи. Диагноз АБЛА должен предполагаться у всех пациентов с гормонозависимой бронхиальной астмой или при сочетании бронхиальной астмы с вышеописанными рентгенологическими признаками.
АБЛА может прогрессировать, проходя стадии гормононезависимой и гормонозависимой бронхиальной астмы, в конечную стадию фиброза легких (сотовые легкие) [185]. Терапия при АБЛА направлена на предупреждение астматических приступов и развития конечной стадии фиброза легких.
Хотя краеугольным камнем в лечении АБЛА являются кортикостероиды, имеется немного данных, касающихся их использования. Все немногие исследования выполнялись на небольших группах пациентов, не были двойными слепыми, контролируемыми. Доза кортикостероидов в них была различной. Несмотря на эти методологические проблемы, имеющиеся данные однозначно подтверждают необходимость применения кортикостероидов в терапии АБЛА (АН). Rosenberg et а1. [186] наблюдал 22 пациентов с АБЛА, которые в течение недели принимали преднизолон по 0,5 мг/кг/сут, затем по 0,5мг/кг через день. После шести недель лечения была предпринята попытка отменить преднизолон. При такой схеме терапии отмечалась быстрое уменьшение отдышки, хрипов и кашля. При снижении дозы преднизолона у большинства пациентов появились симптомы легкой бронхиальной астмы, которая в большинстве случаев контролировалась применением ингаляционных бронходилятаторов и/или кортикостероидов. Уровни IgE в крови коррелировали с активностью заболевания, понижаясь при клиническом ответе на гормональную терапию и повышаясь перед обострением процесса.
Все немногочисленные исследования, посвященные лечению кортикостероидами хронического АБЛА, были ретроспективными. Safirstein et а1. [187] в течение пяти лет наблюдал пациентов с АБЛА и выяснил, что у не леченных больных хроническое течение характеризовалось обструкцией дыхательных путей, повторными легочными инфильтратами с эозинофилией и, во многих случаях, выраженной деструкцией легких. Наличие симптомов не всегда может служить прогностическим признаком. Так у некоторых асимптоматических пациентов развивались эозинофилия и легочные инфильтраты с исходом в легочную деструкцию. Ежедневная доза преднизолона выше 7,5 мг/сут ассоциировалась с меньшим количеством повторных инфильтратов. Middleton et а1. [188] описал 65 больных с «астматической легочной эозинофилией», 32 из которых имели АБЛА. У пациентов, получавших постоянную гормональную терапию, развивалось меньшее количество рентгенологических изменений по сравнению с пациентами, получавших кортикостероиды непостоянно. В этом исследовании была подобрана доза преднизолона в 10 мг/сут, которая необходима для предотвращения повторного возникновения инфильтратов на неопределенный период. Capewell et а1. [189] более 14 лет изучал клиническое течение АБЛА у 33 пациентов. 28 (85%) из этих пациентов длительно лечились преднизоном в среднесуточной дозе 7,4 мг. За период наблюдения не было отмечено статистически значимых изменений при спирометрии. Обнадеживает то, что время наблюдения не отмечалось ухудшения функции легких. Однако требуется проспективное исследование с целью избежать проблем, возникающих при использовании исторической контрольной группы в ретроспективном исследовании.
Ингаляционные кортикостероиды (беклометазон) не эффективны при АБЛА [185], хотя некоторые врачи не разделяют это мнение [199]. Имеются сообщения о возможной эффективности высоких доз этих препаратов [200]. Вероятно, имеется связь между количеством грибов, содержащихся в воздухе, и обострениями АБЛА [201, 202]. Попытки повлиять на течение заболевания с помощью изменения характеристик окружающей среды не исследованы, и подобный подход остается теоретическим. Гипосенсибилизация и избегание возможных мест скопления грибов успеха не имели.