аримидекс или анастрозол что лучше
Аримидекс или анастрозол что лучше
В большинстве случаев обследования больных с локализованными опухолями врач приходит к выводу, что болезнь носит преимущественно системный характер, и метастазы разовьются позже. Обнаружение многочисленных метастазов, часто спустя годы после проведения мастэктомии, а также в течение многолетнего наблюдения за больными подтверждает этот вывод.
По данным классических исследований Бринкли и Хейбитл, общая выживаемость больных раком молочной железы через 25 лет после лечения составляет только 20%. Даже среди пациенток, которым мастэктомия была сделана своевременно («ранние» операбельные случаи), выживаемость составляет лишь 30%.
Обычно появление метастазов приводит к смертельному исходу в пределах трех лет, хотя в случаях, когда лечение оказывается эффективным, пациентки могут жить дольше. Вероятность метастазирования опухоли сильно зависит от степени вовлечения подмышечных лимфатических узлов в патологический процесс, что определяется при гистологическом анализе образцов, взятых во время операции.
Существует взаимосвязь между количеством пораженных подмышечных лимфатических узлов и вероятностью распространения метастазов.
Со времени проведения первой операции терапевтической овариэктомии, проведенной Битсоном в 1896 г., стало очевидно, что при изменении гормонального статуса организма в случаях распространенного опухолевого процесса, по крайней мере для одной трети пациенток достигается симптоматический эффект.
Использовались различные методы: удаление яичников или их облучение (иногда называемое «создание искусственной менопаузы»), лечение эстрогенами, антиэстрогенами и антагонистами гонадотропин-рилизинг-гормона (например, гозерелином). Этот гормон регулирует секрецию лютеинизирующего гормона (LHRH).
Также применяли анаболические стероиды, глюкокортикоиды и прогестерон, проводили удаление надпочечников или гипофиза и назначали ингибиторы ароматазы (анастрозол или летрозол).
Стандартный подход основан на менструальном статусе пациентки. Для большинства больных с метастазирующими опухолями в пременопаузе и перименопаузе используется хирургическое удаление яичников или их облучение. Однако с появлением антагонистов гонадотропин-рилизинг-гормона эти процедуры стали применять реже.
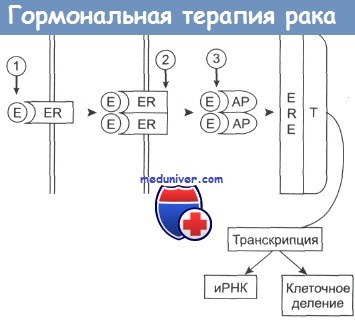
Комплекс приобретает активность (АР) и присоединяется к эстроген-зависимым структурам (ERE) клеточного ядра.
Происходит активация таких белков, участвующих в транскрипции (Т), как РНК-полимераза II, что приводит к синтезу белка и делению клетки.
Гозерелин вызывает снижение уровня эстрогенов в плазме крови (1); фульвестран (2) предотвращает процесс димеризации рецептора и его активацию; тамоксифен (3) связывается с активным комплексом, подавляя его способность инициировать транскрипцию.
Антагонисты обеспечивают стойкое снижение уровня эстрогенов и вызывают у пациентки состояние менопаузы, которое длится в продолжении примерно двух месяцев с начала применения гозерелина. Препарат назначается ежемесячно в виде внутримышечных инъекций. Вместе с тем в качестве альтернативы снова стал популярным такой хирургический метод, как лапароскопическое удаление яичников.
Это достаточно безопасная и несложная операция, после которой пациентка на одну ночь остается в стационаре. Следует отметить, что перед операцией больные проходят тщательный отбор по критерию гормональной чувствительности опухоли, и тем, для кого не предполагается проявление лечебного эффекта, операция не проводится.
Для пациенток с опухолью в постменопаузе широко применяется тамоксифен, поскольку он практически не проявляет побочных эффектов. Препарат действует как антиэстроген, но, вероятно, оказывает и прямой цитотоксический эффект. В течение почти 20 лет тамоксифен использовался в качестве стандартного препарата адъювантной терапии.
Тамоксифен назначается перорально в ежедневной стандартной дозе 20 мг. Он обладает медленным кумулятивным действием. Побочные эффекты редки, однако могут наблюдаться приливы, тошнота, гиперкальциемия, тромбоцитопения, удержание жидкости и расстройство менструального цикла. После приема препарата большинство пациенток прибавляют 1-2 фунта в весе и некоторые отмечают ухудшение состояния кожи, волос и ногтей.
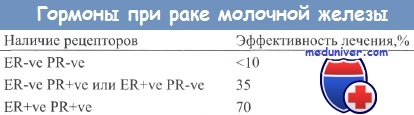
Гораздо более существенный эффект получен при назначении гормонотерапии пациенткам с гормонально зависимыми опухолями, в то время как при лечении гормонально независимых опухолей благоприятный эффект наблюдался лишь в редких случаях. Прогноз в случаях гормонально зависимых и независимых опухолей отличается. Для больных с гормонально-зависимыми опухолями характерен более длительный безрецидивный период и большая выживаемость.
Совместное определение показателей ER и PR обеспечивает более точный прогноз в отношении чувствительности опухоли к гормонотерапии, чем это оказывается возможным при оперировании только показателем ER. Больные с PR-положительными опухолями также характеризуются более длительным безболезненным периодом.
На эффективность гормонотерапии сильно влияет характер распространения метастазов. Костные метастазы проявляют некоторую чувствительность к гормонам, хотя после лечения пациентки живут в среднем около 12-15 месяцев. Тем не менее некоторые больные с гормоночувствительными опухолями и с костными метастазами живут дольше, иногда несколько лет.
В большинстве случаев, при рецидиве опухоли, развившейся в пременопаузе, применяется гозерин (или его аналоги) или лапароскопическая овариэктомия (или облучение яичников). Эти меры эффективны для гормонально чувствительных опухолей. При опухолях в периоде постменопаузы обычно назначают тамоксифен, если пациентки раньше не получали этот препарат в качестве средства адъювантной терапии.
В любом случае можно ожидать, что выживаемость больных составит по крайней мере 30%. Экзогенные гормоны назначают до тех пор, пока не наступит эффект. В дальнейшем гормональную терапию продолжают только тем пациенткам, у которых проявился эффект первичного лечения. Предложены новые противоопухолевые препараты, относящиеся к группе ингибиторов ароматазы.
К числу их относится анастрозол, который блокирует биосинтез предшественников эстрогенов и их последующие превращения в тканях. Анастрозол действует при пероральном применении. Он хорошо переносится больными, так же как и другие родственные соединения, благодаря чему эти препараты быстро заняли место тамоксифена, который оказался неэффективным в лечении пациенток с гормонозависимыми опухолями, развивающимися в период постменопаузы. Рекомендуемая ежедневная доза препарата составляет 1 мг.
Если после первичного лечения возникает рецидив, то назначают другие препараты, например анаболические стероиды, прогестогены и глюкокортикоиды. Анаболические стероиды более эффективны у пациенток с опухолями, развившимися в постменопаузе, и, по-видимому, их особенно необходимо применять в случаях обнаружения костных метастазов.
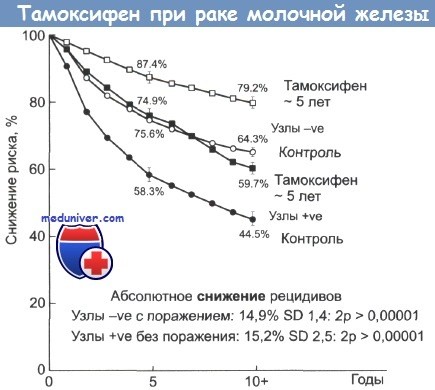
Светлые значки — пациентки без признаков поражения лимфатических узлов; затемненные значки — пациентки с признаками поражения лимфоузлов.
Благоприятный эффект достигается примерно у 20% пациенток, однако недостатком применения стероидов является вирилизация. Удобным для применения является нандролон деканоат (Deca-Durabolin), который назначается в виде внутримышечных инъекций в дозе 50-100 мг каждые 3-4 недели. Если гормонотерапия раньше давала положительные результаты, то можно применять прогестогены. Наиболее часто используется ацетат медроксипрогестерона (МРА, Provera), который обычно назначают перорально в дозе 100 мг три раза в день.
Однако его применение ограничено из-за развития побочного эффекта — прибавления в весе. Такой же эффективностью обладает другое производное прогестерона — мегестрол-ацетат (Megace).
Широко обсуждается вопрос выбора метода лечения первого рецидива опухоли. Следует в этом случае использовать гормональный метод или же химиотерапию с использованием цитотостатиков? Если принимать во внимание количественные показатели, то выбирать надо между гормонотерапией (эффективна в 30% случаев) и комбинационной химиотерапией (эффективность которой в два раза выше). Однако это упрощенное решение вопроса, ответить на который на самом деле сложно.
Реакция опухоли на гормоны обычно носит более продолжительный характер, и у пациентки наблюдаются минимальные токсические проявления. При химиотерапии развивается более кратковременный эффект, который сопровождается токсическими и психологическими осложнениями. Большинство клиницистов в Великобритании в качестве средства первичного лечения предпочитают использовать гормональную терапию. Выбор облегчается все более широким применением метода анализа состояния рецепторов эстрогенов: гормональная терапия должна проводиться только среди пациенток с ER-положительными опухолями. Недавно предложен препарат фульвестрант (Faslodex), подавляющий функции рецепторов эстрогенов. Он может применяться у пациенток с гормоноустойчивыми опухолями, которые развились в постменопаузе. Одним из основных преимуществ этого препарата, по сравнению с агонистом эстрогенов, тамоксифеном, является отсутствие побочных эффектов. Он также не опустошает пул эстрогенов в женском организме, что происходит при применении ингибиторов ароматазы.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Гормонотерапия рака молочной железы
Гормонозависимый рак
Гормонотерапия при раке
Гормоночувствительность
Подробнее о принципах лечения рака молочной железы смотрите ЗДЕСЬ (для специалистов)
Гормонотерапия при раке
Oncotype DX
Endopredict (Эндопредикт)
Эстрогеновые рецепторы
Эстрогеновые рецепторы обозначаются ER.
Рецепторы прогестерона
Прогестиновые рецепторы обозначаются PR. Они тоже находятся на оболочках клеток. С ними взаимодействует прогестерон, стимулируя клетки к делению.
Гормональная терапия
Гозерелин
Удаление яичников
Лучевая кастрация тоже представляет собой исторический интерес.
Когда начинать гормонотерапию
Где купить препараты для гормонотерапии смотрите ЗДЕСЬ
Никто не собирается гормонотерапией делать из женщины мужчину. Борода и усы у Вас не вырастут, голос не изменится.
Как переносится гормонотерапия
Гормонотерапия по сравнению с химиотерапией переносится совершенно иначе. Неприятные ощущения могут возникать в период адаптации в начале лечения (1 мес), но совсем не обязательно. При гормонотерапии нет проявлений токсичности (тошнота, рвота, кишечные расстройства). Она не требует контроля анализов крови.
Тамоксифен
Тамоксифен противопоказан при глаукоме. Обязательно скажите своему врачу, если она у Вас есть.
При сопутствующей сердечной патологии частота и степень её усугубления на фоне приёма Тамоксифена была ниже, чем на фоне приёма ингибиторов ароматазы.
Анализ на Циклин Д1 можно сдать в лаборатории, тел.8 (812) 439-95-28.
Торемифен
Ингибиторы ароматазы
При Her2/neu позитивных (Her2/neu3+) и гормонопозитивных (ER+ и PR+) опухолях Тамоксифен не показал должной эффективности, по сравнению с ингибиторами ароматазы.
Анастрозол иногда провоцирует обострения ревматоидного артрита. Смена его на Фемару (Летрозол) нивелирует этот побочный эффект. Анастрозол и Фемара провоцируют остеопороз и требуют параллельного назначения препаратов кальция и витамина Д (например, КальцийД3 компании Никомед), равно как и ежегодной контрольной остеосцинтиграфии.
Прогнозы при раке молочной железы СМОТРИТЕ ЗДЕСЬ
Гормонотерапия рака молочной железы
Гормонотерапия рака груди
Для проведения гормонотерапии есть оригинальные препараты и дженерики. Стоимость оригинальных препаратов не всегда неподъёмна. Информация об аптеках, легально продающих препараты для гормонотерапии находится ЗДЕСЬ.
| Мы стараемся обеспечить всем нашим пациентам консультацию грамотного химиотерапевта, мотивированного при назначении гормонотерапии только потребностями пациента, а не другими причинами. |
Дополнительно о гормонотерапии Вы можете прочитать ЗДЕСЬ.
Специалисты Университетского Маммологического Центра регулярно повышают свой профессиональный уровень, посещают отечественные и зарубежные конференции, чтобы быть в курсе всех современных тенденций в онкологии и пластической хирургии.
Автор: Чиж Игорь Александрович
заведующий, кмн, онколог высшей квалификационной категории,
хирург высшей квалификационной категории, пластический хирург
Запишитесь на консультацию по телефону: 8 (812) 939-18-00 или через форму на сайте
Сравнительная оценка фармацевтического качества препаратов анастрозола
Полный текст:
Аннотация
Ключевые слова
##article.ConflictsofInterestDisclosure##:
##article.articleInfo##:
Депонировано (дата): 05.06.2018
##article.reviewInfo##:
##article.editorialComment##:
Для цитирования:
Белоусов Ю.Б., Соколов А.В., Зырянов С.К., Лелишенцев А.А., Камаев А.В., Зверков Ю.Б. Сравнительная оценка фармацевтического качества препаратов анастрозола. Качественная Клиническая Практика. 2010;(1):16-21.
ВВЕДЕНИЕ
Рак молочной железы (РМЖ) в настоящее время – это наиболее часто диагностируемое онкологическое заболевание у женщин в Европе и США. Предполагается, что за период с 2001 по 2010 год будет выявлено 5 миллионов новых случаев этого заболевания. К сожалению, несмотря на все достижения в диагностике и лечении РМЖ, более 50% пациентов погибают от распространённого РМЖ. Большая часть опухолей молочной железы имеет рецепторы к эстрогенам и, соответственно, рост этих опухолей может быть стимулирован эстрогенами. У женщин в постменопаузе основным источником циркулирующих эстрогенов является андростендион, синтезируемый надпочечниками. В периферических тканях (например, в жировой ткани) при участии фермента ароматазы он превращается в эстрон и в дальнейшем, в эстрадиол [1].
Таким образом, лечение гормонозависимых опухолей молочной железы должно быть направлено на снижение уровня эстрогенов, что может произойти вследствие овариоэктомии у женщин в пременопаузе или использования антиэстрогенных препаратов как в пре-, так и в постменопаузе.
Первые представители класса ингибиторов ароматазы не нашли достаточно широкого применения в медицинской практике вследствие неселективности своего действия и необходимости парентерального введения. Ситуация с использованием препаратов, обладающих сходным механизмом, изменилась с появлением нового нестероидного ингибитора ароматазы анастрозола. Препарат не обладает прогестогенной, андрогенной и эстрогенной активностью. В суточных дозах до 10 мг анастрозол не оказывает влияния на секрецию кортизола и альдостерона, следовательно, при применении анастрозола не требуется заместительного введения кортикостероидов.
Анастрозол применяется при адъювантном лечении ранних стадий эстроген-положительного РМЖ, а также для лечения распространённого РМЖ у женщин в постменопаузе.
В проведённых клинических исследованиях установлено, что эффективность анастрозола прямо коррелирует с принимаемой дозой. Так, в исследовании фармакокинетики, проведённом на здоровых женщинах с сохранённой репродуктивной функцией, показано, что изменение синтеза гормонов гипофиза при применении данного препарата происходит практически линейно при эскалации принимаемой дозы с 5 до 20 мг [2].
Аналогичные зависимости установлены во влиянии приёма препарата на уровень сывороточного эстрадиола у женщин в постменопаузе. Чрезвычайно важным является тот факт, что снижение уровня циркулирующего эстрадиола отмечалось только на 6 день от начала приёма анастрозола. Таким образом, можно полагать, что одним из факторов, обусловливающих эффективность проводимой терапии, является кумулятивная доза препарата.
В исследовании, проведённом с участием 14 женщин в постменопаузе, у которых диагностированы распространённые формы РМЖ с наличием рецепторов к эстрогенам, было установлено, что применение анастрозола сопровождается снижением концентрации эстрогенов и внутри опухоли. Через 15 недель приёма анастрозола оказалось, что внутриопухолевые концентрации эстрадиола, эстрона и эстрона сульфата достигли значений в 11,1, 16,7 и 26,6%, соответственно, от базового уровня. У трёх пациенток уровень перечисленных гормонов был ниже предела детекции [3]. Нельзя не отметить, что анастрозол обладает достаточно благоприятным профилем безопасности. Из неблагоприятных побочных реакций, которые развиваются часто, можно отметить «приливы» жара, артралгию, сухость влагалища. Приём препарата может вызвать снижение минеральной плотности костной ткани в связи со снижением уровня циркулирующего эстрадиола, тем самым, повышая риск возникновения остеопороза и перелома костей.
Учитывая высокую эффективность препарата в лечении РМЖ, становится понятным интерес фармацевтических компаний к производству генерических копий анастрозола. По данным на 10.02.2010 г., в РФ зарегистрированы 1 оригинальный препарат и 3 воспроизведённых препарата анастрозола [4]. Учитывая растущую обеспокоенность пациентов, широкой медицинской общественности, регуляторных органов, связанную с зачастую неудовлетворительной клинической эффективностью при применении генериков, было решено провести выборочный сравнительный фармакохимический анализ лекарственных форм анастрозола различных производителей с целью изучения их фармацевтической эквивалентности.
Для достижения цели были поставлены следующие задачи:
В качестве объектов исследования были избраны лекарственные препараты анастрозола, выпускаемые различными производителями: «Аримидекс» – таблетки, покрытые плёночной оболочкой, №28, содержащие активное вещество анастрозол в количестве 1 мг, производства компании «АстраЗенека Фармасьютикалс ЛП.», США; «Анастера®» – таблетки, покрытые плёночной оболочкой, №28, содержащие активное вещество анастрозол в количестве 1 мг, производства компании «Лаборатория Блипак С.А.», Аргентина; «Веро-Анастрозол®» – таблетки, покрытые плёночной оболочкой, №28, содержащие активное вещество анастрозол в количестве 1 мг, производства компании ОАО «Верофарм», Россия.
Все выбранные образцы были закуплены в розничной аптечной сети в количестве, достаточном для проведения данного исследования в соответствии с требованиями Государственной Фармакопеей (ГФ).
Проведённые исследования выполнены сотрудниками Испытательной лаборатории ООО «Национальное агентство клинической фармакологии и фармации» в полном соответствии с требованиями нормативной документации и требованиями ГФ выпуск XI, с использованием современного оборудования.
Объекты исследования
1. Таблетки «Аримидекс®», покрытые оболочкой, №28, 1 мг производства компании «АстраЗенека Фармасьютикалс ЛП.», США. Серия: DF 960, произведены: 02 2006, годен до: 02 2011.
Состав: 1 таблетка, покрытая оболочкой содержит:
активное вещество: анастрозол 1 мг;
вспомогательные вещества: лактозы моногидрат, повидон, карбоксиметилен крахмал натрия, магния стеарат, вода очищенная
состав оболочки: макропол 300, гипромеллоза, титана диоксид, вода очищенная.
2. Таблетки «Анастера®», покрытые плёночной оболочкой, №28, 1 мг, производства компании «Лаборатория Блипак С.А.», Аргентина. Серия: ANO12A, произведены: 05/09/08, годен до: 09/2010.
Состав: 1 таблетка, покрытая плёночной оболочкой содержит:
активное вещество: анастрозол 1 мг;
вспомогательные вещества: лактозы моногидрат, крахмал кукурузный, повидон (поливинилпирролидон К-30), карбоксиметилкрахмал натрия, магния стеарат, опадрай II белый, гипролоза (гидроксипропилцеллюлоза) 28-40%, лактозы моногидрат 21-40%, макропол (полиэтиленгликоль 4000) 8-14%, титана диоксид (Е171) 20-30%.
3. Tаблетки «Веро-Анастрозол®», покрытые плёночной оболочкой, №28, 1 мг, производства компании ОАО «Верофарм», Россия. Серия: произведены: 10808, годен до: IX 10.
Состав: 1 таблетка, покрытая плёночной оболочкой, содержит:
активное вещество: анастрозол 1 мг;
вспомогательные вещества: крахмал кукурузный, лактоза (сахар молочный), повидон (поливинилпирролидон), карбоксиметилкрахмал натрия (прмогель), магния стеарат,
состав оболочки: гипромеллоза (гидроксипропилметилцеллюлоза), повидон (поливинилпирролидон), полисорбат (твин-80), тальк (магния гиброкси-силикат), титана диоксид.
Представленные образцы были исследованы на соответствие требованиям нормативной документации (НД), причём, для корреляции полученных данных, исследования проводили по НД фирмы производителя и разработчика данного препарата – компании «АстраЗенека Фармасьютикалс ЛП.», США.
Результаты и обсуждение
Исследование представленных на анализ образцов на подлинность подтверждалась методом высокоэффективной жидкостной хроматографии (ВЭЖХ) по сопоставлению на хроматограммах времен удерживания анастрозола стандартного и испытуемого растворов.
Определение средней массы и отклонений в массе проводили по методике и в соответствии с требованиями ГФ XI, вып. 2, стр. 156. Результаты данного теста представлены в табл. 1.
Таблица 1. Результаты определения средней массы таблеток и отклонения от средней массы
Объект
Средняя масса
20 таблеток, мг
Отклонение в массе отдельных таблеток, мг
Сравнительный фармакоэкономический анализ применения анастрозола, летрозола и экземестана при адъювантной терапии рака молочной железы
Полный текст:
Аннотация
Актуальность. В данной статье отражены результаты анализа эффективности затрат, сравнивающего альтернативные схемы гормональной терапии рака молочной железы (РМЖ) ингибиторами/инактиваторами ароматазы. Цель: сравнительная фармакоэкономическая оценка терапии анастрозолом, летрозолом и экземестаном пациенток с I–II стадиями РМЖ в условиях российской системы здравоохранения. Методология: Марковское моделирование, анализ эффективности затрат. Результаты. При анализе эффективности затрат инициальной адъювантной терапии при РМЖ наиболее экономически эффективным препаратом является летрозол. При анализе эффективности затрат при переключении с продолжением терапии тамоксифеном при РМЖ наиболее экономически эффективным препаратом является экземестан. Вывод. Все три препарата: анастрозол, летрозол и экземестан более чем в 2 раза меньше установленного «порога готовности платить», поэтому могут быть рекомендованы для включения в список ЖНВЛП (кроме анастрозола, который уже присутствует там) и для применения в системе государственного возмещения.
Ключевые слова
##article.ConflictsofInterestDisclosure##:
##article.articleInfo##:
Депонировано (дата): 06.06.2018
##article.reviewInfo##:
##article.editorialComment##:
Для цитирования:
Белоусов Д.Ю., Афанасьева Е.В., Зырянов С.К. Сравнительный фармакоэкономический анализ применения анастрозола, летрозола и экземестана при адъювантной терапии рака молочной железы. Качественная Клиническая Практика. 2012;(2):45-55.
Введение
Рак молочной железы (РМЖ) – занимает первое место среди злокачественных новообразований у женщин и является одной из главных причин смертности женского населения во всём мире. Заболеваемость РМЖ увеличивается с возрастом. Как правило, опухоли возникают после 35-40 лет, пик заболеваемости регистрируют у женщин в возрасте 60-65 лет [14].
В России в структуре заболеваемости злокачественными новообразованиями РМЖ занимает 1-ое место (18,1%). Распространённость РМЖ в 2011 г. на 100 000 населения – 369,5 человек. В 2011 г. выявлено 57 379 больных РМЖ женщин, из них 55 184 поставлено на учёт. Удельный вес больных с диагнозом, подтверждённым морфологически, от числа больных с впервые в жизни установленным диагнозом РМЖ – 96,6%. Удельный вес больных с опухолевым процессом I стадии от числа больных с впервые в жизни установленным диагнозом РМЖ – 18,5%, II стадии – 46,5%, III стадии – 24,8%, IV стадии – 9,1% [19].
Радикальное лечение РМЖ получило 36 469 женщин [19], в том числе:
Пятилетняя выживаемость в 2011 г. составила 57,6%. Индекс накопления контингентов больных с РМЖ – 9,5. Одногодичная летальность с момента установления РМЖ – 8,7% [19].
Как уже было сказано выше, среди женщин с впервые выявленным РМЖ в 65% случаев диагностируют I-II стадии заболевания [19]. Преобладающее большинство этих больных, после завершения хирургического этапа лечения, нуждается в проведении адъювантной лекарственной терапии. Одними из основных критериев выбора метода лекарственной терапии (использование цитостатиков, средств гормонотерапии) служит наличие или отсутствие экспрессии рецепторов эстрогенов, прогестерона и Her2-new в ткани опухоли, а так же состояние менструальной функции у женщины. Перечисленные факторы являются не только прогностическими, но и предсказательными в отношении чувствительности опухолевых клеток к тому или иному виду лечения и, в частности, гормонотерапии.
До настоящего времени ингибиторы/инактиваторы ароматазы третьего поколения служат краеугольным камнем гормонотерапии метастатического рака молочной железы, а сегодня всё шире используются для проведения адъювантной терапии у больных операбельным раком молочной железы в менопаузе. Последнее стало возможным после анализа результатов трёх крупных рандомизированных исследований, показавших, что использование ингибиторов/инактиваторов ароматазы III поколения: анастрозола, летрозола, экземестана в монорежиме или последовательно, после завершения 2-5 лет терапии тамоксифеном увеличивает длительность безрецидивного периода в сравнении с использованием тамоксифена [1, 2, 10-12].
Полученные данные кардинально изменили подходы к адъювантной гормонотерапии больных РМЖ в менопаузе.
Современные принципы адъювантной гормонотерапии больных РМЖ были сформулированы на совещании экспертов, состоявшемся в марте 2007 года в St. Gallen. А именно:
Изменение ранее существовавшей клинической практики проведения адъювантной терапии у больных РМЖ в менопаузе вызвало целый ряд вопросов у клиницистов:
Если обратиться к результатам ранее завершённых клинических исследований, нестероидные ингибиторы ароматазы III поколения (анастрозол и летрозол) и стероидный инактиватор (экземестан) снижают уровень эстрогенов в сыворотке крови более чем на 98%. Поэтому мы предположили, что любой из препаратов равно эффективен в режиме адъювантной терапии при гормоночувствительном РМЖ, любой режим терапии (моно или последовательно) в равной мере снижает абсолютный риск рецидива и риск смерти, и нет различий в побочных эффектах между лекарственными препаратами.
Очевидно, что для окончательного суждения о преимуществах или недостатках того или иного препарата и режиме его назначения, эффективности и безопасности терапии, сходстве и различиях между ингибиторами/инактиваторами ароматазы необходимы дальнейшие исследования. В современных условиях одним из основных критериев выбора схемы лечения, наряду с клинической эффективностью, переносимостью и безопасностью, является анализ эффективности затрат (cost effectiveness analysis / CEA). Любое различие по показателю «затраты-эффективность» (cost effectiveness ratio / CER) может оказаться существенным аргументом в пользу выбора того или иного лекарственного препарата и режима его назначения, поскольку даже при условиях схожей противоопухолевой эффективности ингибиторов/инактиваторов ароматазы, различные режимы терапии могут отличаться между собой по показателю CER.
В настоящее время в Российской Федерации требуется проведение оценки клинической и экономической эффективности медицинских технологий (ОМТ). Это является результатом осознания того, что решения, связанные с распределением ресурсов в стране с бюджетной системой финансирования здравоохранения, должны быть подкреплены информацией о стоимости лечения и об относительной эффективности медицинского вмешательства.
В данной статье отражены результаты анализа эффективности затрат, сравнивающего альтернативные схемы гормональной терапии рака молочной железы ингибиторами/инактиваторами ароматазы.
Цель исследования
Целью данной работы являлась сравнительная фармакоэкономическая оценка терапии анастрозолом, летрозолом и экземестаном пациенток с I-II стадиями РМЖ в условиях российской системы здравоохранения.
Задачи исследования
Популяция больных
Женщины, находящиеся в менопаузе, с I-II стадией рака молочной железы, находящиеся на гормональной адъювантной терапии ингибиторами/инактиваторами ароматазы.
Методология исследования
При проведении фармакоэкономического анализа был использован применяемый в РФ Отраслевой стандарт «Клинико-экономического исследования» [17]. Были использованы следующие методы экономического анализа:
Марковское моделирование. Для прогнозирования вероятности развития событий при лечении РМЖ и ассоциированных с ними прямых медицинских затрат за определённый период времени при использовании различных терапевтических стратегий была разработана Марковская модель, которая выбрана из-за длительного течения РМЖ. Её структура позволяет следующее:
Модель представлена на рис. 1 и табл. 1, продолжительность цикла модели 1 год (всего 5 циклов), включает следующие состояния [5]:
Рис. 1
Марковская модель прогрессирования рака молочной железы
Таблица 1
Матрикс Марковской модели рака молочной железы с переходом из одного состояния в другое
Для проведения клинико-экономического анализа разработан алгоритм принятия возможных решений при развитии рецидива заболевания (рис. 2).
Рис. 2
Алгоритм принятия возможных решений при развитии рецидива РМЖ («древо» решений)
Стоимость прямых медицинских затрат. По Стандарту оказания медицинской помощи больным со злокачественными новообразованиями молочной железы [20] были рассчитаны прямые медицинские затраты на использование медицинских ресурсов при оказании медицинской помощи больным РМЖ на:
Прямые медицинские затраты. Для расчётов ценовых показателей стоимости медицинских услуг мы использовали Прейскурант на оказание медицинских услуг клиник ПМГМУ им. И.М. Сеченова [18], ФГБУ «Российский научный центр рентгенорадиологии» за 2012 г. г. Москва [24]; цены на препараты сравнения были рассчитаны как средние розничные в аптеках г. Москвы [13].
Показатель эффективности затрат. Так как у сравниваемых стратегий разные показатели эффективности и затрат был проведён анализ показателя эффективности затрат (cost—effectiveness ratio – CER). Наиболее фармакоэкономически приемлемым считался наименьший показатель CER, который рассчитывался по следующей формуле:
CER = DC ÷ Ef, где
DC – прямые медицинские затраты (равно CoI – стоимости болезни);
Ef – эффективность (действенность), выраженная в показателях безрецидивной выживаемости (DFS – disease—free survival).
Вероятность перехода в состояние и эффективность препаратов. Вероятность перехода из одного состояния здоровья в другое и эффективность сравниваемых препаратов оценивалась по результатам контролируемых клинических исследований: ATAC [10, 11], ARNO 95 [6], BIG 1-98 [1, 2, 12], IES [3], на которых и обосновывался данный модельный фармакоэкономический анализ.
Вероятность перехода из одного состояния в другое
Исследование ATAC – оценка эффективности терапии анастрозолом по сравнению с тамоксифеном в качестве инициальной адъювантной терапии I-II стадии РМЖ (табл. 3) [10, 11].
Таблица 3
Вероятность перехода в исследовании ATAC из одного состояния в другое [10, 11]