артгелия что за лекарство
Препарат Артлегия для лечения коронавируса
В период отсутствия специфических медикаментов врачи использовали уже существующие медикаменты для лечения Covid-19. Некоторые из них позволяли получить отличные результаты, снизить проявление инфекции и улучшить состояние пациентов. Одним из них стала «Артлегия», которая прошла ряд клинических испытания и доказала свою эффективность. Поэтому лекарство стало одним из первых отечественных средств, включенных в список рекомендаций Минздрава. Насколько он подходящий, и как его применять, стоит разобраться подробнее.
Лекарственный препарат «Артлегиа» представляет собой отечественный продукт, который производит ярославская компания. Назначается пациентам в рамках рекомендаций Министерства здравоохранения для лечения коронавируса. Основным его преимуществом является предотвращение развития «цитокинового шторма» и поражения легких, сердца, легких, почек. Большинство зарегистрированных летальных случаев из-за него.
Артлегиа позволяет снизить иммунный ответ организма за счет особого механизма действия на этот белок. За непродолжительный период исследований было отмечена высокая эффективность борьбы с инфекцией. Поэтому Минздрав допустил его применение при лечении коронавируса.
Инструкция по применению препарата
Артлегия не является специфическим препаратом от коронавируса. Он не выпускается в форме таблеток, а представлен в виде инъекций. Предназначен для терапии ревматоидного артрита. Основным преимуществом выделяют успешное прохождение испытаний, в том числе и международных.
Препарат вводится подкожно в области бедра или передней брюшной стенки. Перед введением потребуется раствор нагреть до комнатной температуры. Для этого потребуется достать его из холодильника и оставить на 30 минут. Использовать горячую воду или другие приспособления недопустимо.
Первое применение стоит выполнить под контролем медицинского сотрудника. После этого состояние человека отслеживается в течение получаса. При введении применяют шприцы, предназначенные для однократного приема. В случае пропуска инъекции, следует руководствоваться рекомендациями производителя в инструкции по применению. Они подробно описаны в таблице.
| Режим дозирования | Интервал от даты пропуска | Действие |
| ОКЗ 64 мг к4н | ≤14 дней | Выполнить инъекцию вместо пропущенной и далее по графику |
| >14 дней | Отменить пропущенную инъекцию | |
| ОКЗ 64 мг к2н | ≤7 дней | Выполнить инъекцию вместо пропущенной и далее по графику |
| >7 дней | Отменить пропущенную инъекцию |
В процессе лечения пациента могут наблюдаться повышение показателей функции печени, усталость, тошнота, рвота, лихорадка или сыпь. Корректирует дозировку или отменяет препарат врач с учетом общего состояния и выраженность побочных эффектов.
Советы
Совет №1
Все лекарственные препараты имеет свои противопоказания. Поэтому перед началом применения рекомендуется проконсультироваться с врачом. Он изучит анамнез, проведет опрос и подберет подходящую дозировку.
Совет №2
Менять самостоятельно дозировку недопустимо. Увеличенное количество не позволит быстрее выздороветь, но спровоцирует появление ряда побочных эффектов. Сниженное количество не даст ожидаемого результата.
Совет №3
Принимать таблетки рекомендуется пациентам строго под контролем врача, который сможет отследить динамику терапии и своевременно ее скорректировать.
Совет №4
Недопустим прием препарата детям, женщинам в период беременности и пациентам с хроническими инфекционными заболеваниями.
Часто задаваемые вопросы
Можно ли использовать Артлегию для профилактики?
Артлегия представляет собой серьезное лекарственное средство, предназначенное для лечения ревматоидного артрита. Во время приема требуется контроль показателей и состояния больного. У пациентов могут наблюдаться нежелательные реакции в виде нейтропении, лейкопении, повышения уровня печеночных трансаминаз. Поэтому его использование в профилактических целях недопустимо.
Доказана ли эффективность Артелгии в лечении коронавируса?
Известно 30 случаев успешного лечения пациентов препаратом. Исследования проводились в 17 стационарах в разных городах России. Они были выписаны домой после выздоровления и за их состоянием продолжают наблюдать специалисты. Точной статистики нет, а применение его приостановлено, после выпуска специфического препарата для лечения Covid-19 «Авифавир».
Можно ли Артелгию комбинировать с другими препаратами?
Да, медикамент можно принимать в комплексе с другими препаратами. Но схему лечения и дозировку подбирает врач с учетом возраста пациента, наличия хронических патологий, тяжести коронавируса. Следует учитывать, что клинических исследований лекарственных взаимодействий олокизумаба не проводилось.
Одна ампула – 50 тысяч рублей: кому необходим самый дорогой препарат при COVID-19?
Сейчас в аптеках стали продавать лекарства, выпущенные именно для лечения COVID-19. Но некоторые препараты, назначаемые при лечении коронавируса, не купишь просто так Фото: Галина Соловьёва
На все препараты, входящие в действующие рекомендации Министерства здравоохранения России по лечению COVID-19, с декабря 2020 года по май 2021 года в нашей стране израсходовали более 40 миллиардов рублей. Больше всего затрат пришлось на фавипиравир, в народе известный под торговым названием Арепливир – 6,6 миллиарда рублей (одна упаковка из 40 таблеток – 5 тысяч рублей в среднем). А вот на втором месте оказался малоизвестный препарат Артлегиа – на его закупку потратили 6,3 миллиарда рублей (одна ампула стоит примерно 50 тысяч рублей). «ОГ» узнала, что это за препарат, кому он показан и нет ли проблем с его закупками у свердловских больниц.
Только для тяжелобольных
– Мой отец тяжело заболел коронавирусом, в течение нескольких дней его состояние в больнице не улучшалось, и в медучреждении сказали приобрести препарат Артлегиа, – рассказывает екатеринбуржец Артём Смолин. – Пришлось купить это лекарство, которое оказалось совсем не дешёвым. Радует, что отцу стало лучше, но очень интересно, что это за чудо-препарат, названия которого я никак не мог найти в рекомендациях Минздрава России по лечению больных коронавирусом? Почему больница не предоставила это лекарство в рамках лечения по системе ОМС?
Как выяснилось, препарат Артлегиа, разработанный группой компаний «Р-Фарм», уже давно существует на рынке как средство для лечения ревматоидных заболеваний. Во временные методические рекомендации Министерства здравоохранения России по профилактике, диагностике и лечению COVID-19 его включили ещё в июне 2020 года. Однако в них он, как и многие другие лекарства, занесён не под торговым названием, а под наименованием, означающим действующее вещество препарата – олокизумаб.
Казалось бы, где связь между ревматоидным артритом и коронавирусом. Но по мере узнавания COVID-19 медики и учёные выяснили, что организм человека при этой болезни часто максимально активирует защитные механизмы иммунитета для борьбы с вирусом, что вызывает неконтролируемый выброс белков, приводящих к цитокиновому шторму и поражению внутренних органов: лёгких, сердца, почек. Клетки организма провоцируют воспаление и по сути сами себя убивают. А Артлегиа, как показали клинические испытания, позволяет оказывать влияние на этот белок так, чтобы снизить иммунный ответ организма. Так что называть его лекарством именно от коронавируса не совсем верно.
– Это специфический генно-инженерный препарат, который входит в схемы лечения ковидных больных, – комментирует «Облгазете» главный внештатный специалист по инфекционным болезням в Свердловской области Марина Холманских. – В свердловских ковидных больницах его также применяют, но назначают не всем подряд, а только при тяжёлых формах коронавируса по строгим клиническим и лабораторным показаниям – с целью упреждающего противовоспалительного действия или уже подавления цитокинового шторма, возникшего на фоне COVID-19. То есть человек уже находится в больнице в тяжёлом состоянии. Артлегиа относится к группе генно-инженерных препаратов – ингибиторов интерлейкина-6, поэтому помимо неё в рекомендации Минздрава входят и другие похожие лекарства. Те, что посильнее, как Артлегиа, применяются в инъекционных формах, послабее – в таблетках. Но все они находятся в одном ценовом диапазоне.
С весны – около 80 упаковок
По словам Марины Холманских, высокие цены на Артлегиа и другие препараты этой группы объясняются тем, что на исследовательские работы при их создании было потрачено очень много денег и сил. Выпускаются они в ограниченных количествах, так как пациентов с ревматоидными заболеваниями у нас не так много. Но, несмотря на выросшую востребованность этого препарата из-за пандемии, ситуация не изменилась.
– Сейчас мы находимся на гребне третьей волной коронавируса, в стационарах лечится большое количество пациентов, и есть большая потребность в этих препаратах не только в нашей области, но и во всей стране, – говорит главный инфекционист Среднего Урала. – При этом количество фабрик и заводов, которые производят эти препараты, не увеличилось. Соответственно, возник дефицит лекарств. Есть медицинские организации, которые смогли заключить договоры на поставку этих препаратов и закупить их, а какие-то хотят, но не могут этого добиться. Цены на эти препараты, конечно, поднялись, но незначительно: что в начале пандемии стоили в районе 50 тысяч рублей, что сейчас.
Мы позвонили главным врачам Богдановичской ЦРБ, Шалинской и Кировградской ЦГБ – они ответили, что их больницы не закупают Артлегиа и другие похожие препараты, так как в их медучреждениях не размещают больных коронавирусом, которым показано такое лечение. А вот в екатеринбургской ГКБ №14, в которую привозят ковидных больных разной степени тяжести, этот препарат закупают и используют.
– С этой весны наша больница уже два раза закупала Артлегиа: первый раз – около 50 упаковок, второй раз – около 30. Трудностей с закупками не было, – рассказали «ОГ» в пресс-службе екатеринбургской городской больницы №2. – Курс лечения для одного больного – упаковка, это одна ампула. Препарат, конечно, дорогой, но зато очень эффективный.
В аптеке не найдёшь
По словам Марины Холманских, все свердловские больницы закупают Артлегиа только на те деньги, которые предоставляются в рамках системы Обязательного медицинского страхования (ОМС).
– Я не слышала, чтобы в больницах нашего региона не хватало каких-то препаратов для лечения коронавирусных больных: все стараются всё закупать, – комментирует врач. – Если где-то создаётся временный дефицит чего-то, то медучреждение просит необходимый препарат у другой больницы, но, разумеется, с возвратом. Это не возбраняется: всё делается в интересах пациентов.
Учитывая показания для назначения, приобрести Артлегиа просто так нельзя: на сайте Медгородок.ру, где отражается наличие всех препаратов в аптеках Свердловской области, его нет. Как извернуться с его покупкой обычному человеку в случае необходимости – непонятно. Но по идее таких случаев быть и не должно, даже несмотря на дефицит необходимых препаратов на рынке сегодня.
– В начале пандемии мы вместе с инфекционистами нашего региона провели оценку каждого случая лечения коронавируса. Для всех случаев у нас рассчитана средняя стоимость лечения применяемых препаратов, – рассказали «Облгазете» в пресс-службе Территориального фонда обязательного медицинского страхования Свердловской области. – Артлегиа есть в официальных схемах лечения больных COVID-19, поэтому этот препарат входит в оплату по системе ОМС и бесплатно предоставляется пациентам.
Если же вас по какой-то причине вынудили приобрести препарат, который должен бесплатно предоставляться больницей, то руководитель Свердловской общественной организации по защите прав пациентов Максим Стародубцев рекомендует смело обращаться в вашу страховую компанию, которая поможет возместить понесённые расходы.
Важно
Действующая одиннадцатая версия временных методических рекомендаций Минздрава России по лечению больных COVID-19 предупреждает: при назначении указанных генно-инженерных препаратов, к которым относится и Артлегиа, повышается риск развития вторичной бактериальной инфекции, то есть пневмонии (о том, чем обычное воспаление лёгких отличается от поражения лёгких при COVID-19 и от внебольничной пневмонии – в материале «ОГ» №135 от 28.07.2021).
Сюжет

Рассказываем, как борются с коронавирусной инфекцией в других странах
Регистрационное удостоверение:
Торговое наименование:
Международное непатентованное наименование:
Лекарственная форма:
раствор для подкожного введения
Состав на 1 мл:
Действующее вещество: олокизумаб – 160,0 мг
Вспомогательные вещества: натрия хлорид, полисорбат 80, L-гистидина гидрохлорида моногидрат, сорбитол, вода для инъекций.
Описание
Прозрачная или слегка опалесцирующая жидкость от бесцветного до светло-желтого цвета.
Фармакотерапевтическая группа:
Код ATX:
Фармакологические свойства:
Олокизумаб представляет собой гуманизированное (с присоединенным гипервариабельным участком) моноклональное антитело, относящееся к изотипу иммуноглобулина (immunoglobulin, Ig) G4/каппа. Олокизумаб селективно связывается с человеческим ИЛ-6 и эффективно нейтрализует эффекты ИЛ-6 in vivo и in vitro. Полученные данные свидетельствуют о том, что олокизумаб не связывается в значительной степени с другими молекулами семейства ИЛ-6 и не влияет на их функционирование, а также не активирует сигнальный путь ИЛ-6.
Фармакодинамика:
В двойных слепых рандомизированных клинических исследованиях 2 фазы подкожное введение олокизумаба в дозе от 60 до 480 мг/мес пациентам со среднетяжелым или тяжелым ревматоидным артритом вызывало выраженное снижение уровня С-реактивного белка (СРБ) в плазме в течение 7 дней от начала лечения, сохранявшееся в течение не менее 10 недель после однократного введения, и в течение всего периода терапии при многократном введении препарата.
У пациентов со среднетяжелым или тяжелым ревматоидным артритом, недостаточно контролируемым терапией метотрексатом, подкожное введение олокизумаба в дозе 64 мг каждые 2 недели (к2н) или 64 мг каждые 4 недели (к4н) вызывало резкое снижение среднего уровня СРБ в плазме ко 2 неделе лечения. Низкие уровни СРБ сохранялись в течение 24 недель на протяжении всего периода лечения.
Клиническая эффективность:
Эффективность подкожного введения олокизумаба в дозе 64 мг каждые 2 недели (к2н) и каждые 4 недели (к4н) была изучена у пациентов со среднетяжелым или тяжелым ревматоидным артритом, недостаточно контролируемым терапией метотрексатом, в клиническом исследовании CREDO1.
Олокизумаб в обеих дозировках был значительно эффективнее плацебо в отношении снижения активности ревматоидного артрита вне зависимости от пола, индекса массы тела, активности заболевания, уровня антител к ревматоидному фактору и/или циклическому цитрирулированному пептиду. Длительность периода от постановки диагноза до начала лечения и продолжительность предшествующей терапии метотрексатом также не влияла на клиническую эффективность препарата. Кроме того, доля пациентов, достигших низкой активности заболевания и ремиссии, была значимо выше среди получавших олокизумаб по сравнению с плацебо. У пациентов, получавших олокизумаб, также чаще отмечалось улучшение качества жизни, уменьшение боли и количества болезненных и припухших суставов. Воздействие олокизумаба было заметным уже через 4 недели лечения, выраженный эффект развивался приблизительно через 12 недель от начала введения препарата и сохранялся в течение не менее чем 24 недель.
Фармакокинетика
Биодоступность олокизумаба оценивалась на основании данных, полученных для 173 пациентов с легким или умеренным ревматоидным артритом, получавших олокизумаб в различных дозах в течение 12 недель, объединенных с данными, полученными у 40 пациентов с легким или умеренным ревматоидным артритом после однократного введения различных доз олокизумаба и данными, полученными у 41 здорового добровольца после однократного введения различных доз олокизумаба. При подкожном введении биодоступность составляет 63% (доля относительной стандартной ошибки (% ОСО) = 4,9%).
После однократного подкожного введения олокизумаба пациентам с легким или умеренным ревматоидным артритом в дозах от 0,3 до 6 мг/кг максимальная концентрация препарата в крови (Сmax) дозозависимо возрастала. Время достижения Сmax составляло от 4 до 12 дней, при этом поддающиеся определению уровни олокизумаба сохранялись приблизительно до 16 недель.
После однократного подкожного введения олокизумаба в дозе 64 мг пациентам с ревматоидным артритом средней и тяжелой степени, недостаточно контролируемым на фоне лечения метотрексатом, Сmax достигалась в среднем через 7-10 дней (Таблица 1).
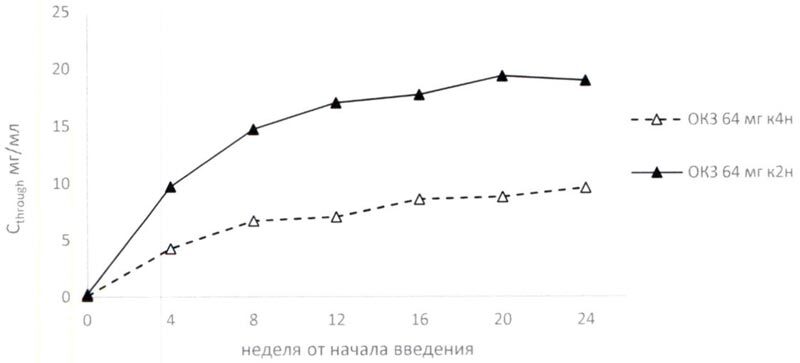
При многократном введении стационарная концентрация олокизумаба в крови нарастала в течение начального периода терапии и достигала равновесного состояния через 16 (64 мг к4н) и 14 (64 мг к2н) недель от начала лечения (Таблица 1, Рисунок 1).
Таблица 1. Фармакокинетические параметры олокизумаба после подкожного введения пациентам с РА средней и тяжелой степени
| ФК параметр | Исходные значения | Неделя 20 | ||
| ОКЗ 64 мг к4н N = 18 | ОКЗ 64 мг к2н N = 18 | ОКЗ 64 мг к4н N = 18 | ОКЗ 64 мг к2н N = 18 | |
| Сmax (мкг/мл) | 6,18 | 6,22 | 17,00 | 21,55 |
| % CV | 50,0 | 39,2 | 55,7 | 25,0 |
| AUC0-t* (мкг*ч/мл) | 2886 | 1556 | 8411 | 5485 |
| % CV | 45,3 | 38,9 | 29,9 | 31,8 |
| tmax (ч) | 190,2 | 234,4 | 244,5 | 127,8 |
| Медиана | 166,5 | 236,7 | 167,6 | 96,7 |
| Мин. – макс. | 92,8-402,3 | 95,8-359,2 | 95,4-670,7 | 0,0-334,7 |
РА – ревматоидный артрит; ОКЗ – олокизумаб; к2н – каждые 2 недели; к4н – каждые 4 недели; Сmax – максимальная концентрация препарата в крови; AUC0-t – площадь под кривой концентрация-время; tmax – время достижения максимальной концентрации препарата; *AUC для введения к4н рассчитывалась за период 672 часа (28 дней) и для введения к2н за период 336 часов (14 дней)
В исследовании in vitro на криоконсервированных гепатоцитах человека олокизумаб обращал ингибиторный эффект ИЛ-6 на активность CYP1А1/2, 2В6, 2С9, 3А4/5 и 2С19, а также на активность NTCP.
Оценки клиренса олокизумаба у пациентов с легким или умеренным ревматоидным артритом составляли 0,17 л/сут (доля относительной стандартной ошибки [% ОСО] = 4,9%) с низкой или средней индивидуальной вариабельностью.
Уровень снижения СРБ у пациентов с активным ревматоидным артритом, получавших олокизумаб, не зависел от дозы препарата. Кроме того, у пациентов с легким и умеренным ревматоидным артритом была выявлена положительная корреляция концентрации олокизумаба в плазме с уровнем нейтропении, повышением уровней ACT, АЛТ и триглицеридов в плазме, хотя величина эффекта была невелика. Также к 14 дню после введения олокизумаба наблюдалось стойкое снижение уровня VEGF и амилоидного сывороточного белка А во всех терапевтических группах без зависимости от дозы.
Показания к применению
Терапия пациентов старше 18 лет с ревматоидным артритом средней или высокой степени активности в комбинации с метотрексатом, при недостаточной эффективности монотерапии метотрексатом.
Противопоказания
Гиперчувствительность к олокизумабу, любому компоненту препарата в анамнезе.
Активные инфекционные заболевания (в том числе и туберкулез).
Детский возраст до 18 лет.
Наследственная непереносимость фруктозы (препарат содержит сорбитол).
Период грудного вскармливания.
С осторожностью
Применение при беременности и в период грудного вскармливания
Перед назначением препарата Артлегиа женщинам детородного возраста следует выполнить тест на беременность. Лечащий врач должен подробно разъяснить риски применения препарата Артлегиа во время беременности и проинструктировать пациентку, способную к деторождению, о необходимости использования высокоэффективных методов контрацепции и выполнения регулярных тестов на беременность во время лечения и в течение по крайней мере 6 месяцев после получения последней дозы препарата Артлегиа. В случае, если пациентка, получающая препарат Артлегиа, забеременеет, она должна немедленно прекратить применение препарата и обратиться к врачу.
Применение препарата Артлегиа у беременных систематически не изучалось. В связи с тем, что препарат Артлегиа показан к применению в комбинации с метотрексатом, имеющим хорошо известное тератогенное действие, применение препарата Артлегиа при беременности не рекомендуется.
В исследованиях на животных обнаружена репродуктивная токсичность. Предполагается, что ИЛ-6 играет важную роль в раскрытии шейки матки и, возможно, в рождении плаценты. Таким образом, применение препарата Артлегиа может нарушать родовую деятельность.
Проникновение олокизумаба в грудное молоко не изучалось. Клинические данные о риске для ребенка, находящегося на грудном вскармливании, отсутствуют. Так как препарат Артлегиа показан к применению в комбинации с метотрексатом, который секретируется в грудное молоко, рекомендуется прекратить грудное вскармливание при назначении препарата.
Клинические данные о влиянии олокизумаба на фертильность у человека отсутствуют.
В исследованиях на животных отрицательного воздействия олокизумаба на фертильность самцов и самок яванских макак не обнаружено.
Способ применения и дозы
Препарат Артлегиа вводится подкожно, в область бедра или передней брюшной стенки, 0,4 мл раствора с концентрацией 160 мг/мл единовременно. Перед введением раствор следует нагреть до комнатной температуры. Время хранения препарата при температуре >8 °С не должно превышать 4 часов.
Первое применение препарата проводят под контролем квалифицированного медицинского сотрудника. После первой инъекции следует наблюдать за состоянием пациента в течение 30 минут. После обучения технике выполнения подкожных инъекций под контролем медицинского сотрудника пациент (или лицо, осуществляющее за ним уход) может вводить препарат самостоятельно. Решение о возможности самостоятельного введения препарата Артлегиа пациентом принимает врач, имеющий опыт диагностики и лечения ревматоидного артрита.
Для введения препарата Артлегиа следует использовать только шприцы для однократного применения.
Если была пропущена очередная инъекция препарата, следует ввести пропущенную дозу как можно быстрее, при этом интервал между любыми двумя введениями должен составлять не менее половины интервала выбранного режима дозирования (см. Таблица 2).
Таблица 2. Действия в случае пропуска инъекции
| Режим дозирования | Интервал от даты пропуска | Действие |
| ОКЗ 64 мг к4н | ≤14 дней | Выполнить инъекцию вместо пропущенной и далее по графику |
| >14 дней | Отменить пропущенную инъекцию | |
| ОКЗ 64 мг к2н | ≤7 дней | Выполнить инъекцию вместо пропущенной и далее по графику |
| >7 дней | Отменить пропущенную инъекцию |
ОКЗ – олокизумаб; к2н – каждые 2 недели; к4н – каждые 4 недели
Прекращение применения препарата
Терапию препаратом Артлегиа следует отменить, если у пациента наблюдается:
Повышение биохимических показателей функции печени, соответствующее следующим условиям:
У пациента наблюдаются любые из перечисленных ниже лабораторных отклонений:
Подтвержденная беременность во время применения препарата Артлегиа (см. раздел «Применение при беременности и в период грудного вскармливания»).
Перфорация желудочно-кишечного тракта (см. раздел «Особые указания»).
Тяжёлая или угрожающая жизни инфекция (см. раздел «Особые указания»).
Применение у детей
Безопасность и эффективность препарата Артлегиа у детей и подростков младше 18 лет на данный момент не установлены. Данные по применению отсутствуют.
Рекомендуемая доза составляет 64 мг 1 раз каждые 4 недели или 1 раз каждые 2 недели подкожно.
Особые группы пациентов
Пожилые пациенты (>65 лет): коррекция дозы не требуется.
Пациенты с почечной недостаточностью: безопасность и эффективность препарата Артлегиа у пациентов с почечной недостаточностью не изучалась. Данные по применению отсутствуют.
Пациенты с печеночной недостаточностью: безопасность и эффективность препарата Артлегиа у пациентов с печеночной недостаточностью не изучалась. Данные по применению отсутствуют.
Инструкция по подготовке к инъекции и введению препарата
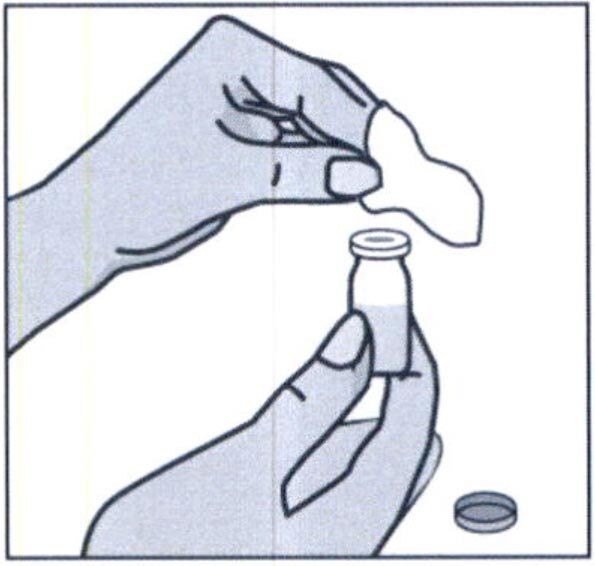
Извлеките флакон с препаратом Артлегиа из холодильника заранее: следует подождать примерно 30 минут перед инъекцией, чтобы препарат нагрелся до комнатной температуры. Не подогревайте препарат.
Подготовьтесь к инъекции
Вымойте руки теплой водой с мылом, выберите ровную чистую поверхность, внимательно осмотрите флакон с препаратом и не используйте его, если:
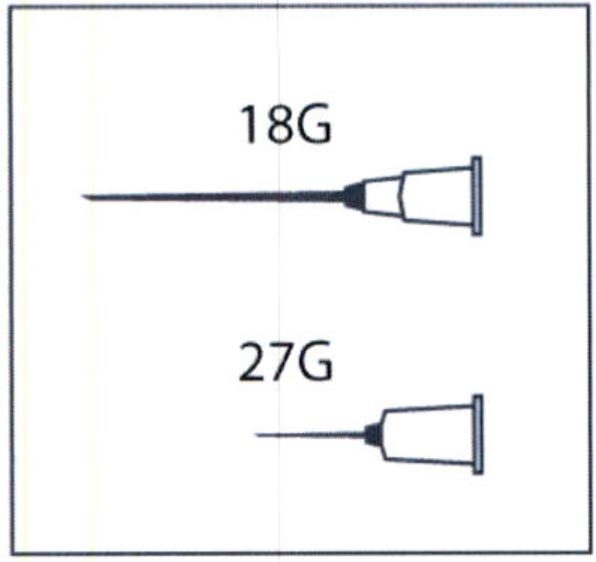
Приготовьте одноразовый шприц для подкожных инъекций вместимостью 1-2 мл, две одноразовых стерильных инъекционных иглы (рекомендуется использовать иглу размера 18G для набора препарата из флакона и иглу 27G для выполнения подкожной инъекции), 2 спиртовые и 1 стерильную салфетки.
Наденьте на шприц более толстую иглу для набора препарата, не снимая защитный колпачок. Удалите пластмассовую защитную крышку с флакона, протрите резиновую пробку спиртовой салфеткой.
Возьмите шприц в правую руку, удалите колпачок с иглы шприца и введите иглу вертикально в центр пробки флакона так, чтобы кончик иглы появился с внутренней стороны пробки.
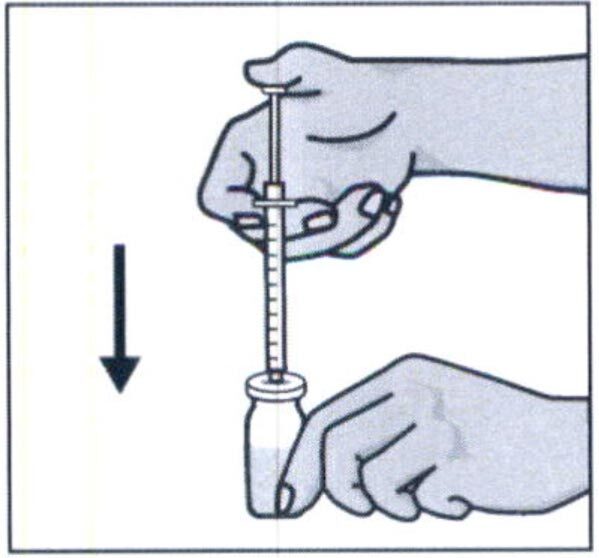
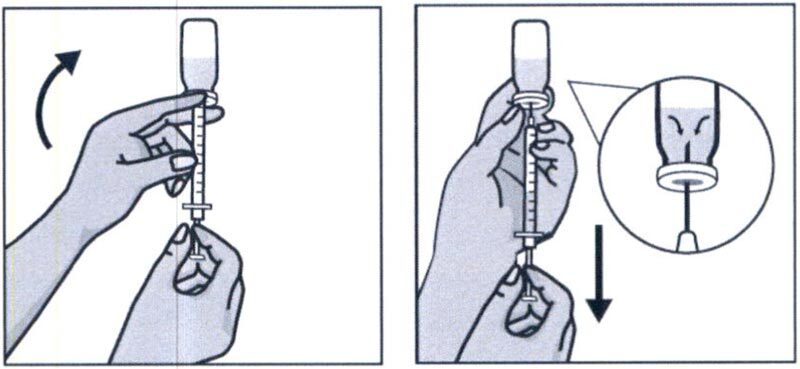
Удерживая правой рукой шприц, возьмите левой рукой флакон и переверните его так, чтобы вся жидкость собралась над пробкой. Оттягивая поршень шприца вниз, наберите в шприц все содержимое флакона.
Вытащите иглу из флакона и закройте колпачком. Не снимая защитный колпачок замените на иглу для подкожных инъекций. Использованную иглу для набора препарата выбросьте в контейнер для острых предметов.
Внимание! Не выполняйте инъекцию иглой для набора препарата, это может привести к боли и повреждениям в месте инъекции.
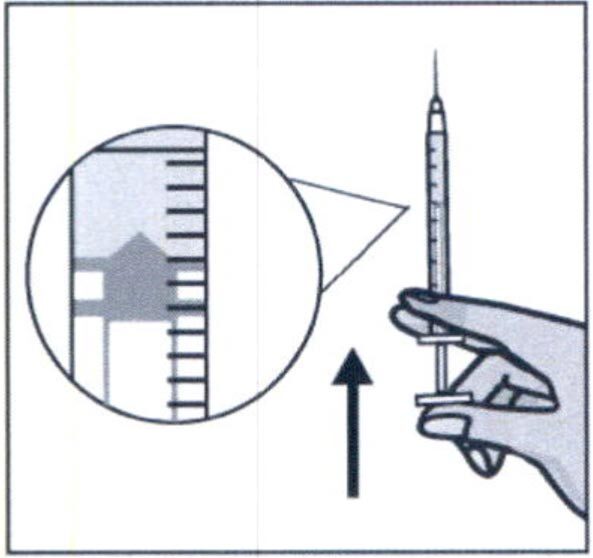
Осторожно снимите колпачок с иглы для подкожных инъекций. Не прикасайтесь к ней и соблюдайте осторожность чтобы не уколоться кончиком иглы. Удерживайте шприц вертикально и постучите по нему пальцем, чтобы пузырьки воздуха поднялись вверх. Удерживая шприц вертикально, медленно сдвиньте поршень чтобы изгнать из шприца воздух и избыточный объем жидкости так, чтобы поршень шприца остановился на отметке 0,4 мл.
Поместите шприц на картонную коробку таким образом, чтобы игла оставалась сверху упаковки и не касалась других поверхностей.
Выберите место для инъекции
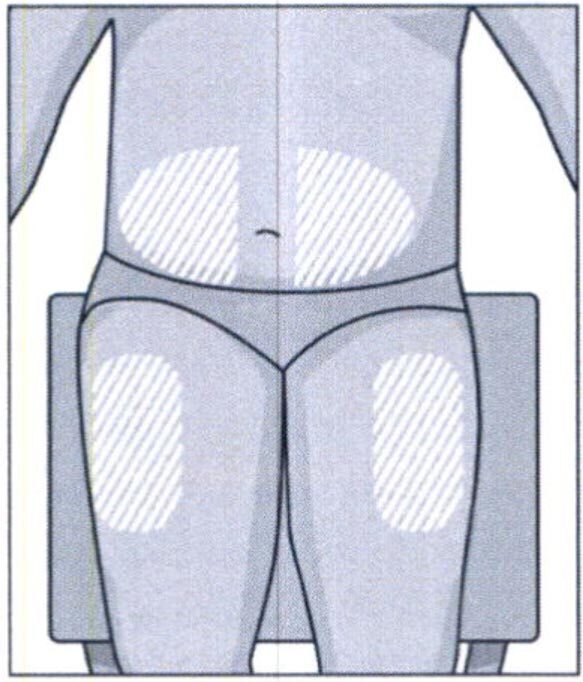
Выберите место инъекции на верхней части бедра или на животе на расстоянии не менее 5 см от пупка. Если инъекции делает медицинский работник, то препарат можно вводить в другие места для подкожных инъекций. Не рекомендуется введение препарата в места родинок, шрамов, повреждений или уплотнений, покраснений, повышенной чувствительности кожных покровов.
Рекомендуется регулярно менять место введения препарата. Новое место для инъекции должно находиться на расстоянии не менее 2,5 см от предыдущего места инъекции. При желании можно поочередно выполнять инъекции под кожу бедер и живота.
Протрите кожу выбранного места инъекции новой спиртовой салфеткой. Позвольте месту инъекции высохнуть и не прикасайтесь к нему до инъекции.
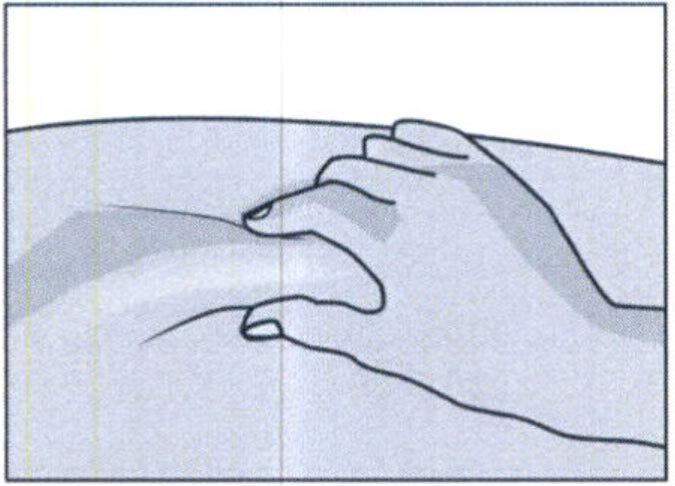
Осторожно сожмите кожу вокруг обработанного места инъекции второстепенной рукой (например, если Вы правша, используйте левую руку) и плотно удерживайте ее.
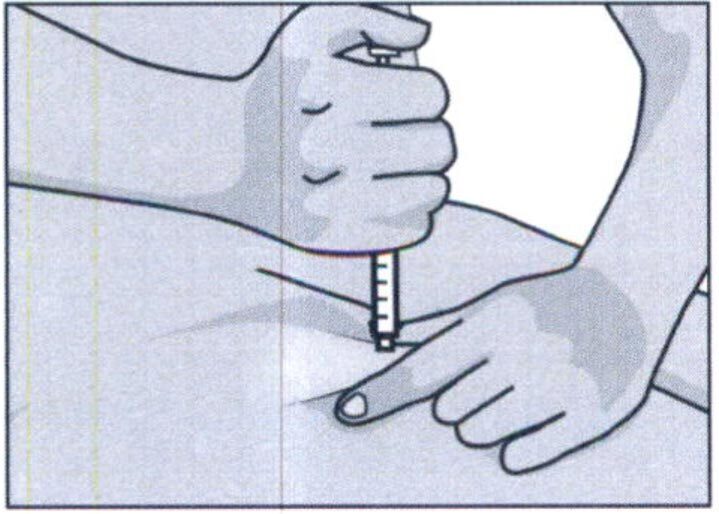
Удерживайте шприц в ведущей руке над приподнятым участком кожи под углом 90 градусов. Воткните иглу в кожу быстрым плавным толкающим движением. Если количество подкожного жира на брюшной стенке невелико, можно выполнять инъекцию под углом 45 градусов.
Не смещайте иглу относительно тканей и медленно нажимайте на поршень, пока весь объем препарата из шприца не будет введен под кожу. Поршень должен достичь дна шприца. Подождите несколько секунд перед извлечением иглы.
Извлеките иглу из кожи под тем же углом, под которым она была введена. В месте инъекции возможно небольшое кровотечение. При необходимости приложите стерильную салфетку на место инъекции.
Помните!
Выбрасывайте использованные шприцы в контейнер для острых предметов сразу после инъекции. Когда контейнер будет заполнен полностью, аккуратно и тщательно закройте его и выкиньте в мусорное ведро.
Всегда используйте новый шприц, не используйте повторно старые шприцы.
Побочное действие
Безопасность применения препарата Артлегиа оценивалась в двойном слепом рандомизированном клиническом исследовании CREDO1. Всего в исследовании участвовало 428 пациентов со среднетяжелым и тяжелым ревматоидным артритом с недостаточным контролем на терапии метотрексатом. 142 пациента получали олокизумаб в дозе 64 мг один раз каждые 2 недели (к2н), 143 пациента получали олокизумаб 64 мг один раз каждые 4 недели (к4н), 143 пациента получали плацебо. Все пациенты находились на фоновой терапии метотрексатом.
Наиболее часто встречающимися нежелательными реакциями были лейкопения, нейтропения, повышение уровня печеночных трансаминаз.
Перечень нежелательных реакций приведен в соответствии с системно-органными классами (СОК) MedDRA. В пределах каждого класса нежелательные реакции распределены по категориям частоты встречаемости: очень часто (≥1/10), часто (от ≥1/100 до
| Класс частоты | |||
| Перечень СОК | Очень часто | Часто | Нечасто |
| Инфекции и паразитарные заболевания | бронхит | легочный туберкулез, кандидоз кожи, вульвовагинальный кандидоз, отрубевидный лишай, подкожный абсцесс, рожистое воспаление, сепсис, вызванный стафилококковой инфекцией, синдром токсического шока | |
| Нарушения со стороны крови и лимфатической системы | лейкопения, нейтропения | эозинофилия | |
| Нарушения метаболизма и питания | гиперхолестеринемия | ||
| Нарушения со стороны печени и желчевыводящих путей | повышение уровня ACT, повышение уровня АЛТ | повышение уровня ГГТ | |
| Нарушения со стороны кожи и подкожных тканей | зуд, сыпь | изменение цвета пота, дерматит, экхимоз, зудящая сыпь | |
| Общие нарушения и реакции в месте введения | боль в месте инъекции, эритема | ||
| Лабораторные и инструментальные данные | позитивный тест на микобактерию туберкулеза | ||
Несмотря на то, что у пациентов в исследовании CREDO1 не было выявлено нежелательных явлений со стороны желудочно-кишечного тракта (ЖКТ), связанных с применением олокизумаба, в продолжающихся клинических исследованиях, включающих в общей сложности более 2000 пациентов с ревматоидным артритом, были зарегистрированы случаи перфорации дивертикула, связанные с применением олокизумаба. Частота данной нежелательной реакции неизвестна. В связи с тем. что риск перфорации желудочно-кишечного тракта характерен для ингибиторов ИЛ-6, следует соблюдать осторожность при применении препарата у пациентов с факторами риска перфорации ЖКТ.
В исследовании CREDO1 наблюдалось дозозависимое увеличение реакций гиперчувствительности в группах пациентов, получавших олокизумаб: доля пациентов, у которых в ходе лечения возникло хотя бы одно нежелательное явление, относящееся к реакциям гиперчувствительности, включая: зуд, сыпь, аллергический дерматит, повышение уровня эозинофилов в крови, составила 4,2% в группе, получавшей олокизумаб к4н, 7,0% в группе, получавшей олокизумаб к2н и 2,1% в группе плацебо.
В продолжающихся клинических исследованиях был зарегистрирован случай анафилактической реакции на введение олокизумаба (частота неизвестна).
В исследовании CREDO1 инфекции встречались с приблизительно одинаковой частотой во всех терапевтических группах: 14,1% в группе, получавшей олокизумаб 64 мг к4н, 15,4% в группе, получавшей олокизумаб 64 мг к2н и 16,2% в группе плацебо.
В группе пациентов, получавших олокизумаб 64 мг к2н, чаще развивались связанные с инфекциями серьезные нежелательные явления (2.8%) по сравнению с группой пациентов, получавших олокизумаб 64 мг к4н (0%) и плацебо (1,4%).
В группах пациентов, получавших олокизумаб, были зарегистрированы следующие случаи серьезных инфекций, не встречавшихся в группе плацебо: подкожный абсцесс (2), легочный туберкулез (1), сепсис, вызванный стафилококковой инфекцией (1), и синдром токсического шока (1).
Повышение уровня печеночных трансаминаз
В исследовании CREDO1 частота повышения АЛТ, расцененного исследователями как нежелательное явление, составляла 23,2% в группе, получавшей олокизумаб 64 мг к4н. 17,5% в группе, получавшей олокизумаб 64 мг к2н и 17,7% в группе плацебо. Частота повышения ACT, расцененного исследователями как нежелательное явление, составляла 15,5% в группе, получавшей олокизумаб к4н, 11,2% группе, получавшей олокизумаб к2н и 7,0% в группе плацебо.
В целом в течение периода терапии наблюдались колебания индивидуальных уровней АЛТ. Всего подъем уровня АЛТ выше верхней границы нормы (1×ВГН) отмечался хотя бы один раз за период лечения (24 недели) приблизительно у 50% пациентов, получавших олокизумаб и у 27% пациентов, получавших плацебо (Таблица 4). Ни у кого из пациентов не отмечалось одновременного повышения АЛТ и ACT >3×ВГН с повышением билирубина >2×ВГН.
Таблица 4 Повышение уровня АЛТ у пациентов в исследовании CREDO1
| Уровень АЛТ | Доля пациентов | |||||
| Исходный уровень | За период лечения* | |||||
| ОКЗ 64 мг к4н | ОКЗ 64 мг к2н | Плацебо | ОКЗ 64 мг к4н | ОКЗ 64 мг к2н | Плацебо | |
| >1×ВГН ≤3×ВГН | 9,9% | 8,4% | 9,9% | 52,9% | 47,5% | 27,0% |
| >3×ВГН ≤5×ВГН | 0 | 0 | 0 | 5,7% | 6,4% | 3,5% |
| >5×ВГН | 0 | 0,7% | 0 | 5,7% | 2,8% | 1,4% |
*учитывалось наибольшее значение АЛТ у каждого пациента за 24-недельный период лечения
ВГН – верхняя граница нормы; ОКЗ – олокизумаб
В исследовании CREDO1 повышение уровня липидов крови на фоне лечения, расцененное исследователями как нежелательное явление, наблюдалось у 8,5% пациентов в группе, получавшей олокизумаб 64 мг к4н, 8,4% пациентов в группе, получавшей олокизумаб 64 мг к2н и 2,8% пациентов в группе плацебо.
В среднем уровни общего холестерина, ЛПНП и ЛПВП возрастали в группах пациентов, получавших олокизумаб, в течение первых 4 недель терапии. Затем в группе, получавшей олокизумаб 64 мг к2н, средние уровни липидов снижались и к концу периода лечения возвращались к значениям в группе плацебо, тогда как у пациентов, получавших олокизумаб 64 мг к4н, высокие средние уровни липидов в крови сохранялись до конца периода лечения.
В исследовании CREDO1 среднее абсолютное число нейтрофилов через 12 недель терапии снизилось в группах, получавших олокизумаб, по сравнению с плацебо и затем оставалось стабильным до конца периода лечения (Таблица 5).
Таблица 5. Динамика среднего абсолютного числа нейтрофилов в течение 24 недель терапии
| Длительность лечения | Препарат и доза | ||
| ОКЗ 64 мг к4н | ОКЗ 64 мг к2н | Плацебо | |
| 0 | 5,9×10 9 /л | 5,2×10 9 /л | 5,7×10 9 /л |
| 12 недель | 3,9×10 9 /л | 3,4×10 9 /л | 5,6×10 9 /л |
| 24 недели | 3,7×10 9 /л | 3,2×10 9 /л | 5,3×10 9 /л |
Соответственно доля пациентов, у которых хотя бы один раз в ходе лечения регистрировалось такое нежелательное явление, как нейтропения, составляла 11,2% пациентов в группе, получавшей олокизумаб 64 мг к4н, 7,7% пациентов в группе, получавшей олокизумаб 64 мг к2н и 3,5% пациентов в группе плацебо.
Передозировка
В клинических исследованиях случаев передозировки не наблюдалось. Однако дополнительные клинические данные показывают, что общий профиль безопасности олокизумаба у пациентов, получавших препарат в дозе 240 мг к2н (480 мг в месяц) в течение 12 недель сопоставим с общим профилем безопасности у пациентов, получавших препарат в рекомендованной дозе.
Данные о передозировке у детей отсутствуют.
Взаимодействие с другими лекарственными средствами
Одновременное применение с метотрексатом не влияло на экспозицию олокизумаба. Не ожидается также влияния олокизумаба на экспозицию метотрексата при их одновременном применении, клинические данные отсутствуют. Во всех клинических исследованиях у пациентов с ревматоидным артритом олокизумаб применялся совместно с метотрексатом.
Специальные клинические исследования лекарственных взаимодействий олокизумаба не проводились. По результатам клинического исследования CREDO1 не сообщалось о случаях клинически значимых лекарственных взаимодействий олокизумаба с другими препаратами.
В исследовании in vitro на криоконсервированных гепатоцитах человека олокизумаб обращал ингибиторный эффект ИЛ-6 на активность CYP1A1/2, 2В6, 2С9, 3А4/5 и 2С19, а также на активность NTCP. Таким образом, следует принимать во внимание, что у пациентов с активным ревматоидным артритом может потребоваться коррекция доз препаратов, метаболизируемых данными изоформами CYP, после начала применения препарата Артлегиа.
Концентрация следующих препаратов может снизиться при совместном применении с препаратом Артлегиа (список не является исчерпывающим): статины (симвастатин, ловастатин, аторвастатин); оральные контрацептивы; блокаторы кальциевых каналов; глюкокортикоиды (дексаметазон, метилпреднизолон); варфарин; хинидин; теофиллин; тизанидин; фенитоин; пимозид; циклоспорин; сиролимус; такролимус; бензодиазепины (например, диазепам, алпразолам, триазолам, мидазолам, бромазепам).
Особые указания
Назначать лечение препаратом Артлегиа и наблюдать за ходом лечения разрешается врачам, имеющим опыт в диагностике и лечении ревматоидного артрита.
Анафилактические или анафилактоидные реакции: введение препаратов, содержащих белки, может быть связано с возникновением иммунологических/аллергических или неиммунологических реакций повышенной чувствительности к препарату, которые могут быть тяжелыми. Эти реакции могут возникать в виде острой инфузионной реакции, аллергической реакции или реакции гиперчувствительности замедленного типа. Таким образом, первое введение препарата Артлегиа следует выполнять в медицинском учреждении, где имеются лекарственные средства и оборудование для купирования анафилактических и анафилактоидных реакций. В клинических исследованиях был отмечен случай серьезной анафилактической реакции на введение препарата Артлегиа.
Инфекции: для пациентов, получающих иммуносупрессивные препараты, включая блокаторы сигнального пути ИЛ-6, характерна повышенная частота развития инфекций. Применение препарата Артлегиа связано с повышенным риском развития или активизацией инфекций. Не следует начинать терапию препаратом Артлегиа пациентам с инфекциями в активной фазе. Следует с осторожностью проводить лечение препаратом Артлегиа пациентов, имеющих факторы риска развития инфекций. При развитии серьезных инфекций терапию препаратом Артлегиа следует прекратить. Пациентов следует проинструктировать о возможных признаках и симптомах развития инфекции, требующих немедленного обращения к врачу.
Туберкулезная инфекция: перед началом терапии препаратом Артлегиа необходимо провести обследование пациента на наличие латентной формы туберкулезной инфекции. Пациентам с выявленной латентной формой туберкулезной инфекции перед началом терапии препаратом Артлегиа следует провести стандартный курс противотуберкулезной терапии.
Следует с осторожностью назначать препарат Артлегиа пациентам, находящимся в тесном контакте (совместное проживание или нахождение в других замкнутых пространствах, например, на рабочем месте, на общественных собраниях или в здании на протяжении длительных периодов в течение дня) с лицом, страдающим активным туберкулезом. Перед применением препарата Артлегиа у таких пациентов следует тщательно оценить соотношение риска и пользы применения препарата.
Риск перфорации желудочно-кишечного тракта: при применении ингибиторов сигнального пути ИЛ-6 известны случаи перфорации желудочно-кишечного тракта, в основном на фоне дивертикулита. Следует соблюдать осторожность при применении препарата Артлегиа у пациентов с дивертикулитом или перфорацией кишечника в анамнезе и другими факторами риска перфорации кишечника. При появлении желудочно-кишечных симптомов, таких как абдоминальная боль, на фоне лечения препаратом Артлегиа, следует незамедлительно провести обследование пациента.
Почечная недостаточность: пациентов с почечной недостаточностью не включали в клиническое исследование препарата Артлегиа. В связи с отсутствием данных следует соблюдать осторожность при применении препарата Артлегиа у пациентов с нарушениями функции почек.
Нарушения функции печени: применение препарата Артлегиа так же, как и других ингибиторов ИЛ-6, связано с повышением уровня АЛТ, ACT и гамма-глутамилтрансферазы (см. раздел «Повышение уровня печеночных трансаминаз»). Пациентов с уровнем АЛТ или ACT ≥1,5×ВГН не включали в клиническое исследование. Следует соблюдать осторожность при применении препарата Артлегиа у пациентов с нарушениями функции печени и печеночной недостаточностью.
Мониторинг лабораторных показателей крови: в клинических исследованиях было зарегистрировано снижение абсолютного числа нейтрофилов и лейкоцитов на фоне лечения препаратом Артлегиа и другими ингибиторами ИЛ-6. По данным применения других ингибиторов ИЛ-6, нейтропения на фоне лечения не приводила к повышению частоты инфекций. Пациентов с уровнем лейкоцитов 9 /л, уровнем нейтрофилов 6 /л ( Вакцинация: безопасность иммунизации живыми вакцинами на фоне применения ингибиторов ИЛ-6, в том числе олокизумаба, не установлена. Пациентов с необходимостью вакцинации живыми вакцинами не включали в клиническое исследование.
Злокачественные новообразования: данные о безопасности применения олокизумаба у пациентов со злокачественными новообразованиями отсутствуют, риск развития злокачественных опухолей на фоне терапии препаратом Артлегиа не известен.
Влияние на способность управлять транспортными средствами, механизмами
Исследования по изучению влияния препарата на способность управлять транспортными средствами и механизмами не проводились. Хотя на данный момент при терапии олокизумабом нежелательные реакции, связанные с головокружением, не отмечались, головокружение часто наблюдалось при терапии другими ингибиторами ИЛ-6. Пациентам, испытывающим головокружение во время терапии препаратом Артлегиа, следует рекомендовать не управлять транспортными средствами и механизмами до тех пор, пока головокружение не прекратится.
Форма выпуска
Раствор для подкожного введения, 160 мг/мл.
По 0,4 мл препарата во флаконах вместимостью 2 мл из стекла, укупоренных пробками из хлорбутилкаучука и герметизированные колпачками комбинированными алюминиевыми с пластмассовыми отщелкивающимися крышками.
По 1 флакону вместе с инструкцией по применению в картонную пачку.
Условия хранения
В защищённом от света месте при температуре от 2 до 8 °С.
Хранить в недоступном для детей месте.
Срок годности
Не использовать по истечении срока годности, указанного на упаковке.
Условия отпуска
Отпускают по рецепту.
Производитель
Российская Федерация, Ярославская обл., г.о.г. Ярославль, г. Ярославль, ул. Громова, д. 15.
Владелец регистрационного удостоверения/ Организация, принимающая претензии от потребителей:
АО «Р-Фарм», Россия
123154, г. Москва, ул. Берзарина, д. 19, корп. 1