аттенуированный вирус что это
Аттенуированный вирус что это
Вакцины — иммунобиологические препараты, предназначенные для активной иммунопрофилактики, то есть для создания активной специфической невосприимчивости организма к конкретному возбудителю. Вакцинация признана ВОЗ идеальным методом профилактики инфекционных заболеваний человека. Высокая эффективность, простота, возможность широкого охвата вакцинируемых лиц с целью массового предупреждения заболевания вывели активную иммунопрофилактику в большинстве стран мира в разряд государственных приоритетов. Комплекс мероприятий по вакцинации включает отбор лиц, подлежащих вакцинации, выбор вакцинного препарата и определение схемы его использования, а также (при необходимости) контроль эффективности, купирование возможных патологических реакций и осложнений. В качестве Аг в вакцинных препаратах выступают:
• цельные микробные тела (живые или убитые);
• отдельные Аг микроорганизмов (наиболее часто протективные Аг);
• токсины микроорганизмов;
• искусственно созданные Аг микроорганизмов;
• Аг, полученные методами генной инженерии.
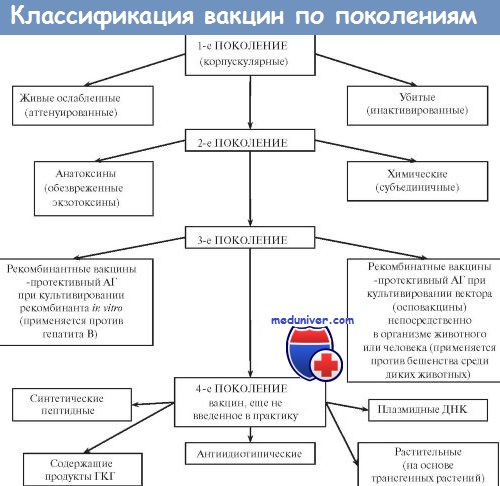
Большинство вакцин разделяют на живые, инактивированные (убитые, неживые), молекулярные (анатоксины) генно инженерные и химические; по наличию полного или неполного набора Аг — на корпускулярные и компонентные, а по способности вырабатывать невосприимчивость к одному или нескольким возбудителям — на моно- и ассоциированные.
Живые вакцины
Живые вакцины — препараты из аттенуированных (ослабленных) либо генетически изменённых патогенных микроорганизмов, а также близкородственных микробов, способных индуцировать невосприимчивость к патогенному виду (в последнем случае речь идёт о так называемых дивергентных вакцинах). Поскольку все живые вакцины содержат микробные тела, то их относят к группе корпускулярных вакцинных препаратов.
Иммунизация живой вакциной приводит к развитию вакцинального процесса, протекающего у большинства привитых без видимых клинических проявлений. Основное достоинство живых вакцин— полностью сохранённый набор Аг возбудителя, что обеспечивает развитие длительной невосприимчивости даже после однократной иммунизации. Живые вакцины обладают и рядом недостатков. Наиболее характерный — риск развития манифестной инфекции в результате снижения аттенуации вакцинного штамма. Подобные явления более типичны для противовирусных вакцин (например, живая полиомиелитная вакцина в редких случаях может вызвать полиомиелит вплоть до развития поражения спинного мозга и паралича).
Ослабленные ( аттенуированные ) вакцины
Ослабленные (аттенуированные) вакцины изготавливают из микроорганизмов с пониженной патогенностью, но выраженной иммуногенностью. Введение вакцинного штамма в организм имитирует инфекционный процесс: микроорганизм размножается, вызывая развитие иммунных реакций. Наиболее известны вакцины для профилактики сибирской язвы, бруцеллёза, Ку-лихорадки, брюшного тифа. Однако большая часть живых вакцин — противовирусные. Наиболее известны вакцина против возбудителя жёлтой лихорадки, противополи-омиелитная вакцина Сэйбина, вакцины против гриппа, кори, краснухи, паротита и аденовирусных инфекций.
Дивергентные вакцины
В качестве вакцинных штаммов используют микроорганизмы, находящиеся в близком родстве с возбудителями инфекционных болезней. Аг таких микроорганизмов индуцируют иммунный ответ, перекрёстно направленный на Аг возбудителя. Наиболее известны и длительно применяются вакцина против натуральной оспы (из вируса коровьей оспы) и БЦЖ для профилактики туберкулёза (из микобактерий бычьего туберкулёза).
АТТЕНУАЦИЯ
АТТЕНУАЦИЯ (латинский attenuatio уменьшение, ослабление) — стойкое необратимое ослабление вирулентности патогенных микроорганизмов. Впервые аттенуированные штаммы микроорганизмов были получены Л. Пастером (1880), применившим их в качестве вакцинных для борьбы с куриной холерой, сибирской язвой и бешенством. Аттенуированные штаммы микроорганизмов нашли широкое применение при изготовлении живых вакцин против чумы, туляремии, бруцеллеза, сибирской язвы, туберкулеза, бешенства, гриппа, желтой лихорадки, кори, полиомиелита, Ку-лихорадки и пр. (см. Вакцины).
При получении аттенуированных штатов обычно используют длительные пассажи на животных, в частности, резистентных к возбудителю, в культуре ткани и в питательных средах при измененной температуре или при добавлении в среду сапонина, желчи, антибиотиков и других веществ. Значительно быстрее можно получать аттенуированные штаммы путем обработки микроорганизмов мутагенами с последующей селекцией клонов, обладающих сниженной вирулентностью. Аттенуированные штаммы встречаются также среди микроорганизмов, циркулирующих в природе.
Механизм аттенуации связан с селекцией в процессе пассажей мутантов, обладающих сниженной вирулентностью, однако образующаяся популяция обычно генетически гетерогенна и содержит как аттенуированные микроорганизмы, так и сохранившие вирулентность. Поэтому важным заключительным этапом получения аттенуированных штаммов является клонирование, то есть выделение из образующейся популяции микроорганизмов клонов, обладающих наиболее сниженной вирулентностью, с последующим приготовлением из таких клонов генетически однородной популяции. Примерами получения аттенуированных штаммов может служить получение штаммов: вируса бешенства (путем пассажей через организм кролика), туберкулезных бактерий БЦЖ (путем их пассирования в течение 13 лет на среде из глицеринового картофеля с добавлением желчи) и вируса желтой лихорадки (при пассажах вируса в куриных эмбрионах и культуре ткани).
Применение живых вакцин из аттенуированных штаммов микроорганизмов требует постоянного контроля стабильности наследственных свойств и генетической однородности популяции.
Аттенуированный вирус что это
Все вирусные популяции характеризуются генетическим полиморфизмом, в основе которого лежат спонтанные мутации как результат ошибок при считывании вирусного генома в процессе репликации.
Спонтанные мутации ответственны за фенотипические изменения различных свойств вируса, в том числе вирулентности. В природе вирусы в процессе передачи от хозяина к хозяину совершают множество циклов репродукции. В этот период постоянно генерируются спонтанные мутации, которые могут вызывать изменения свойств вируса. В организме природного хозяина селекционируются преимущественно вирулентные вирусные частицы, которые способны передаваться серийно восприимчивым организмам.
Адаптация вирусов к неестественным условиям репродукции сопровождается прогрессирующей селекцией спонтанных мутантов адекватно новым условиям размножения.
Вирулентность вируса может быть снижена разными путями, в том числе пассированием в культурах клеток особенно неестественного хозяина. При этом преимущественно накапливаются мутанты, которые размножаются быстрее, чем полевой вирус. Затем такие мутанты селекционируют и определяют пригодность для использования в качестве живой вакцины. Аттенуированные мутанты часто являются пригодными в качестве живых вакцин потому, что они не долго размножаются в организме естественного хозяина и в то же время часто вызывают выраженный иммунный ответ.
У РНК-вирусов защитный механизм считывания генетической информации менее эффективен, чем у ДНК-вирусов. Они обладают значительно более высокой скоростью мутации, не менее чем в 100 раз, чем ДНК-вирусы ДНК-вирусы генетически более стабильны и труднее адаптируются. Частота ошибок у РНК-зависимых полимераз значительно выше, чем у ДНК-зависимых полимераз. На 10 000 оснований РНК-вирусов приходиться примерно одна мутация. РНК-полимераза коронавирусов может привести примерно к трем редким мутациям вируса на каждые 30 кb генома в процессе репродукции. Нелетальные мутанты РНК-вирусов накапливаются достаточно быстро. Гены, кодирующие разные белки, изменяются с разной скоростью.
Классическая аттенуация вирусов связана с селекцией спонтанных мутантов с пониженной вирулентностью. Идеально, аттенуация вирусных штаммов не должна сопровождаться потерей способности удовлетворительно размножаться в организме естественного хозяина, изменением антигенности и потерей протективных свойств.
Генетические мутации наиболее часто сопровождаются заменой единичных нуклеотидов (точечные, миссенс мутации). Реже мутации связаны с делецией или инсерцией единичных нуклеотидов или блоков нуклеотидов. Фенотипическая экспрессия мутаций может проявляться изменением различных свойств вируса.
Точечные мутации, сопровождающиеся специфическими аминокислотными заменами, в кодируемых вирусом белках могут снижать их функцию in vivo и тем самым вызывать аттенуацию вируса для хозяина. По уровню аттенуации и их потенциальной полезности для живых вирусных вакцин различают три класса точечных мутаций: чувствительные к температуре (ts мутанты); зависящие от протеолитического расщепления (Ра мутанты) и с измененным тканевым (клеточным) тропизмом.
Ts мутанты обычно являются условно летальными вирусами, которые эффективно размножаются при 32—34°С. Аттенуирующие ts мутации идентифицированы в большинстве, если не во всех генах вирусов; ts мутацию можно вызвать почти в любом гене. Ts мутанты особенно пригодны для иммунизации людей против респираторных вирусных болезней. Они хорошо размножаются в верхнем отделе респираторного тракта человека (32—34°С) и плохо — в нижнем (37°С).
Обнаружение ts мутантов (неспособных удовлетворительно размножаться при температуре несколько выше, чем нормальная температура тела) обычно отражает снижение вирулентности и указывает на возможность их использования в качестве живой вакцины. Однако, даже вакцины, содержащие более чем одну мутацию, доставляют беспокойство, связанное с возможностью восстановления вирулентности в процессе размножения в привитом организме.
Вакцинные штаммы полиовируса являются температурочувствительными со значительно сниженной способностью к размножению и нейровирулентностью для обезьян при введении в спиной мозг. Однако такие штаммы хорошо размножаются в кишечнике вакцинированных животных и могут вызывать виремию, и создают иммунитет. Хотя вакцинный вирус выделяется с фекалиями, контактная передача чувствительным организмом происходит очень редко.
Аттенуация путем адаптации вируса к размножению при пониженной температуре приводит к получению холодоадаптированных (Са) мутантов. К Са мутантам относятся безопасные вакцинные штаммы для интраназального применения, т.к. они хорошо размножаются при пониженной температуре носовой полости (около 33°С у большинства видов млекопитающих), но не при температуре низлежащих респираторных путей и легких. Холодоадаптированные вакцинные штаммы против гриппа, содержащие мутации почти в каждом гене, не давали реверсии. В 1997 году вакцину против гриппа людей, основанную на таких мутациях, использовали в США. Са мутанты успешно использовали при создании живых вакцин против ряда вирусных болезней животных.
Ра мутанты играют важную роль в аттенуации вирусов, инфекционность которых зависит от протеолиза структурного белка.
Известно, что протеолитическое расщепление парамиксовирусов необходимо для активации инфекционности и играет важную роль в проявлении тканевого тропизма и патогенности. Трипсин-подобные ферменты, присутствующие в клетках хозяина, требуются для расщепления предшественника белка сплавления FO на две субъединицы F1 и F2. Ра мутанты устойчивые к активации трипсином, оказывались аттенуированными.
Протеолитическое расщепление ГА вируса гриппа клеточными протеазами является важным для инфекционности вирусного потомства. В культуре клеток куринного эмбриона не происходит расщепления гемагглютинина.
Точечные мутации могут сочетаться с делеционными мутациями.
Национальный Фармацевтический журнал
Войти на сайт
ВАКЦИНЫ ПРОТИВ COVID-19 И АДЪЮВАНТЫ, УЛУЧШАЮЩИЕ ИХ СВОЙСТВА.

Новый адъювант для профилактических вакцин компании SEPPIC

• вакцины на основе цельного (полногеномного) ослабленного вируса;
• инактивированные вакцины на основе полностью нежизнеспособного вируса;
• векторные вакцины;
• генетические вакцины (ДНК и РНК вакцины);
• субъединичные вакцины на основе отдельных компонентов патогена, таких как белки, пептиды или генетический материал (например, белковые или рекомбинантные вакцины). Разработчики из различных стран на основании накопленных знаний и имеющихся у них результатов и методов исследований выбирают для разработки тот тип вакцины, который считают наиболее действенным для обеспечения эффективной защиты людей от вируса SARS-CoV-2 (Рис.1).
На настоящий момент среди вакцин-кандидатов против COVID-19, зарегистрированных в списке ВОЗ, можно найти практически все из вышеназванных типов вакцин. Коротко напомним, что представляет собой каждый из них и чем они отличаются друг от друга.

Векторные вакцины – это также вакцины на основе живых вирусов, однако здесь есть небольшой, но очень важный нюанс: это вакцины на основе хорошо изученных и достаточно безобидных для человека вирусов («векторов» или вспомогательных транспортных вирусов) с встроенными в них фрагментами генома «злого вируса» (Рис. 3). В случае векторных вакцин в геном хорошо изученного и, в целом, безобидного вируса, например, аденовируса («вектора»), путём генетических модификаций встраивается небольшой ген – участок генома SARS-CoV-2. При вводе в организм такой векторной вакцины генетически модифицированные вспомогательные вирусы провоцируют такой же сильный иммунный ответ на белки-антигены SARS-CoV-2, как в случае «живой» полногеномной вирусной вакцины.
Преимущество указанных вакцин, по замыслу разработчиков, в той же высокой эффективности, что и у вакцин на основе живых ослабленных вирусов, но в большей управляемости в связи с достаточной изученностью и предсказуемостью «вектора»-носителя. Векторные вакцины начали разрабатываться и изучаться относительно недавно, поэтому к массовому применению вакцин этого типа ученые также подходят с должной и необходимой осторожностью.

Еще два перспективных типа вакцин против COVID-19, разрабатываемые мировым сообществом, – вакцины на основе нуклеиновых кислот, а именно, ДНК- и РНК-вакцины. В случае ДНК-вакцины нуклеотидная последовательность, кодирующая антиген SARS-CoV-2, встраивается в вектор – бактериальную плазмиду – небольшую стабильную кольцевую молекулу ДНК, способную к автономной репликации. Сама по себе плазмида не вызывает нужного специфического иммунного ответа, для этого, собственно, в неё и вшивают гены иммуногенных белков. Указанный модифицированный геном направляется в клетку, встраивается в ее ядро и образует вирусный белок (антиген), индуцирующий иммунный ответ.
Согласно замыслу разработчиков, ДНК-вакцины не могут вызвать заражение SARS-Cov-2, однако иммунитет, который они обусловливают, должен оказаться таким же сильным, как в случае «живых» вакцин. Тем не менее, влияние ДНК-вакцин на живые организмы изучено еще в меньшей степени, чем влияние векторных вакцин, поэтому вряд ли в ближайшее время ДНК-вакцины будут допущены к массовому применению на людях. 
В случае применения РНК-вакцины получается двойной иммунный ответ: с одной стороны, выработку антител вызывают вирусные белки, с другой стороны, сами липидные частицы с мРНК могут стимулировать иммунный ответ, так как «похожи на вирус» и воспринимаются организмом соответственно. Разработчики предполагают, что при вакцинации РНК-вакцинами из-за их «двойного действия» в организме быстро возникнет сильный и стойкий иммунитет.
В случае генетических вакцин преимуществом является их относительно быстрое и экономически выгодное производство: небольшую молекулу мРНК можно довольно быстро воссоздать, наработка нужного антигена обойдется недорого. Это делает вакцину доступной широким массам. Тем не менее иммунологи очень осторожно относятся к РНК-вакцинам, так как из-за малого периода их изучения никто не знает наверняка, как именно мРНК будет вести себя в живом, особенно в репродуктивном, организме.

Одним из самых безопасных типов вакцин в настоящее время считаются субъединичные вакцины, то есть вакцины на основе белков или фрагментов вируса (Рис. 6), не имеющих в своем составе ни ДНК, ни РНК как, например, белковые вакцины.
Попадая в организм при вакцинации, смесь фрагментов вирусных белков-антигенов также способна вызывать иммунный ответ. При этом такая вакцина абсолютно безопасна, здесь невозможны мутации вируса, поэтому вызвать у человека заболевание COVID-19 такая вакцина не может. Недостатком субъединичных вакцин является довольно длительный и сложный процесс наработки и очистки – получить достаточное для вакцинации очищенное количество вирусного белка не так легко. Кроме того, в чистом виде белковые вакцины не вызывают сильный иммунный ответ, поэтому недостаточно эффективны. В связи с этим при разработке белковых вакцин очень важно:
а) усилить иммунный ответ, вводя в состав белковых вакцин соединения, усиливающие их эффективность (эти вещества называют адъюванты),
б) увеличить количество нарабатываемой вакцины также за счет добавления к наработанному вирусному белку существенного количества того же адъюванта.

Наконец, мы подошли к еще одному безопасному и перспективному типу вакцин – инактивированным вакцинам. Здесь так же, как и в случае «живых» вакцин на основе ослабленного вируса используется цельный геном SARS-Cov-2, но в случае инактивированных вакцин вирус полностью деактивирован либо высокой температурой, либо дезинфицирующими составами, либо определенным видом излучения, что делает его совершенно нежизнеспособным. Этот инактивированный вирус никогда не сможет инфицировать клетку. Тем не менее по структуре «неживой» инактивированный вирус остается полным аналогом «живого» вируса и поэтому вызывает в организме иммунный ответ. Проблема в том, что в чистом виде инактивированные вирусы индуцируют существенно более низкий иммунный ответ, нежели живые, пусть даже и ослабленные вирусы. В связи с этим в составах инактивированных вакцин так же, как и в случае субъединичных вакцин используют адъюванты – вещества, которые значительно усиливают иммунный ответ, делая эти вакцины схожими по эффективности с живыми.
Основываясь на вышесказанном, мы склоняемся к выводу, что наиболее безопасными для человека являются субъединичные и инактивированные вакцины. Для повышения эффективности указанных безопасных вакцин до уровня более иммуногенных «живых», векторных или генетических вакцин необходимо применение в их составах современных адъювантов. Что же такое адъюванты и какова их роль в вакцинах?

Адъювант (от лат. adjuvans – «помогающий, поддерживающий») – соединение или комплекс веществ, используемых для усиления иммунного ответа при введении одновременно с антигеном.
Адъюванты на протяжении десятилетий применяются для улучшения иммунного ответа на вакцинные антигены. Включение адъювантов в состав вакцин направлено на усиление, ускорение и продление специфического иммунного ответа до желаемого уровня. Таким образом, адъюванты играют ключевую роль в получении эффективного и длительного иммунитета.
Использование адъювантов в вакцинах позволяет:
• Усилить краткосрочный иммунный ответ;
• Увеличить продолжительность иммунитета, то есть сократить частоту требуемых бустерных иммунизаций;
• Направить иммунный ответ (гуморальный или клеточный иммунитет);
• Уменьшить антигенную нагрузку при сохранении эффективности вакцины;
• Улучшить иммунный ответ у ослабленных или иммунокомпроментированных вакцинируемых лиц;
• Снизить себестоимость вакцины;
• Повысить стабильность вакцины.
Интерес к адъювантам для вакцин резко возрос в 2000-е годы. Ведущие фармацевтические компании-производители путем применения адъювантов разработали более эффективные и безопасные вакцины против гриппа.
В последние годы появляется все больше и больше новых вакцин-кандидатов как для профилактики инфекционных заболеваний, так и для терапии самых тяжелых заболеваний человечества. В связи с низкой иммуногенностью таких вакцин во многих случаях требуется введение в их состав адъювантов. Новые достижения в области аналитической биохимии, очистке макромолекул, технологии рекомбинантной ДНК, улучшенное понимание иммунологических механизмов и патогенеза заболевания позволили улучшить техническую основу разработки и применения адъювантов.
В настоящее время известно довольно много эффективных адъювантов, которые классифицируются по природе происхождения, механизму действия и физическим или химическим свойствам.
Так, в современных вакцинах широко применяются гели гидроксида алюминия, фосфаты алюминия или кальция, препараты на основе масляных эмульсий и ПАВ, дисперсные адъюванты, например, виросомы, структурные комплексы сапонинов и липидов и многие другие типы адъювантов.
Как уже упоминалось выше, наиболее эффективно и поэтому чаще всего адъюванты используются в следующих категориях вакцин:
• вакцины на основе белков (рекомбинантные субъединичные);
• инактивированные;
• векторные вакцины (для уменьшения дозы).
Для каждой вакцины адъювант подбирается таким образом, чтобы получить оптимальное соотношение эффективности указанной вакцины (получение сильного и продолжительного иммунного ответа) и ее безопасности для человека (минимальная реактогенность и отсутствие побочных эффектов).
К сожалению, немаловажным аспектом уже зарегистрированных в настоящее время адъювантов является их недоступность широкому кругу разработчиков. Практически все имеющиеся на настоящий момент современные адъюванты, применяемые в профилактических вакцинах, за исключением соединений алюминия, являются собственностью крупнейших фармацевтических компаний (см. табл. 2). В первую очередь, к ним относятся адъюванты для приготовления эмульсионных вакцин. Эти адъюванты на настоящий момент считаются наиболее перспективными в профилактических вакцинах, но остаются при этом и наименее доступными, так как были специально разработаны крупными биофармацевтическими компаниями исключительно для вакцин собственного производства.
Эти недоступные широкому кругу разработчиков адъюванты ведущих фармацевтических компаний отлично зарекомендовали себя в составах готовых вакцин указанных производителей. К примеру, эмульсионные адъюванты масло-в-воде MF59, AS03 и AF03 продемонстрировали высокую эффективность в вакцинах против гриппа. Сегодня вакцинами на их основе провакцинировано >120 миллионов человек, их профиль безопасности и иммуногенности тщательно и глубоко изучен и подтвержден на значительном количестве клинических испытаний (см. табл. 3).

Франсуа Бертран, руководитель направления разработки и производства адъювантов компании Seppic, в своем выступлении по поводу выпуска адъюванта SEPIVAC TM SWE на мировой рынок сказал: «Указанная разработка иллюстрирует наше общее стремление привнести готовый эффективный и общедоступный адъювант в мировое сообщество разработчиков вакцин. Мы твердо верим, что SEPIVAC TM SWE ускорит разработку новых профилактических вакцин для людей и будет способствовать более здоровому будущему человечества во всем мире».