авелокс или азитромицин что лучше
НОВЫЕ ФТОРХИНОЛОНЫ: новые возможности лечения внебольничной пневмонии
Инфекции дыхательных путей по частоте возникновения занимают первое место среди инфекционных заболеваний человека. Несмотря на наличие в арсенале врача большого количества антибактериальных препаратов разных классов, в последние годы наблюдается отчетлив
Инфекции дыхательных путей по частоте возникновения занимают первое место среди инфекционных заболеваний человека. Несмотря на наличие в арсенале врача большого количества антибактериальных препаратов разных классов, в последние годы наблюдается отчетливая тенденция к увеличению смертности от пневмонии во всех развитых странах мира. Причина может быть связана прежде всего с ростом резистентности основных возбудителей внебольничных инфекций дыхательных путей ко многим антибактериальным препаратам. Этим объясняется интерес клиницистов к новым антибактериальным средствам, к которым отмечается меньший уровень резистентности бактерий.
Этиология внебольничной пневмонии непосредственно связана с нормальной микрофлорой «нестерильных» верхних отделов дыхательных путей (полости рта, носа, рото- и носоглотки). Из множества видов микроорганизмов, колонизующих верхние отделы дыхательных путей, лишь некоторые, обладающие повышенной вирулентностью, проникая в нижние дыхательные пути, способны вызывать воспалительную реакцию даже при минимальных нарушениях защитных механизмов. Такими типичными бактериальными возбудителями внебольничной пневмонии являются следующие перечисленные ниже микроорганизмы.
Streptococcus pneumoniae — самый частый возбудитель внебольничной пневмонии у лиц всех возрастных групп (30-50%). Наиболее остро в настоящее время стоит проблема распространения среди пневмококков пенициллинрезистентных штаммов. В некоторых странах частота устойчивости пневмококков к пенициллину может достигать 60%. Масштабных исследований распространения резистентности пневмококков к пенициллину в нашей стране не проводилось. По данным локальных исследований в Москве, частота устойчивых штаммов составляет 2%, штаммов с промежуточной чувствительностью — около 20%. Устойчивость пневмококков к пенициллину связана не с продукцией β-лактамаз, а с модификацией мишени действия антибиотика в микробной клетке — пенициллинсвязывающих белков, поэтому ингибитор-защищенные пенициллины в отношении этих пневмококков также неактивны. Устойчивость пневмококков к пенициллину обычно ассоциируется с устойчивостью к цефалоспоринам I-II поколений, макролидам, тетрациклинам, ко-тримоксазолу.
Haemophilus influenzae — второй по частоте возбудитель (10-20%), особенно у лиц, страдающих хроническими обструктивными болезнями легких, а также у курильщиков; высокой природной активностью в отношении гемофильной палочки обладают аминопенициллины, амоксициллин/клавуланат, цефалоспорины II-IV поколений, карбапенемы, фторхинолоны. Основной механизм резистентности H. influenzae связан с продукцией β-лактамаз.
Staphylococcus aureus — нечастый возбудитель пневмонии (около 5%), наиболее опасен для пожилых людей, наркоманов, алкоголиков, после перенесенного гриппа. Препаратами выбора при стафилококковых пневмониях являются оксациллин, также активны амоксициллин/клавуланат, цефалоспорины, фторхинолоны.
Klebsiella pneumoniae — редкий возбудитель внебольничной пневмонии (менее 5%), встречается, как правило, у больных с тяжелыми сопутствующими заболеваниями (сахарный диабет, застойная сердечная недостаточность, цирроз печени и др.). Наиболее высокой природной активностью в отношении этого возбудителя обладают цефалоспорины III-IV поколений, карбапенемы, фторхинолоны.
Определенное значение в этиологии пневмонии имеют также два других микроорганизма, характеризующихся особыми биологическими свойствами и внутриклеточной локализацией в макроорганизме — Micoplasma pneumoniae и Chlamidia pneumoniae. В отношении этих микроорганизмов клинически неэффективны все β-лактамные антибиотики. Наибольшей природной активностью обладают макролиды и тетрациклины, несколько менее активны ранние фторхинолоны.
В настоящее время в качестве основных средств стартовой терапии внебольничной пневмонии в амбулаторной практике обычно рекомендуются аминопенициллины (ампициллин, амоксициллин), защищенные аминопенициллины (амоксициллин/клавуланат), пероральные цефалоспорины II поколения (цефуроксим аксетил), макролиды (эритромицин, кларитромицин, рокситромицин, азитромицин, спирамицин, мидекамицин). При тяжелом течении пневмонии у госпитализированных больных целесообразно применение парентеральных цефалоспоринов III поколения или фторхинолонов. Клиническая эффективность всех указанных препаратов примерно одинакова, однако при лечении внебольничной пневмонии ни один из этих антибиотиков не может считаться идеальным.
Аминопенициллины характеризуются высокой природной активностью в отношении S. pneumoniae (амоксициллин более высокой, чем ампициллин), однако о проблемах, связанных с возрастающим распространением пенициллинрезистентных пневмококков, упоминалось выше. Имеются данные, что амоксициллин пока сохраняет клиническую эффективность в отношении штаммов пневмококка с промежуточной чувствительностью, а также в отношении устойчивых штаммов. Однако можно предположить снижение клинической эффективности амоксициллина при выделении штаммов пневмококка с высоким уровнем резистентности. Аминопенициллины неэффективны при пневмонии, вызванной S. aureus и K. pneumoniae.
Назначение амоксициллина/клавуланата и цефуроксима аксетила предусмотрено большинством международных и отечественных стандартов лечения внебольничной пневмонии ввиду высокой активности против пневмококков, гемофильной палочки, стафилококков. Однако в отношении пенициллинрезистентных пневмококков мы сталкиваемся с теми же проблемами, что и у аминопенициллинов.
Следует подчеркнуть, что все пенициллины и цефалоспорины неактивны в отношении микоплазм, а также хламидий, и поэтому клинически неэффективны при атипичных пневмониях.
Макролидные антибиотики проявляют высокую природную активность в отношении пневмококков, стафилококков, микоплазм, хламидий и низкую — в отношении гемофильной палочки. Однако в последние годы во всех регионах мира, в том числе и в нашей стране, отмечается неуклонная тенденция повышения устойчивости пневмококков к макролидам. Резистентность пневмококков обычно ассоциируется с неуспехом терапии макролидами. Следует отметить, что новые полусинтетические макролиды не имеют преимуществ перед эритромицином, когда речь идет об устойчивых штаммах пневмококков. В последние годы значение макролидов при внебольничной пневмонии пересматривается. По всей видимости, эти препараты могут быть рекомендованы только в случае нетяжелой пневмонии при подозрении на атипичную этиологию.
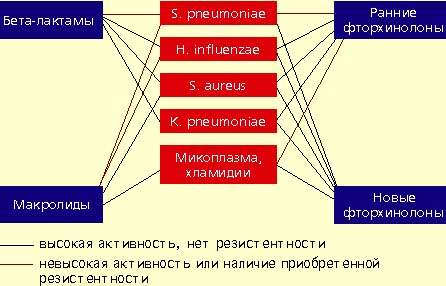 |
| Антимикробная активность бета-лактамов, макролидов и фторхинолонов в отношении наиболее значимых возбудителей внебольничной пневмонии |
Фторхинолоны обладают широким спектром антимикробной активности. Эти препараты проявляют природную активность в отношении практически всех потенциальных возбудителей внебольничной пневмонии. Однако применение ранних фторхинолонов (ципрофлоксацин, офлоксацин, пефлоксацин) при внебольничной пневмонии было ограничено из-за их слабой природной активности в отношении основного возбудителя пневмонии — S. pneumoniae. Значения минимальных подавляющих концентраций (МПК) ранних фторхинолонов в отношении пневмококков составляют от 4 до 8 мкг/мл, а их концентрация в бронхолегочной ткани значительно ниже, что недостаточно для успешной терапии. Описаны случаи, когда терапия фторхинолонами при пневмококковой пневмонии не приносила успеха.
Определенные перспективы лечения внебольничной пневмонии связаны с появлением в последние годы препаратов нового поколения фторхинолонов, которые характеризуются более высокой активностью в отношении S. pneumoniae. Современная классификация фторхинолонов представлена в таблице.
Первым препаратом нового поколения фторхинолонов является левофлоксацин, представляющий собой левовращающий изомер офлоксацина. Левофлоксацин характеризуется более высокой активностью против пневмококков (МПК = 2 мкг/мл) по сравнению с офлоксацином и ципрофлоксацином, причем препарат сохраняет активность и в отношении пенициллинрезистентных штаммов S. pneumoniae. Левофлоксацин — это первый и пока единственный антибактериальный препарат, который официально рекомендован в США для лечения пневмонии, вызванной пенициллинрезистентными пневмококками. Среди новых фторхинолонов только левофлоксацин выпускается в двух лекарственных формах — для приема внутрь и для внутривенного введения. Поэтому левофлоксацин может применяться не только в амбулаторной практике, но и при тяжелых пневмониях у госпитализированных больных. В большом количестве клинических исследований показана высокая эффективность левофлоксацина при внебольничной пневмонии в дозе 500 мг, вводимой однократно в сутки. К несомненным достоинствам левофлоксацина можно отнести его хорошую переносимость.
Вторым препаратом нового поколения фторхинолонов, внедренным в клиническую практику, был спарфлоксацин. Он зарегистрирован в нашей стране и выпускается только в пероральной форме. Однако наряду с доказанной высокой клинической эффективностью следует отметить ряд нежелательных эффектов, отмеченных при его применении. Прежде всего речь идет о существенной фототоксичности спарфлоксацина (т. е. повышенной чувствительности кожи к ультрафиолету); по некоторым данным, частота возникновения этого нежелательного явления составляет более 10%. Фототоксичность характерна для всех препаратов класса фторхинолонов, однако при использовании других препаратов этой группы (например, левофлоксацина, офлоксацина, ципрофлоксацина) это побочное явление возникает гораздо реже. К другим достаточно серьезным нежелательным явлениям, связанным с приемом спарфлоксацина, относится удлинение интервала QT на ЭКГ, что может сопровождаться появлением желудочковых аритмий, иногда опасных для жизни. Клиническое значение этого феномена до конца не ясно, однако известен факт отзыва с рынка препарата этого класса (грепафлоксацина) именно по данной причине. Таким образом, спарфлоксацин, по всей видимости, не может быть рекомендован для рутинного применения в амбулаторной практике при пневмонии, учитывая наличие других, более безопасных препаратов этой группы.
Последним зарегистрированным в нашей стране новым фторхинолоном является моксифлоксацин. Пока он существует только для перорального приема, однако в следующем году ожидается появление в клинической практике парентеральной лекарственной формы. Моксифлоксацин характеризуется очень высокой природной активностью в отношении пневмококков (МПК = 0,25 мкг/мл), в том числе пенициллинрезистентных штаммов, а также более высокой активностью (по сравнению с ранними фторхинолонами) в отношении микоплазм и хламидий. Моксифлоксацин в суточной дозе 400 мг (однократно) показал высокую клиническую эффективность и хорошую переносимость при внебольничной пневмонии. В контролируемых исследованиях не отмечено клинически значимого удлинения интервала QT и существенной фототоксичности.
Ряд перспективных препаратов нового поколения фторхинолонов в настоящее время проходят стадию клинического изучения. В 2001 году ожидается разрешение клинического применения в России еще двух препаратов этой группы — гемифлоксацина и гатифлоксацина.
Почему азитромицин остается препаратом выбора при внебольничных инфекциях нижних дыхательных путей
Инфекционно-воспалительные заболевания дыхательных путей занимают первое место в структуре инфекционной патологии. Пневмония является наиболее частой инфекционной причиной смерти в мире.
Инфекционно-воспалительные заболевания дыхательных путей занимают первое место в структуре инфекционной патологии. Пневмония является наиболее частой инфекционной причиной смерти в мире. В России ежегодно около 1,5 млн человек переносят пневмонию. В связи с этим остается актуальной проблема рационального выбора антибактериального средства для лечения инфекций нижних дыхательных путей. Выбор препарата для антибактериальной терапии должен основываться на его спектре действия, охватывающем выделенный или предполагаемый возбудитель, чувствительный к данному антибиотику, фармакокинетических свойствах антибактериального средства, обеспечивающих его проникновение в терапевтической концентрации в соответствующие ткани, клетки и жидкости организма, данных о безопасности антибиотика (побочных эффектах, противопоказаниях и возможном нежелательном взаимодействии с другими лекарствами), характеристиках лекарственной формы, способе введения и режиме дозирования, обеспечивающих высокий комплаенс терапии, фармакоэкономических аспектах лечения [4, 6, 8].
Инфекции нижних дыхательных путей и принципы выбора антибиотика
При неспецифических внебольничных инфекциях выбор антибактериального препарата в большинстве случаев основывается на статистических данных о наиболее частых их возбудителях, а также сведениях о подтвержденной в контролируемых клинических исследованиях эффективности тех или иных антибиотиков при инфекциях известной этиологии. Вынужденно эмпирический подход к лечению связан с отсутствием возможности микробиологического исследования в амбулаторных лечебных учреждениях, длительностью бактериологической идентификации возбудителя и определения его чувствительности к антибиотикам (3–5 дней, а в случае «атипичных» патогенов и больше), невозможностью в ряде случаев получить биологический материал для посева или бактериоскопии (например, около 30% больных пневмониями имеют непродуктивный кашель, что не позволяет исследовать мокроту), трудностями в разграничении истинных возбудителей и сапрофитов (обычно микроорганизмов ротоглотки, попадающих в исследуемый материал). Сложности выбора лекарственного средства в амбулаторных условиях определяются также отсутствием полноценного наблюдения за течением заболевания и, следовательно, своевременной коррекции лечения при его неэффективности. Антибиотики по-разному проникают в различные ткани и биологические жидкости. Лишь некоторые из них хорошо проникают в клетку (макролиды, тетрациклины, фторхинолоны, в меньшей степени — клиндамицин и сульфаниламиды). Поэтому, даже если препарат in vitro проявляет высокую активность в отношении данного возбудителя, но не достигает в месте его локализации уровня, превышающего минимальную подавляющую концентрацию (МПК) для данного микроорганизма, клинического эффекта он не окажет, хотя микробная резистентность к нему будет вырабатываться. Не менее важным аспектом антибактериальной терапии является ее безопасность, особенно для амбулаторного больного, лишенного повседневного медицинского наблюдения. В амбулаторных условиях следует отдавать предпочтение пероральному приему антибиотиков. В педиатрической практике имеют значение органолептические свойства препарата. Для повышения исполняемости пациентом врачебных назначений режим дозирования антибиотика должен быть максимально простым, т. е. предпочтительнее препараты с минимальной кратностью приема и коротким курсом лечения.
Возбудители неспецифических внебольничных инфекций нижних дыхательных путей
Острые респираторные вирусные инфекции (ОРВИ), протекающие с синдромом бронхита, в ряде случаев, чаще в детском возрасте, могут осложняться присоединением бактериальной флоры с развитием острого бронхита. Возбудителями острого бактериального бронхита в детском возрасте являются пневмококк, микоплазма или хламидия, реже гемофильная палочка, моракселла или стафилококк. Острый бактериальный бронхиолит у детей вызывают моракселла, микоплазма и возбудитель коклюша. Острый гнойный трахеобронхит у взрослых в 50% случаев вызывает гемофильная палочка, в остальных случаях пневмококк, реже моракселла (5–8% случаев) или внутриклеточные микроорганизмы (5% случаев).
Среди бактериальных возбудителей обострений хронического бронхита главную роль играют Haеmophilus influenzae (30–70% случаев), Streptococcus pneumoniae и Moraxella catarrhalis. Для курильщиков наиболее характерна ассоциация H. influenzae и M. catarrhalis. В отягощенных клинических ситуациях (возраст старше 65 лет, многолетнее течение болезни — более 10 лет, частые обострения — более 4 раз в год, сопутствующие заболевания, выраженные нарушения бронхиальной проходимости — объем форсированного выдоха за первую секунду (ОФВ1)
С. В. Лукьянов, доктор медицинских наук, профессор ФГУ «Консультативно-методический центр лицензирования» Росздравнадзора, Москва
Моксифлоксацин улучшает долговременный прогноз у больных с инфекционным обострением хронического бронхита
Опубликовано в журнале: Пульмонология, 2003, №6
© КОЛЛЕКТИВ АВТОРОВ, 2003 УДК 616.248-036.17 Л.И.Дворецкий, С.В.Яковлев, В.Е.Ноников, А.Ю.Стрекачев, Н.В.Дубровская ММА им. И.М.Сеченова; ЦКБ УД Президента РФ, Москва
Половина случаев обострения хронического бронхита связана с бактериальной инфекцией и требует назначения антибактериальных препаратов. В плацебо-контролируемых исследованиях, проведенных в 80-х годах прошлого столетия, убедительно показано, что антибиотики имеют преимущество по сравнению с плацебо, приводят к более быстрому исчезновению симптомов обострения, укорачивают сроки выздоровления
Для лечения обострений хронического бронхита обычно рекомендуются 3 группы препаратов:
Многочисленные контролируемые исследования обычно демонстрируют одинаковую клиническую эффективность различных антибиотиков при обострении хронического бронхита, хотя сравниваемые препараты могут существенно различаться по уровню активности в отношении наиболее типичных возбудителей заболевания. В частности, макролидные антибиотики, широко применяемые при хроническом бронхите, характеризуются очень слабой активностью против гемофильной палочки (ответственной за половину всех случаев обострения хронического бронхита) и существенно уступают по этому показателю бета-лактамам и фторхинолонам. Среди антибиотиков, рекомендуемых для лечения хронического бронхита, наиболее активны in vitro против гемофильной палочки фторхинолоны (МПК90 16
Закономерен вопрос, действительно ли различия в активности антибиотиков in vitro имеют реальное клиническое значение?
С современных позиций доказательной медицины основным критерием клинической эффективности препаратов являются результаты контролируемых сравнительных исследований. Однако при внебольничных респираторных инфекциях, в частности при обострении хронического бронхита, результаты контролируемых клинических исследований не могут служить обоснованием для рекомендаций по выбору антибиотика, так как чувствительность таких исследований в выявлении различий между препаратами крайне низка. Это в первую очередь связано с тем, что при обострении хронического бронхита уровень спонтанного выздоровления (без антибиотиков) достаточно высокий (более 90%) и для того, чтобы выявить клинически значимые различия между антибиотиками, требуется включить в исследование очень большое количество пациентов (несколько тысяч), что нереально в практической медицине.
Еще одна причина лимитации контролируемых исследований в выявлении различий между антибиотиками — чрезмерная «жесткость» протоколов по критериям включения пациентов в исследование: как правило, из большинства исследований исключают больных с серьезной сопутствующей патологией, тяжелым обострением, в некоторых исследованиях лимитирован возраст пациентов, т. е. в исследованиях обычно не анализируются случаи заболевания с более серьезным прогнозом и клинические ситуации, при которых можно ожидать этиологическую роль возбудителей с более высоким уровнем антибиотикорезистентности.
Несмотря на кажущуюся равноценную эффективность антибиотиков при хроническом бронхите, мнение экспертов и клинический опыт практических врачей все же позволяют выделить более эффективные антибиотики для лечения обострения хронического бронхита по сравнению с другими. Результаты опроса врачей поликлиник об эффективности различных антибиотиков при хроническом бронхите показали превосходство бета-лактамов по сравнению с макролидами (наши данные). В другом исследовании 75% врачей и 79% пациентов отметили отчетливое превосходство моксифлоксацина по сравнению с макролидами (эритромицин, азитромицин, кларитромицин или рокситромицин) при обострении хронического бронхита [2].
Какие же объективные критерии следует учитывать при оценке эффективности антибиотиков при обострении хронического бронхита?
Исследования последних лет позволили установить отчетливую связь между бактериологическим успехом лечения обострения хронического бронхита и долговременным прогнозом ХОБЛ. Эрадикация возбудителя при хроническом бронхите является наиболее важным фактором благоприятного долговременного прогноза [8]. Установлено, что эрадикация Haemophilus influenzae из бронхиального секрета при обострении заболевания способствует замедлению прогрессирования структурных изменений в бронхах, восстановлению активности факторов местной защиты легких, удлинению сроков ремиссии заболевания [6,7]. В некоторых исследованиях установлены различия в бактериологической эффективности антибиотиков при обострении хронического бронхита. Например, в работе DeAbate и соавт. [4] было показано, что клиническая эффективность моксифлоксацина и азитромицина при инфекционном обострении хронического бронхита была одинаковой, однако лечение моксифлоксацином сопровождалось существенно более высоким уровнем эрадикации Н.influenzas и Н.parainfluenzae (97 и 88%) по сравнению с азитромицином (83 и 62%). Сходные данные наблюдались в другом исследовании: грепафлоксацин приводил к более быстрой (на 2-й день лечения) и более полной (93%) эрадикации H.influenzae из мокроты по сравнению с кларитромицином (20% через 7 дней лечения) [11]. Кроме того, эрадикация S.pneumoniae и H.influenzae во время лечения будет также способствовать ограничению селекции в популяции резистентных штаммов микроорганизмов.
Таким образом, при инфекциях с высоким уровнем спонтанного выздоровления, таких как обострение хронического бронхита, основное внимание должно уделяться не столько клиническому, сколько бактериологическому эффекту лечения, т. е. способности антибиотика элиминировать возбудителя из бронхов. Однако при хроническом бронхите во многих случаях сложно оценить истинный уровень эрадикации возбудителей на фоне лечения, так как положительный клинический эффект обычно сопровождается прекращением выделения гнойной мокроты, но при этом совсем не обязательно, что будет достигнута эрадикация возбудителя из бронхов (случаи так называемой предполагаемой эрадикации, которые также относят к положительному бактериологическому эффекту, совсем не обязательно соответствуют истинному уровню эрадикации).
С учетом вышеизложенного наиболее объективным и достоверным критерием эффективности антибиотиков при хроническом бронхите следует считать длительность безрецидивного периода (долговременный прогноз) и эрадикацию возбудителя.
В пилотном исследовании, учитывающем долговременный прогноз, проведенном в середине 90-х годов, было показано, что длительность безрецидивного периода после обострения хронического бронхита составила 142 дня при лечении ципрофлокса-цином и 51 день при лечении кларитромицином [3]. Хотя различия не были достоверными, данное исследование показало целесообразность учета длительности ремиссии при сравнении эффективности различных режимов антибактериальной терапии обострения хронического бронхита. В последние годы были проведены 2 исследования по влиянию моксифлоксацина на долговременный прогноз у пациентов с хроническим бронхитом. Выбор моксифлоксацина в качестве основного препарата для лечения обострения хронического бронхита вполне оправдан, так как он характеризуется наиболее выраженной антимикробной активностью in vitro в отношении наиболее актуальных возбудителей обострения хронического бронхита у пациентов всех возрастных групп (табл.2).
Таблица 2 Сравнительная активность фторхинолонов in vitro в отношении возбудителей обострения хронического бронхита [10]
В 2001—2003 г. мы провели открытое, рандомизированное, проспективное, многоцентровое, сравнительное клиническое исследование моксифлоксацина и макролидных антибиотиков при лечении инфекционного обострения у больных хроническим бронхитом. В исследование включали пациентов с документированным диагнозом обострения хронического бронхита.
Все пациенты были рандомизированы на 2 группы: 1-я группа получала моксифлоксацин внутрь в дозе 400 мг 1 раз в сутки в течение 5 дней; 2-я группа получала макролидный антибиотик в стандартной дозе (по усмотрению врача) в течение 7 дней (ази-тромицин 5 дней). У пациентов оценивали клиническую эффективность лечения на 3-5-й день после окончания терапии. В последующие сроки в течение 12 мес наблюдали за пациентами с целью выявления обострений заболевания и фиксировали потребность в повторных назначениях антибиотиков.
Оценка клинической эффективности лечения обострения была проведена у 29 пациентов, получавших моксифлоксацин, и 31 пациента, получавшего макролид (азитромицин, спирамицин или кларитромицин). Пациенты обеих групп не различались по возрасту (средний возраст пациентов 1-й и 2-й групп был 58,1 и 57,3 года), давности ХОБЛ и выраженности инфекционного обострения.
На фоне применения моксифлоксацина клиническая эффективность лечения обострениях бронхита составила 96,6%, на фоне макролидных антибиотиков — 93,5%. Переносимость препаратов была хорошей, нежелательные явления (возможно, связанные с препаратом) отмечены соответственно у 6,9 и 6,5% больных.
В настоящее время обработаны результаты 6-месячного наблюдения за пациентами после окончания лечения. Повторное инфекционное обострение хронического бронхита, потребовавшее назначения антибиотиков, наблюдалось у 3,6% пациентов, получавших моксифлоксацин, и 13,8% пациентов, получавших макролидный антибиотик. Срок ближайшего обострения составил соответственно 4 и 1,5 мес.
Таким образом, предварительные результаты позволяют сделать заключение, что моксифлоксацин по сравнению с макролидными антибиотиками улучшает долговременный прогноз при обострении хронического бронхита, при этом частота повторных бронхо-легочных инфекций в ближайшие 6 мес при лечении моксифлоксацином в 3,8 раза меньше, чем при применении макролидов.
Исследование MOSAIC. Результаты данного международного, многоцентрового, двойного, слепого, сравнительного исследования моксифлоксацина и стандартных режимов терапии (СРТ) обострения хронического бронхита представлены в 2003 г. на двух международных конференциях [12,13].
В исследование были включены 733 пациента с инфекционным обострением хронического бронхита, из них 357 пациентов получали моксифлоксацин в дозе 400 мг 1 раз в сутки в течение 5 дней, 376 пациентов — в течение 7 дней СРТ (амоксициллин 500 мг 2 раза в сутки или кларитромицин 500 мг 2 раза в сутки, или цефуроксим аксетил 250 мг 2 раза в сутки). Пациенты сравниваемых групп не различались по возрасту (средний возраст 64,5 и 62,5 года), полу, наличию сопутствующей патологии, длительности курения и давности заболевания, а также тяжести обострения.
Положительный клинический эффект наблюдался у 87,6% пациентов, получавших моксифлоксацин, и у 83% пациентов, получавших СРТ, при этом полное исчезновение симптомов обострения в конце лечения отмечено соответственно у 70,9 и 62,8% больных (различия достоверны, р=0,02). Бактериологическая эффективность (эрадикация возбудителя) была также выше в группе моксифлоксацина (92 и 81%, р=0,05). Средний интервал между окончанием лечения и последующим обострением был на 2 нед больше при применении моксифлоксацина (133 и 118 дней).
Проведенное исследование показало более высокую как клиническую, так и бактериологическую эффективность моксифлоксацина при лечении обострения хронического бронхита по сравнению со СРТ и лучший долговременный прогноз при применении моксифлоксацина.
В заключение следует отметить, что моксифлоксацин наряду с более высокой активностью in vitro в отношении основных респираторных возбудителей имеет также отчетливое преимущество при лечении пациентов с обострением хронического бронхита в сравнении с амоксициллином, цефалоспоринами II поколения и макролидными антибиотиками. Лечение моксифлоксацином приводит к более выраженному клинико-бактериологическому эффекту (выздоровление+эрадикация) при обострении хронического бронхита, что сопровождается удлинением безрецидивного периода и характеризует улучшение долговременного прогноза при ХОБЛ.