базальные отделы сердца что это
Лечение гипертрофической кардиомиопатии
Гипертрофическая кардиомиопатия (ГКМП) – это генетически обусловленное заболевание миокарда, проявляющееся комплексом специфических морфо-функциональных изменений
Лечение гипертрофической кардиомиопатии
Гипертрофическая кардиомиопатия (ГКМП) – это генетически обусловленное заболевание миокарда, проявляющееся комплексом специфических морфо-функциональных изменений и постепенно прогрессирующим течением с высоким риском развития жизнеугрожающих аритмий и внезапной смерти.
Типичными являются морфологические изменения: аномалия архитектоники сократительных элементов миокарда (гипертрофия и дезориентация мышечных волокон), развитие фибротических изменений мышцы сердца, патология мелких интрамиокардиальных сосудов.
При ГКМП происходит массивная гипертрофия миокарда левого (и реже правого желудочка), чаще асимметричного характера за счет утолщения межжелудочковой перегородки, часто с развитием обструкции выходного тракта левого желудочка (ЛЖ) при отсутствии каких-либо явных причин.
Общепризнанной является представление о преимущественно наследственной природе ГКМП. В связи с этим, широкое распространение получил термин «семейная гипертрофическая кардиомиопатия». К настоящему времени установлено, что более половины всех случаев заболевания являются наследуемыми, при этом основной тип наследования – аутосомно-доминантный. Оставшиеся приходятся на так называемую спорадическую форму; в этом случае у пациента нет родственников, болеющих ГКМП или имеющих гипертрофию миокарда. Считается, что большинство, если не все случаи спорадической ГКМП, также имеют генетическую причину, т. е. вызваны случайными мутациями.
Гипертрофическая кардиомиопатия – это генетически гетерогенное заболевание, причиной которого являются более 200 описанных мутаций нескольких генов, кодирующих белки миофибриллярного аппарата. К настоящему времени известны 10 белковых компонентов сердечного саркомера, выполняющих контрактильную, структурную или регуляторную функции, дефекты которых наблюдаются при ГКМП. Причем в каждом гене множество мутаций могут становиться причиной заболевания (полигенное мультиаллельное заболевание).
Наличие той или иной ассоциированной с ГКМП мутации признается «золотым» стандартом диагностики заболевания. При этом описанные генетические дефекты характеризуются разной степенью пенетрантности, выраженностью морфологических и клинических проявлений. Тяжесть клинической картины зависит от присутствия и степени гипертрофии.
Таким образом, ГКМП характеризуется крайней гетерогенностью вызывающих ее причин, морфологических, гемодинамических и клинических проявлений, разнообразием вариантов течения и прогноза, что существенно затрудняет выбор адекватных и наиболее эффективных лечебных подходов по контролю и коррекции имеющихся нарушений.
Возможны три гемодинамических варианта обструктивной ГКМП:
Cимптомы болезни разнообразны и малоспецифичны, связаны с гемодинамическими нарушениями (диастолическая дисфункция, динамическая обструкция путей оттока, митральная регургитация), ишемией миокарда, патологией вегетативной регуляции кровообращения и нарушением электрофизиологических процессов в сердце. Диапазон клинических проявлений крайне велик: от бессимптомных до неуклонно прогрессирующих и трудно поддающихся медикаментозному лечению форм, сопровождающихся тяжелой симптоматикой.
Повышение диастолического давления в левом желудочке из-за диастолической дисфункции, динамическая обструкция выносящего тракта левого желудочка проявляются одышкой в покое и при физической нагрузке, утомляемости, слабости. Нарастание давления в малом круге кровообращения сопровождается развитием острой левожелудочковой недостаточности (чаще в ночные часы – сердечная астма, альвеолярный отек легких).
Падение фракции выброса при физической нагрузке или нарушениях сердечного ритма сопровождается ухудшением кровообращения головного мозга. Преходящая ишемия мозговых структур проявляется кратковременной потерей сознания (обморок) или предобморочными состояниями (внезапная слабость, головокружение, потемнение в глазах, шум и «заложенность» в ушах).
Методы исследования:
ЭХО-КГ – основной метод диагностики ГКМП. Критериями диагностики ГКМП на основании данных ЭХО-КГ являются:
Если в покое обструкции выносящего тракта левого желудочка нет, ее можно спровоцировать медикаментозными (ингаляция амилнитрита, введение изопреналина, добутамина) или функциональными пробами (проба Вальсальвы, физическая нагрузка), которые уменьшают преднагрузку или повышают сократимость левого желудочка.
Катетеризация сердца и коронарная ангиография проводятся для оценки коронарного русла перед миоэктомией или операцией на митральном клапане, а также чтобы выяснить причину ишемии миокарда. При этом к характерным признакам ГКМП относят:
Сцинтиграфия миокарда и позитронно-эмиссионная томография
При гипертрофической кардиомиопатии сцинтиграфия миокарда имеет некоторые особенности, однако в целом ее значение в диагностике ишемии такое же, как и обычно. Стойкие дефекты накопления указывают на рубцовые изменения после инфаркта миокарда, обычно они сопровождаются снижением функции левого желудочка и плохой переносимостью физической нагрузки. Обратимые дефекты накопления указывают на ишемию, вызванную снижением коронарного резерва при нормальных артериях или коронарным атеросклерозом. Обратимые дефекты часто никак не проявляются, однако, по-видимому, они повышают риск внезапной смерти, особенно у молодых больных с гипертрофической кардиомиопатией. При изотопной вентрикулографии можно выявить замедленное наполнение левого желудочка и удлинение периода изоволюмического расслабления.
Позитронно-эмиссионная томография – более чувствительный метод, кроме того, она позволяет учесть и устранить помехи, связанные с затуханием сигнала. Позитронно-эмиссионная томография с фтордезоксиглюкозой подтверждает наличие субэндокарлиальной ишемии, вызванной снижением коронарного резерва.
Современные подходы к лечению ГКМП
По современным представлениям, лечебная стратегия определяется в процессе разделения больных на категории в зависимости от описанных выше вариантов течения и прогноза.
Все лица с ГКМП, включая носителей патологических мутаций без фенотипических проявлений болезни и пациентов с бессимптомным течением заболевания, нуждаются в динамическом наблюдении, в ходе которого оцениваются характер и выраженность морфологических и гемодинамических нарушений. Особое значение имеет выявление факторов, определяющих неблагоприятный прогноз и повышенный риск внезапной смерти (в частности, скрытых, прогностически значимых аритмий).
Общие мероприятия
Ограничение значительных физических нагрузок и запрещение занятий спортом, способных вызывать усугубление гипертрофии миокарда, повышение внутрижелудочкового градиента давления и риска внезапной смерти.
Медикаментозное лечение
До настоящего времени окончательно не решен вопрос о необходимости проведения активной медикаментозной терапии у наиболее многочисленной группы больных с бессимптомной или малосимптомной формами ГКМП и низкой вероятностью внезапной смерти. Противники активной тактики обращают внимание на то, что при благоприятном течении заболевания продолжительность жизни и показатели смертности не отличаются от таковых в общей популяции. Некоторые же авторы указывают на то, что использование в этой группе пациентов β-адреноблокаторов и антагонистов кальция (верапамил) может приводить к сдерживанию гемодинамических нарушений и клинической симптоматики. При этом никто не оспаривает тот факт, что выжидательная тактика в случаях бессимптомного или малосимптомного течения ГКМП возможна лишь при отсутствии признаков внутрижелудочковой обструкции, обмороков и серьезных нарушений сердечного ритма, отягощенной наследственности и случаев ВС у близких родственников.
Следует признать, что лечение ГКМП, генетически обусловленного заболевания, обычно распознаваемого на поздней стадии, пока может быть в большей степени симптоматическим и паллиативным. Тем не менее к основным задачам лечебных мероприятий относятся не только профилактика и коррекция основных клинических проявлений заболевания с улучшением качества жизни пациентов, но и положительное влияние на прогноз, предупреждение случаев ВС и прогрессирования заболевания.
Основу медикаментозной терапии ГКМП составляют препараты с отрицательным инотропным действием: β-адреноблокаторы и блокаторы кальциевых каналов. Для лечения весьма распространенных при этом заболевании нарушений сердечного ритма используются также дизопирамид (антиаритмический препарат IA класса) и амиодарон.
Предпочтение отдается β-блокаторам без внутренней симпатомиметической активности. Наибольший опыт накоплен по применению пропранолола (обзидан, анаприлин). Его назначают начиная с 20 мг 3-4 раза в день, с постепенным увеличением дозы под контролем пульса и артериального давления (АД) до максимально переносимой в большинстве случаев 120–240 мг/сут. Следует стремиться к применению возможно более высоких доз препарата, так как отсутствие эффекта терапии β-блокаторами, вероятно, связано с недостаточной дозировкой. При этом нельзя забывать о том, что повышение дозировок существенно увеличивает риск известных побочных эффектов.
Инвазивные методы лечения:
1. Чрезаортальная септальная миэктомия
2. Вальвулопластики или протезирования митрального клапана
В ряде случаев при наличии дополнительных показаний для уменьшения выраженности обструкции и митральной регургитации одномоментно выполняется операция вальвулопластики или протезирования митрального клапана низкопрофильным протезом. Улучшить отдаленные результаты миэктомии позволяет последующая длительная терапия верапамилом, обеспечивающая улучшение диастолической функции ЛЖ, что не достигается при хирургическом лечении.
3. Иссечения межжелудочковой перегородки
В настоящее время разработаны и успешно применяются отличные от классической миэктомии методики. В частности, в НЦССХ им. А. Н. Бакулева под руководством академика Л. А. Бокерия разработана оригинальная методика иссечения зоны гипертрофированной МЖП из конусной части правого желудочка. Этот способ хирургической коррекции обструктивной ГКМП является высокоэффективным и может стать методом выбора в случаях одновременной обструкции выходных отделов обоих желудочков, а также в случаях среднежелудочковой обструкции ЛЖ.
4. Транскатетерная септальная аблация
Другим альтернативным методом лечения рефракторной обструктивной ГКМП является транскатетерная алкогольная септальная аблация. Методика предполагает инфузию через баллонный катетер в перфорантную септальную ветвь 1–3 мл 95% спирта, вследствие чего возникает инфаркт гипертрофированного отдела МЖП, захватывающей от 3 до 10% массы миокарда ЛЖ (до 20% массы МЖП). Это приводит к значимому уменьшению выраженности обструкции выходного тракта и митральной недостаточности, объективной и субъективной симптоматике заболевания.
В Волынской больнице отработана методика выполнения транскатетерной септальной аблации при ГКМП. Доказан положительный результат данного вмешательства при относительно низком риске развития осложнений.
Как все это работает? Несколько слов о строении сердца и его отделов
Строение сердца у млекопитающих, имеющих 2 круга кровообращения, примерно одинаково. Сердце состоит из двух предсердий (первых камер на пути притекающей крови), двух желудочков, клапанов между этими камерами и входящих и отходящих от сердца сосудов с клапанами у их начала.
Между правым предсердием и правым желудочком находится правый клапан предсердно-желудочковый, или атрио-вентрикулярный, который состоит из 3-х створок. Поэтому его называют трехстворчатым, или трикуспидальным.
Между левым предсердием и левым желудочком находится левый предсердно-желудочковый клапан, который состоит из двух створок и называется митральным.
Клапаны, расположенные в устьях сосудов, отходящих от сердца, или магистральных сосудов, а именно – аорты и легочной артерии – соответственно носят названия «аортальный» и «легочный».
Клапаны аорты и легочной артерии другие по строению. Каждый из них состоит из 3-х полулунных створок, замыкающихся в центре. При открытии они прижимаются к стенке своего сосуда (аорты или легочной артерии), а закрываются, полностью замыкая просвет сосуда. При этом их вид напоминает фирменный знак компании «Мерседес».
Ткань самих створок, как атрио-вентрикулярных, так и полулунных — тонкая, у детей даже прозрачная, но поразительно эластичная и прочная, рассчитанная природой на непрекращающуюся ритмичную работу, исчисляемую миллиардами однообразных действий.
Между полостями сердца, или его камерами, расположены перегородки, разделяющие потоки венозной и артериальной крови. Это межпредсердная перегородка, т.е. между правым и левым предсердиями, и межжелудочковая перегородка – между правым и левым желудочками. В нормальном, сформированном сердце они полностью закрыты, в них нет никаких отверстий или дефектов и, таким образом, кровь из одной половины сердца в другую никогда не поступает.
Остановимся подробнее на анатомическом устройстве сердца и его камер. Ведь даже те из них, которые называются одинаково (предсердия или желудочки), устроены абсолютно по-разному и выполняют разные функции.
Сердце по форме напоминает грушу, лежащую несколько на боку, с верхушкой, расположенной слева и внизу, а основанием — правее и вверху. Верхушка сердца – это та его часть, движения которой можно почувствовать, если положить ладонь на грудную клетку в пятом межреберье слева от грудинной кости. Его толчок легко можно ощутить и у себя, и у ребенка. Это движения верхушки сердца при каждом сокращении. Сокращения почти синхронны с пульсом, который тоже можно легко прощупать на руке (там, где предплечье переходит в кисть) или на шейных сосудах. Пульс – это наполнение сосудов волной крови, поступающей из сердца с каждым его сокращением. Частота пульса, его ритмичность являются косвенным и легко доступным отражением деятельности самого сердца.
Верхушка — самая подвижная часть сердца, хотя и всё оно, все его отделы находятся в постоянном движении.
Работа сердца, его движение, состоит из двух чередующихся фаз — сокращения (систолы) и расслабления (диастолы).
Ритмичное, постоянное чередование этих фаз, необходимое для нормальной работы, обеспечивается возникновением и проведением электрического импульса по системе особых клеток – по узлам и волокнам проводящей системы сердца. Импульсы возникают вначале в самом верхнем, так называемом, синусовом узле, далее проходят ко второму, атрио-вентрикулярному узлу, а от него – по более тонким волокнам – к мышце правого и левого желудочков, вызывая сокращение всей их мускулатуры.
Правое предсердие принимает венозную кровь из полых вен, т.е. от всего тела и вдобавок венозную кровь самого сердца. Это – большая по объему и, пожалуй, самая растягиваемая камера сердца. При необходимости она способна вместить в несколько раз больше крови, чем в обычных условиях, т.е. обладает гигантским «запасом» объема. Стенка правого предсердия состоит из слоя тонких мышечных волокон. Помимо функции «приема» венозной крови, правое предсердие выполняет функцию водителя сердечного ритма. В его стенках залегают оба главных узла проводящей системы сердца.
Правое предсердие соединяется или, точнее, открывается в правый желудочек через предсердно-желудочковое отверстие, регулируемое трикуспидальным клапаном. Это отверстие достаточно широкое, чтобы пропустить весь объем крови из предсердия в правый желудочек в период расслабления его мышц, т.е. в фазу диастолы, и заполнить его полость.
— значительно более толстостенная, чем предсердие, мышечная структура. Это — самый передний отдел сердца, лежащий тотчас под грудинной костью. Он относительно растяжимый в случае необходимости. Форма его полости напоминает новый месяц, появившийся в небе. Если внимательно присмотреться, то видно, как светящаяся полоса месяца полукругом охватывает большой темный шар неосвещенной части Луны. Так и правый желудочек обтекает своей полостью мощный цилиндрический левый.
открывается в легочную артерию, которая вместе с аортой является так называемым магистральными, или «великим», сосудом. На переходе от желудочка в легочную артерию расположен трехстворчатый, полулунный клапан легочного ствола, пропускающий кровь в одном направлении — в легкие.
— самая заднерасположенная из сердечных камер. Оно принимает окисленную, артериальную кровь из легочных вен. Вен всего четыре и они впадают в заднюю стенку левого предсердия. Камера этого предсердия значительно меньше, чем правого, и способность ее к растяжению существенно меньше.
Левое предсердие открывается через предсердно-желудочковое отверстие в левый желудочек. В этом отверстии находятся двухстворчатый — митральный — клапан, открытие и закрытие которого регулирует процесс заполнения и опорожнения желудочка в фазы систолы и диастолы.
— главный в сердце, да и во всей системе кровообращения. Это — мощная мышечная камера, стенки которой в 3-4 раза толще, чем у правого соседа. Это — компактный конус с отверстием входа (с митральным клапаном) и выхода (с трехстворчатым аортальным полулунным клапаном), лежащими рядом друг с другом и тесно взаимосвязанными.
Чтобы вся эта сложная система стройно и четко работала, она должна получать постоянное необходимое питание в виде кислорода и питательных веществ, а отработанные продукты должны удаляться. Для этого существуют артериальная и венозная системы самого сердца.
самого сердца состоит из двух — левой и правой – коронарных (венечных) артерий, которые отходят в самом начале, в устье восходящей аорты. Это ее первые ветви. Они тот час делятся на более мелкие и разносят кровь по всем участкам непрерывно двигающегося сердца. «Отработанная», отдавшая кислород, кровь втекает по многочисленным мелким венам, которые собираются в одну большую — венечный синус — и впадают в полость правого предсердия. Таким образом, сердце питает само себя, и от правильного положения и состояния венечных артерий его функция зависит напрямую.
Итак, подведем итог. Анатомически сердце — это мощный мышечный орган, имеющий четыре камеры и четыре клапана. Строение камер и клапанов отлично друг от друга, т.к. подчинено выполнению разных задач. Правые отделы сердца отделены от левых перегородками и между собой не сообщаются.
Цитируется по книге Г. Э. Фальковский, С. М. Крупянко. Сердце ребенка. Книга для родителей о врожденных пороках сердца
Базальные отделы сердца что это
В любом эхокардиографическом исследовании центральное место занимает оценка левого желудочка и его функции. В данной главе обсуждаются аспекты нормальной и патологической морфологии левого желудочка, а также качественные и количественные параметры оценки его глобальной и региональной функции. Наиболее частое сердечно-сосудистое заболевание, коронарная болезнь сердца (КБС), преимущественно поражает миокард именно левого желудочка и приводит к типичным общим и локальным изменениям. Некоторые из них можно распознать уже в покое, другие же — при пробе с нагрузкой или стимуляцией.
а) Форма и характеристики левого желудочка сердца. Нормальный левый желудочек представляет собой толстостенное, конусовидное (точнее: эллипсоидное) полое мышечное образование с полукруглым колпачком на верхушке. Его поперечник, как видно на эхокардиографических сечениях по короткой оси в парастернальном или субкостальном доступе, имеет форму окружности. Поэтому объем и массу здорового левого желудочка можно в хорошем приближении рассчитывать, исходя из формы эллипсоида вращения. Линия пересечения со свободной стенкой правого желудочка делит левый желудочек на межжелудочковую перегородку и свободную стенку, от которой отходят папиллярные мышцы; эти последние не контактируют с перегородкой.
2. Характеристики левого желудочка. Отличительными анатомическими признаками левого желудочка в отличие от правого, позволяющими идентифицировать первый, в том числе при различных врожденных мальформациях, являются: две хорошо разграниченные папиллярные мышцы, непосредственное соседство клапанов атриовентрикулярного («входного», т.е. митрального) и артериального («выносящего», т.е. аортального), а также более мелкая по сравнению с правым желудочком трабекулярная сеть, которая к тому же довольно мало развита в области перегородки. Соотношение систолической толщины «компактного» субэп и кардиального миокарда к толщине «некомпактной» трабекулярной зоны составляет менее чем 1/2; это важно при исключении «изолированного некомпактного миокарда» («isolated ventricular non-compaction», одна из форм кардиомиопатии).
3. Объемы. Из-за трабекулярной зоны (наряду с другими причинами) объемы, вычисленные при ангиографии или контрастной ЭхоКГ, всегда несколько больше, чем рассчитанные при двумерной ЭхоКГ, поскольку в первом случае контрастное вещество проникает в трабекулярную зону и оптически добавляет ее к полости желудочка, тогда как при двумерной ЭхоКГ граница проводится по внутреннему краю трабекул (см. раздел «Объемы и фракция выброса»).
б) Приносящий и выносящий тракты. Хотя в левом желудочке, в отличие от правого, нет собственно анатомического разделения на приносящий и выносящий тракты, эти обозначения традиционно используются в качестве функциональных понятий. Через митральный клапан кровь сначала попадает в приносящий тракт левого желудочка, образованный митральными створками, подклапанным аппаратом и папиллярными мышцами. Из приносящего тракта кровь переходит в апикальную область, где в ходе спиралевидного движения разворачивается почти на 180° по направлению к выносящему тракту. Последний образован передней створкой митрального клапана, а также базальными отделами перегородки и передней стенки. В этой области межжелудочковая перегородка имеет наибольшую толщину.
в) Деление на сегменты:
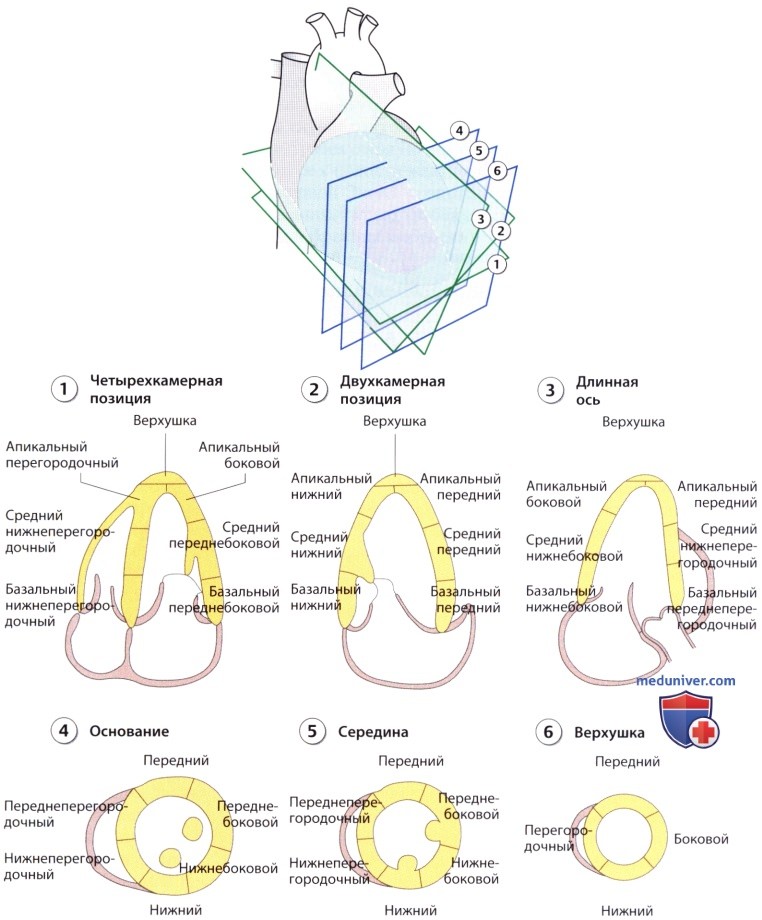
1. 16-сегментная модель. Миокард левого желудочка подразделяют на сегменты, чтобы учесть локальный характер многих патологических изменений, прежде всего при КБС. Наиболее часто используемый принцип, предложенный Американским обществом эхокардиографии в 1989 г., подразумевает деление 6 стенок желудочка в апикально-базальном направлении на три части, примерно соответствующие трем равным отрезкам продольной оси: апикальный, средний и базальный сегмент. Сами же стенки обозначаются следующим образом (по часовой стрелке): передняя, боковая, задняя, нижняя (задняя стенка в узком смысле слова), перегородочная и переднеперегородочная. Однако апикальный переднеперегородочный и апикальный задний сегменты не выделяются, т.е. в апикальном сечении по короткой оси находятся лишь 4 сегмента (передний, перегородочный, боковой и нижний). Причина этого заключается в принципе деления: авторы стремились, чтобы всем сегментам соответствовала примерно одинаковая масса миокарда; поэтому верхушка была поделена на меньшее число частей. Фактически с анатомической точки зрения базальный, средний и апикальный отделы содержат примерно 43, 35 и 21% миокарда соответственно, поскольку по направлению к верхушке миокард истончается, а поперечник желудочка уменьшается. Доступность сегментов для анализа в стандартных сечениях видна на иллюстрациях.
В принципе все сегменты можно визуализировать при исследовании как по длинной, так и по короткой оси. Но поскольку часто не удается достичь качественного изображения в апикальном сечении по короткой оси, то, как правило, апикальные сегменты визуализируются только по длинной оси. Еще одним важным аспектом, особенно для пациентов с КБС, является то, что сегменты обычно можно классифицировать по зонам коронарного кровоснабжения, хотя из-за вариабельности коронарной системы это деление не всегда надежно (например, так называемые левый и правый типы кровоснабжения сердца с соответствующим снабжением нижней и часто также задней стенок, или различная длина передней межжелудочковой ветви с соответствующим разным кровоснабжением нижнего апикального сегмента, и так далее).
2. 17-сегментная модель. В последнее время Американская кардиологическая ассоциация предложила новую систему номенклатуры осей, стенок и сегментов для всех визуализирующих методик, которая, однако, до сих пор еще не нашла значительного распространения в ЭхоКГ. Эта система предусматривает дополнительный семнадцатый, чисто верхушечный сегмент, который «как крышечка» накрывает 6 базальных, 6 средних и 4 апикальных сегмента. Целью новой системы была лучшая согласованность с номенклатурой других визуализирующих методик, в первую очередь сцинтиграфии. Однако для стресс-ЭхоКГ проблема использования этой новой системы заключается в том, что невозможно эхокардиографическими способами оценить функцию этого верхушечного сегмента.
Поэтому в дальнейшем мы будем использовать привычную номенклатуру осей, сечений и 16 сегментов, как это сделано и в актуальных рекомендациях европейских и американских эхокардиографических сообществ.
г) Эхоструктура миокарда. При оптимальных настройках усиления сигнала миокард левого желудочка имеет относительно слабую эхогенность; он значительно темнее, чем эпи-/перикард или эндокард, но несколько светлее, чем полость желудочка. Оценка гистологических изменений миокарда на основании его общей эхогенности крайне ограничена; особенно ненадежным критерием является эхоструктура миокарда для диагностики кардиомиопатии или амилоидоза. Считающееся классическим признаком амилоидоза сердца «зернистое поблескивание» («granular sparkling») может также встречаться при значительном утолщении стенки другой этиологии. Старые постинфарктные рубцы, особенно в перегородке, часто бывают светлее, чем нормальный миокард, что связывается с повышенным содержанием коллагена.
Расположение волокон миокарда. Для эхоструктуры миокарда, кроме воды и содержания коллагена, важную роль играет ход волокон миокарда. У пациентов с сахарным диабетом и ожирением также обнаруживаются отчетливо повышенные значения эхогенности миокарда, хотя это и не всегда видно на глаз. Центральное просветление межжелудочковой перегородки, которое регулярно, хотя и в различной степени, обнаруживается при сканировании из четырехкамерной позиции, связано, по-видимому, с различным расположением волокон миокарда левого и правого желудочков.
Редактор: Искандер Милевски. Дата публикации: 25.12.2019
