болезнь кахексия что такое
Раковая кахексия
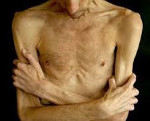
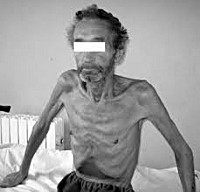
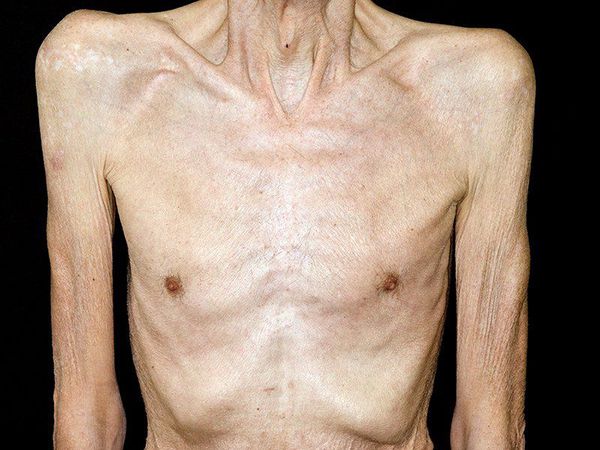
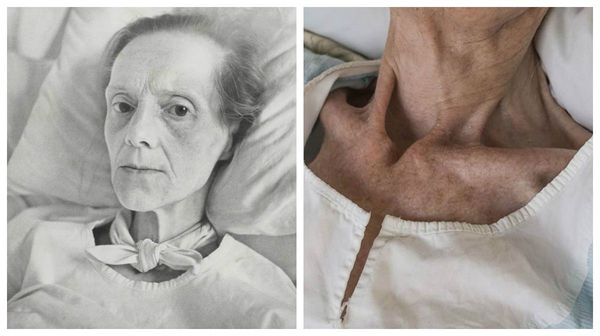
Раковая кахексия – крайнее истощение, возникающее при онкологических заболеваниях. Проявляется резким снижением массы тела, мышечной слабостью, нарушением трудоспособности, расстройствами сна, бледностью и дряблостью кожи, трофическими изменениями волос и ногтей, гипотонией, снижением иммунитета, отеками, психическими расстройствами, аменореей у женщин и утратой либидо у мужчин. Раковая кахексия сопровождается нарушениями всех видов обмена. Нередко становится прямой или косвенной причиной смерти больного. Диагностируется на основании анамнеза, данных внешнего осмотра и объективных исследований. Лечение медикаментозное.
Общие сведения
Раковая кахексия – прогрессирующая потеря массы тела, возникающая при злокачественных новообразованиях и сопровождающаяся нервно-мышечной слабостью, нарушением аппетита, расстройствами белкового, жирового, углеводного и водно-электролитного обмена. Раковая кахексия оказывает выраженное негативное влияние на работу всех органов и систем. Со временем становится причиной несовместимых с жизнью нарушений гомеостаза. По различным данным, является причиной смерти 20-50% пациентов, страдающих онкологическими заболеваниями. Может возникать при опухолях любой локализации, однако чаще диагностируется при поражениях дыхательной и пищеварительной системы. Лечение раковой кахексии осуществляют специалисты в сфере онкологии, диетологии, гастроэнтерологии, пульмонологии и других областей медицины (в зависимости от локализации новообразования).
Патогенез раковой кахексии
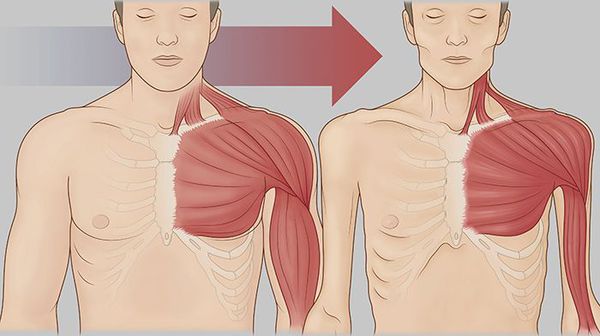
Патогенез данного состояния пока недостаточно изучен. Предполагается, что основную роль в развитии раковой кахексии играет интоксикация организма продуктами распада злокачественного новообразования. Некоторые специалисты указывают, что фактором, провоцирующим и/или усугубляющим данный синдром, является вторичная инфекция в зоне распадающейся опухоли. Установлено, что раковая кахексия по ряду признаков отличается от истощения, обусловленного недостаточным поступлением питательных веществ в организм. При кахексии, вызванной голоданием, отмечается уменьшение количества жировой ткани. Уровень обмена веществ снижается, печень атрофируется, распад белка замедляется. При раковой кахексии больной теряет как жировую, так и мышечную ткань. Уровень обмена веществ остается в норме или повышается, печень увеличивается, распад белка становится более интенсивным.
Кроме того, раковая кахексия сопровождается расстройством всех видов обмена. Нарушения углеводного обмена проявляются снижением уровня глюкозы, уменьшением запасов гликогена, усилением глюконеогенеза и снижением чувствительности к инсулину. Нарушения жирового обмена при раковой кахексии заключаются в уменьшении количества жиров, усилении липолиза, снижении активности липопротеидлипазы, повышении уровня триглицеридов и распаде глицерина. О нарушении белкового обмена свидетельствуют отрицательный азотистый баланс и усиление распада белков, в том числе – за счет поперечно-полосатых мышц.
Раковая кахексия протекает на фоне уменьшения количества поступающих питательных веществ и увеличения энергетических затрат. Постоянным признаком раковой кахексии является расстройство аппетита, обусловленное целым рядом факторов, в том числе – болевым синдромом, вкусовыми и обонятельными нарушениями, химиотерапией, радиотерапией и стоматитом, часто развивающимся у онкологических больных. Другими причинами развития раковой кахексии являются депрессивное расстройство, нарушение функций различных органов, тошнота, рвота, рост опухолей желудочно-кишечного тракта, сдавление желудка и кишечника новообразованиями, расположенными в близлежащих органах.
Увеличение энергетических потерь при раковой кахексии обусловлено синдромом нарушенного всасывания и диареей, которые часто возникают на фоне лучевой терапии, химиотерапии, хирургического удаления значительных участков желудочно-кишечного тракта, новообразований поджелудочной железы, карциноидного синдрома, рака щитовидной железы и гастриномы. Из-за значительных потерь белка у больных раковой кахексией возникают анемия, гипертрансферринемия и гипоальбуминемия. Трофические изменения кожи, снижение иммунитета и ограничение подвижности, обусловленное резкой слабостью, становятся причиной развития пролежней и пневмонии.
Классификация раковой кахексии
Выделяют три стадии раковой кахексии:
Симптомы раковой кахексии
Пациенты предъявляют жалобы на резкую слабость, вялость, повышенную утомляемость, лихорадку, запоры или поносы. Нарушается суточный ритм сна-бодрствования: по ночам больные раковой кахексией страдают от бессонницы, в дневное время чувствуют сонливость. У женщин возникает аменорея, у мужчин отмечается отсутствие либидо. Развиваются психические расстройства. Многие пациенты с раковой кахексией страдают от депрессии. Наблюдаются слезливость, раздражительность и эмоциональная лабильность, сменяющиеся апатией и безразличием. При прогрессировании основного заболевания возможны нарушения сознания.
При внешнем осмотре больных раковой кахексией выявляется истощение различной степени выраженности. Иногда (как правило – при опухолях яичников, матки или молочной железы, сопровождающихся гормональными нарушениями) больные имеют нормальную или повышенную массу тела. Кожа пациентов с раковой кахексией сухая, дряблая, сероватого или желтоватого цвета с землистым оттенком. Отмечается углубление морщин, выраженный дефицит подкожной жировой клетчатки, ломкость волос и ногтей, повышенное выпадение волос. Могут наблюдаться безбелковые отеки, асцит или гидроторакс. Определяются гипотония и тахикардия. Развивается стоматит, возможно расшатывание и выпадение зубов. По анализам крови определяется анемия.
Диагностика раковой кахексии
Диагноз «раковая кахексия» устанавливается с учетом анамнеза (наличие онкологического заболевания), жалоб, данных внешнего осмотра, лабораторных и инструментальных исследований. В процессе диагностики акцентируют внимание на уменьшении количества потребляемой пищи, преобладании катаболических процессов над анаболическими, выраженных расстройствах функции скелетных мышц (уменьшение мышечной массы, снижение силы мышц), изменении функциональных способностей организма и ухудшении качества жизни пациента, страдающего раковой кахексией.
Для оценки уровня анемии, функционального состояния печени и почек проводят общий анализ крови, биохимический анализ крови и общий анализ мочи. При подозрении на септические осложнения назначают анализ мочи на бакпосев. При отсутствии диагноза основного онкологического заболевания пациентов с раковой кахексией направляют на рентгенографию грудной клетки, УЗИ органов брюшной полости, колоноскопию, гастроскопию, гистероскопию, МРТ головного мозга и другие исследования (в зависимости от предполагаемой локализации новообразования). Назначают консультации различных специалистов: терапевта, кардиолога, гастроэнтеролога, невролога, эндокринолога, уролога, гинеколога и т. д.
Лечение раковой кахексии
Лечение симптоматическое. Пациентам с раковой кахексией назначают диету, предусматривающую употребление легкоусвояемых продуктов с большим количеством белков, жиров, микроэлементов и витаминов. Используют препараты для повышения аппетита и противорвотные средства. При необходимости (при выраженном истощении, нарушении глотании, тяжелых инфекционных осложнениях) осуществляют парентеральное введение глюкозы, аминокислотных смесей, витаминов и электролитных растворов. Параллельно проводят терапию основного заболевания.
Прогноз в большинстве случаев неблагоприятный, особенно при рефрактерной раковой кахексии. Состояние пациентов постепенно ухудшается. Расстройства гомеостаза усугубляются из-за нарушения деятельности различных органов и систем и присоединяющихся инфекционных осложнений. При потере 30-50% белка наступает летальный исход. Непосредственной причиной смерти становятся тяжелое общее истощение, пневмонии и обширные пролежни. От раковой кахексии погибает от 20 до 50% больных, страдающих онкологическими заболеваниями.
Что такое кахексия? Причины возникновения, диагностику и методы лечения разберем в статье доктора Плотниковой Яны Яковлевны, эндокринолога со стажем в 8 лет.
Определение болезни. Причины заболевания
Кахексия — это крайнее истощение организма. Сопровождается резким снижением веса, общей слабостью, изменением психоэмоционального состояния и ухудшением жизнедеятельности организма в целом.
Диагноз устанавливается в случаях, когда человек менее чем за год теряет более 50 % исходной массы тела. Т акой дефицит веса является фатальным. На его фоне происходит сбой во всём организме:
Среди сопутствующих хронических болезней, приводящих к кахексии, на первом месте стоят:
Голодание с целью похудения или вынужденный голод, соблюдение изнуря ющих низкокалорийных диет, веганство, недостаточное потребление нутриентов, витаминов, минералов может пагубно сказаться на здоровье и со временем привести к снижению аппетита и развитию анорексии.
Симптомы кахексии
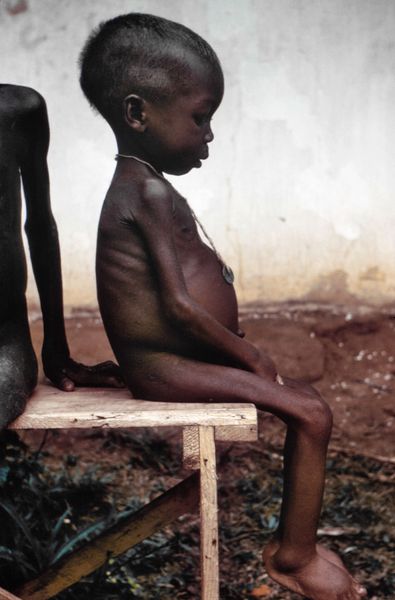
Основной симптом кахексии — резкое снижение массы тела. Вес человека становится на 50 % меньше нормы. Пациент выглядит измождённым, кожа плотно прилегает к костям.
При кахексии больного беспокоят :
Нарушение психического состояния в первую очередь сопровождается синдром хронической усталости — астенией. Человек становится слабым, раздражительным, слезливым, депрессивным. Усиливаются проявления адинамии: резкий упадок сил, мышечная слабость. Это приводит к уменьшению или полному прекращению двигательной активности.
При обострениях основной болезни, ставшей причиной кахексии, может возникнуть аментивное помрачение сознания (бессвязность мышления), которое будет сменяться тревогой, тоскливостью и апатическим ступором.
Патогенез кахексии
Патология пищевого поведения приобретает характер ритуала, сопровождается навязчивыми мыслями о еде. Однако в период наибольшей выраженности нарушения пищевого поведения признаки навязчивости приобретают другой характер. Больной принимает пищу, жуёт, а затем сплёвывает её или вызывает искусственную рвоту.
У пациентов с нервной кахексией обнаруживают следующие симптомы:
Классификация и стадии развития кахексии
В Международной классификации болезней (МКБ-10) выделены три типа кахексии:
Больные с маразмом (алиментарной дистрофией) имеют признаки атрофии скелетной мышечной ткани и подкожно-жировой клетчатки. В то же время функция внутренних органов сохранена. Вес обычно снижен.
В зависимости от причин развития кахексия может быть:
Такж е выделяют три стадии кахексии:
Осложнения кахексии
Как правило, кахексия является осложнением других болезней. Но и сама она тоже может приводить к возникновению ряда заболеваний, таких как:
Вне зависимости от причин, вызвавших кахексию, клинические последствия одинаковы для всех. Они включают в себя следующие проявления:
Своевременно не выявленная и не леченная кахексия может привести к летальному исходу.
Диагностика кахексии
О наличии кахексии свидетельствует нарушение нутритивного (питательного) статуса. Оценить его можно тремя способами:
Определение ИМТ проводится с помощью формулы: ИМТ = вес (кг) / рост 2 (м). Интерпретировать результат можно по приведенной ниже таблице:
Однако по одному ИМТ по дтвердить наличие кахексии у пациента нельзя. Важно учитывать не только низкий вес, но и время, за которое человек его потерял, а также причины похудения. Для этого необходимо тщательно собрать жалобы и анамнез — историю его жизни. Следует уточнить:
Лечение кахексии
Целями лечения кахексии являются:
При определении алгоритма лечения прежде всего необходимо найти первопричинное заболевание, которое послужило развитию кахексии у конкретного пациента:
Пациентам, которые в состоянии принимать пищу, рекомендуется частое употребление высококалорийных продуктов в небольших количествах — яиц, жидких пищевых добавок и др. Хотя данные добавки и увеличение потребляемых калорий положительно влияют на организм, основной процесс кахексии не всегда удаётся остановить, так как она может являться синдромом других заболеваний. Например, кахексия закономерно развиваются у онкобольного.
К стимуляторам аппетита с противо рвотным эффектом относятся каннабиноиды (например дронабинол). Они могут применяться в случае онкозаболеваний. Их приём может осложниться эйфорией, галлюцинациями, психозами, нарушением работы сердечно-сосудистой системы.
В комплексное лечение так же необходимо включать препарат, нормализующий энергию в клетке — гидразина сульфат. Дозировка этого лекарства постепенно увеличивается.
Помимо фармакотерапии, полноценное лечение кахексии включает консультации других специалистов — психотерапевта или психолога, паллиатолога, гастроэнтеролога и др. Они помогут скорректировать факторы, косвенно влияющие на прогрессирование кахексии. С этой целью необходимо подобрать схему противоболевой терапии и назначить различные препараты (по показаниям):
Прогноз. Профилактика
Прогноз кахексии связан с причинным заболеванием или длительным интенсивным воздействием неблагоприятного фактора. В случае кахексии, вызванной онкопроцессом или СПИДом, он будет крайне неблагоприятным. Если же причиной кахексии стало менее опасное заболевание, то она будет лучше поддаваться лечению. Однако оттягивание начала лечения может привести к тяжёлым последствиям. Если же причинное заболевание благополучно удалось разрешить, астения всё равно долгое время будет сохраняться.
Лица, которые склонны к анорексии и кахексии, должны:
Кахексия
Кахексия известна в медицинских кругах еще со времен Гиппократа. Этим термином называют крайне сильное истощение организма человека, осложняющее течение ряда заболеваний, приводя к летальному исходу. У человека наблюдается сильная потеря веса, нарушается обмен веществ, замедляются физиологические процессы. На фоне ухудшения самочувствия изменяется и психическое состояние. Вне зависимости от причин развития недуга проявление симптоматики остается одинаковым. О кахексии в основном идет речь на последней стадии серьезных заболеваний. Речь идет о СПИДе, онкологии, туберкулезе, сепсисе, тяжелых ожогах, при хронической сердечной недостаточности.
Информация о заболевании
Кахексия возникает вследствие сильного уменьшения количества потребляемой пищи и реактивной потери массы тела. Согласно статистике, около 20% онкобольных умирают именно от этого диагноза, а не от канцерогенной опухоли. Заболевание проявляется в виде снижения массы жировой и мышечной тканей. Диагноз ставится пациенту при условии потери массы тела в пределах 50% от исходных значений в течение года. Такой дефицит веса считается в медицине фатальным.
Симптомы заболевания
У заболевания кахексия симптомы проявляются следующие:
Причины возникновения недуга
Заболевание кахексия причины может иметь следующие:
Описание видов заболевания
Признаки кахексии нужно знать, чтобы иметь понятие о возможном изменении состояния человека. В медицинской классификации есть разные формы заболевания с отличающимся патогенезом и механизмом развития. Бывают такие виды кахексии:
Раковая кахексия является распространенным эффектом развивающегося канцерогенного процесса. Характеризуется быстрой потерей веса, а рост опухоли происходит за счет ресурсов организма. Терминальная кахексия возникает из-за недостаточности питания, но вне зависимости от причин болезни всегда наблюдаются инфекции, дисбактериоз, мышечная слабость и др. Гипофизарная и церебральная кахексия возникают в результате нарушения функционирования головного мозга. Если человек стремится сбросить вес, делая это резко и агрессивно, риск возникновения болезни повышается в два раза. Алиментарная кахексия развивается именно по причине неправильного питания. Такого диагноза можно избежать, если не провоцировать организм.
Сердечная кахексия характеризуется снижением способности сердечной мышцы обеспечивать нормальное кровообращение. Кахексия сенильная развивается в пожилом возрасте и сопровождается потерей массы тела. Эта форма болезни является признаком старения. Кахехтиновая разновидность – последствие нарушений в организме из-за туберкулеза или онкозаболевания в анамнезе. Гипоталамическая форма недуга является следствием нарушения белкового обмена и транспорта жиров. Диагноз анорексичной кахексии ставят пациентам, когда наблюдается сбой в работе тонкого кишечника и появляются новобразования, падает уровень сахара в крови.
Возможна ли профилактика кахексии
Кахексия – заболевание, которое можно предупредить. Профилактика заключается в своевременном лечении разных патологий и болезней. Именно они могут стать провоцирующим фактором.
Диагностика и лечение
Для постановки диагноза и анализа состояния пациента назначается ряд анализов и исследований:
Как лечат кахексию
Для заболевания кахексия лечение проводится комплексно. В первую очередь врачу необходимо обеспечить восполнение недостатка питательных веществ в организме. Это сложная задача с учетом того, что у пациентов имеется нарушение работы пищеварительного тракта и отсутствие аппетита. Если у пациента онкология, высококалорийное питание имеет особое значение для восполнения энергии. В систему лечения входят разные виды терапии, что зависит от основного заболевания. Это могут быть антибиотики при наличии инфекции, противогрибковые для лечения стоматита, препараты для восстановления пищеварительных ферментов, усиления аппетита. Один из важных этапов лечения – зондовое питание. Для контроля приема медикаментов, аппетита, питания, устранения побочных эффектов терапия проводится под контролем врачей в стационаре..
Ответы на частые вопросы
Какие основные причины кахексии?
Кахексия является формой сильного истощения организма. Провоцирующим фактором являются различные тяжелые заболевания: онкология, нарушение обмена веществ, голодание, СПИД, туберкулез, сердечная недостаточность, заболевания ЖКТ и др.
Какие врачи лечат кахексию?
Врачи лечат заболевание комплексно. Главные задачи состоят в улучшении качества жизни пациента за счет восстановления питания, восполнения уровня энергии, устранения тошноты, рвоты, обезвоживания и др. Медикаментозная терапия включает в себя антидепрессанты, ферменты, стероиды. Более точная форма лечения подбирается в индивидуальном порядке в зависимости от формы заболевания и сложности его протекания.
Чем опасна кахексия?
Заболевание опасно для жизни. Недомогание, болезненные ощущения, стремительная потеря веса, психические нарушения – часть факторов, которые могут привести к летальному исходу.
Современные подходы к диагностике и лечению синдрома кахексии с позиции врача–терапевта
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Одной из актуальных проблем современной медицины является прогрессирующая потеря массы тела у больных с тяжелой соматической патологией. Известно, что пациенты со сниженной массой тела характеризуются крайне плохим прогнозом: высокой смертностью, частыми госпитализациями, серьезными осложнениями. Даже незначительная потеря массы тела при наличии тяжелых заболеваний может оказать существенное влияние на течение болезни. Так, показано, что при снижении массы тела у стационарного больного всего лишь на 5% продолжительность госпитализации увеличивается в 2 раза, а частота осложнений – в 3,3 раза [1]. Но наибольшую опасность, конечно же, представляет крайняя степень истощения – кахексия.
Кахексия (греч. kachexia = kakos «плохой» + hexis «состояние») – терминальное состояние, осложняющее ряд заболеваний и часто приводящее к гибели больного.
«Плоть исчезает, на ее место выступает влага… плечи, ключицы, грудь, пальцы словно тают. Это состояние – лицо смерти» (Гиппократ).
На фоне успехов в терапии многих неизлечимых ранее заболеваний лечение кахексии представляется не решенной на сегодняшний день проблемой.
Что считать кахексией?
Кахексия может быть установлена в следующих случаях:
• при низкой массе тела (менее 70% от идеальной) или индексе массы тела (ИМТ) (менее 16–17 кг/м2);
• документированном снижении массы тела более чем на 7,5–10% от исходной.
Таким образом, в диагностике кахексии важно учитывать не только низкие весовые показатели, но и скорость снижения массы тела.
Однако однозначных критериев кахексии на сегодняшний день не существует, и в литературе можно встретить различные определения, как и многочисленные синонимы: гипотрофия, белково–энергетическая, питательная или нутритивная недостаточность и др.
Распространенность кахексии
Истинную распространенность недостаточности питания оценить очень сложно, и виной тому следующие причины:
• крайне низкое внимание врачей к состоянию питательного статуса; так, крупное бразильское исследование показало, что массу тела измеряли только у 15,1% больных, при этом недостаточность питания наблюдалась в 48,1%;
• трудности в диагностике потери мышечной массы при сохранении жировой ткани.
Распространенность кахексии будет зависеть прежде всего от нозологии. Так, например, при хронической сердечной недостаточности она составляет от 6 до 16% [2–4]. Однако внедрение в повседневную практику более тонких, хотя и легко выполнимых методов, позволило выяснить, что снижение мышечной массы присуще в той или иной степени примерно 90% больных с признаками ХСН и может иметь место при нормальном или даже повышенном ИМТ [5].
По данным зарубежных исследований, распространенность госпитального голодания чрезвычайно высока и зависит от «профиля» отделения:
• общая хирургия – 40–50%;
• онкология – 50%;
• общая терапия – 48%;
• гастроэнтерология – 65–75%.
Классификация кахексии
По белковым потерям
Безусловно, одной из самых значимых при кахексии является потеря белка. На основании того, какой белок теряется, и строится классификация заболевания. Напомним, что выделяют 2 основных пула белка: соматический (преимущественно периферический белок мышечной ткани) и висцеральный (белки сыворотки крови и внутренних органов)
Согласно международной классификации болезней, различают 3 типа кахексии:
• маразм (истощение соматического пула белка);
• квашиоркор (истощение висцерального пула белка);
• смешанная форма (маразм–квашиоркор).
Квашиоркор – тяжелая форма алиментарной дистрофии, встречается в России довольно редко и преимущественно в результате белкового голодания. Основными характеристиками квашиоркора являются гипопротеинемия, безбелковые отеки и печеночная дисфункция. Масса тела может быть даже повышена за счет отеков и асцита. Квашиоркор распространен в странах Африки, Карибского и Тихоокеанского регионов.
Маразм выражается в истощении энергетических и периферических белковых запасов. Больные с маразмом имеют признаки атрофии скелетных мышц и подкожно–жировой клетчатки при сохранной функции печени и других внутренних органов. Масса тела обычно понижена. Именно этот тип сопровождает многие хронические заболевания.
Сочетанной форме присущи черты как периферического, так и висцерального белкового и энергетического дефицита.
По происхождению
Кахексия может быть первичной (в результате недостаточного потребления пищи) и вторичной (возникает как синдром на фоне других заболеваний).
1) Первичная (экзогенная) кахексия:
• возникает в тех случаях, когда социально–экономические факторы делают невозможным потребление населением достаточного количества пищи хорошего качества. В этих случаях в питании преобладают растительные белки с низкой биологической ценностью. В результате в некоторых странах частота БЭН может достигать 25%.
2) Вторичная (эндогенная) кахексия:
• возникает на фоне острых или хронических заболеваний.
В данной статье мы сознательно не будем касаться первичных вариантов, останавливаясь на вторичных формах, с которыми терапевтам приходится сталкиваться намного чаще.
Основные причины вторичной кахексии
Справедливости ради необходимо отметить, что практически любое хроническое заболевание может привести к прогрессирующей потере массы тела. Однако чаще всего нам приходится сталкиваться с кахексией при следующих болезнях:
• онкологические заболевания;
• гепатиты и циррозы печени;
• заболевания кишечника (болезнь Крона, НЯК, энтериты);
• хронический панкреатит;
• хроническая обструктивная болезнь легких (ХОБЛ);
• хроническая сердечная недостаточность (ХСН);
• последствия травм, ожогов;
• некоторые эндокринные заболевания;
• сепсис;
• туберкулез и другие инфекционные заболевания;
• хроническая алкогольная интоксикация;
• СПИД.
С данными заболеваниями клиницист сталкивается ежедневно. Крайне важно уметь вовремя распознать недостаточность питания и не допустить развития терминальной кахексии.
Клинические последствия кахексии
Вне зависимости от причины, клинические последствия кахексии едины и включают в себя следующие синдромы:
• астено–вегетативный синдром;
• мышечная слабость, снижение толерантности к физической нагрузке;
• иммунодефициты, частые инфекции;
• дисбактериоз (или синдром повышенной контаминации тонкой кишки);
• синдром полигландулярной эндокринной недостаточности;
• жировая дистрофия печени;
• потеря либидо у мужчин, аменорея у женщин;
• полигиповитаминозы.
Влияние кахексии на смертность
Установлено, что масса тела и смертность – взаимосвязанные параметры [6]. Было показано, что смертность резко возрастает при ИМТ менее 19 кг/м2. Дефицит массы тела 45–50% является фатальным.
Патогенез
Механизмы формирования кахексии
Механизмы, приводящие к потере массы тела, можно разделить на несколько групп:
• недостаточное поступление нутриентов (анорексия, болезни ротовой полости, глотки и пищевода и др.);
• нарушения переваривания и/или всасывания (синдромы мальдигестии и мальабсорбции);
• ускоренный катаболизм (у пациентов с ХСН, онкологическими заболеваниями, инфекциями, гипертиреозом, сахарным диабетом и др.);
• повышенные потери нутриентов (при нефротическом синдроме, ХОБЛ, кишечных свищах, плазморея при ожоговой болезни);
• повышенная потребность в нутриентах (во время беременности, лактации, в период реконвалесценции после травм и острых инфекционных заболеваний, после операций).
При многих заболеваниях в формирование кахексии включаются сразу несколько механизмов, что делает их коррекцию особенно сложной.
Механизмы компенсации при голодании
При незначительном дефиците нутриентов включаются механизмы компенсации, которые призваны защитить жизненно важные органы путем перераспределения пластических и энергетических ресурсов. Адаптация происходит через снижение анаболических гормонов (инсулин) и повышение катаболических (соматотропин, глюкагон, адреналин, кортизол)
• Печень обеспечивает до 75% глюкозы за счет распада гликогена.
• Повышается уровень глюконеогенеза, липолиза и кетогенеза (при более длительном голодании).
• Происходит мобилизация энергоресурсов скелетных мышц и жировой ткани. В крови повышаются уровни короткоцепочечных аминокислот (валина, лейцина, изолейцина). Таким образом экономится белок висцеральных органов.
Создается метаболическая ситуация перераспределения ресурсов в пользу инсулиннезависимых тканей (головной и спинной мозг, глазные яблоки, мозговое вещество надпочечников).
У человека с нормальным питательным статусом при полном голодании собственных запасов хватает на 9–10 недель.
Нарушение функций внутренних органов
В период декомпенсации происходит усиление распада белков висцерального пула, что приводит к нарушению функции органов. Уменьшение синтеза белков сыворотки крови в печени приводит к резкому снижению уровня циркулирующих белков. Особенно страдают органы и ткани, представляющие собой депо жиров и углеводов.
• Снижаются сердечный выброс и сократительная способность миокарда. При тяжелой белково–энергетической недостаточности развиваются атрофия и интерстициальный отек сердца.
• Слабость и атрофия дыхательных мышц приводит к нарушению функции дыхания и прогрессирующей одышке.
• Поражение ЖКТ проявляется атрофией слизистой оболочки и потерей ворсинок тонкой кишки, приводящих к синдрому мальабсорбции.
• Снижается число и функциональная способность Т–лимфоцитов, отмечаются различные изменения свойств В–лимфоцитов, гранулоцитов, активности комплемента, что приводит к длительному заживлению ран.
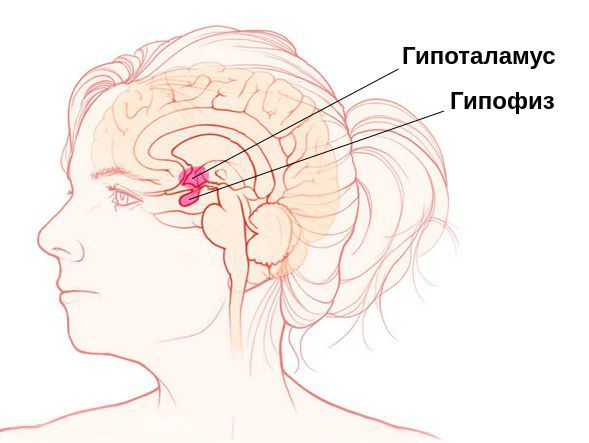
• Особенно страдает функция гипоталамо–гипофизарной системы, чем во многом и обусловлены изменения в организме.
Патогенез некоторых форм
вторичной кахексии
Кахексия при ХСН
Основными причинами снижения массы тела при ХСН являются:
1) анорексия, тошнота и рвота центрального происхождения, а также вследствие дигиталисной интоксикации;
2) мальабсорбция вследствие венозного застоя и фиброза в тонкой кишке;
3) гиперметаболизм. Активация симпато–адреналовой системы неизбежно приводит к преобладанию влияния гормонов катаболизма: в крови у этих пациентов повышен уровень катехоламинов, кортизола. Более того, у данных пациентов гораздо меньше, чем в норме, содержится основных анаболических гормонов – СТГ, половых стероидов. Это приводит к дисбалансу обмена веществ в пользу катаболизма.
Кахексия при онкопатологии
Примерно половина онкологических больных погибает от синдрома CACS (caner – related anorexia – cachexia). При этом причины кахексии множественны:
1) метаболическое обкрадывание организма опухолевыми клетками;
2) мальабсорбция;
3) нарастание концентрации провоспалительных цитокинов (ФНО–a, ИЛ–1, ИЛ–6 и ИФН–g), приводящих к гиперметаболизму. Увеличение уровня этих медиаторов происходит в результате их продуцирования как самой опухолью, так организмом вследствие активации защитных механизмов. При этом уровень провоспалительных медиаторов коррелирует со степенью распространенности опухолевого процесса [7].
4) К похуданию приводит не только сама болезнь, но и ее лечение. Нарушению питания способствуют тошнота и рвота, которые обычно вызываются противоопухолевыми препаратами. Возникает порочный круг: на фоне истощения противоопухолевая терапия более токсична и менее эффективна.
5) Местное воздействие опухоли (дисфагия, стеноз желудка, кишечная непроходимость).
Существует зависимость между локализацией опухоли и степенью белково–энергетической недостаточности. Так, наиболее часто кахексия выявляется у больных с новообразованиями верхних отделов ЖКТ (пищевод, желудок), а также поджелудочной железы и печени – до 80%, легкого – до 60% и молочной железы – 40% [8].
Кахексия при сахарном диабете I типа
Ведущим механизмом катастрофической потери массы тела в этом случае является гастроинтестинальная форма автономной (висцеральной) нейропатии, проявляющаяся дисфункцией пищевода, гастропатией, замедленной эвакуационной функцией желудка, а также диабетическими запором и диареей.
Кроме того, выпадают анаболические функции инсулина в отношении липидов и белков.
Кахексия у пожилых пациентов
В норме возрастные изменения не приводят к развитию кахексии. Тем не менее механизмы, лежащие в основе прогрессивного снижения массы у пожилых пациентов, также представляют некоторый интерес. Начиная с 40–50 лет происходит неуклонное снижение мышечной массы с одновременным увеличением относительной массы жировой ткани (с 25% в 25 лет до 41% в 75). В качестве факторов, ускоряющих эти изменения, принято указывать сидячий образ жизни, а также большое количество социальных и медицинских причин, приводящих к недоеданию.
Единые патогенетические механизмы
вторичной кахексии
Обобщение конкретных механизмов развития кахексии при разнообразных нозологиях позволяет говорить о едином патогенезе данного синдрома. Основополагающими моментами являются активация выработки провоспалительных цитокинов (ФНО–a, ИЛ–1, ИЛ–6), приводящих к анорексии, преобладание эффектов катаболических гормонов (глюкокортикоиды, КА) над анаболическими (СТГ, инсулин, половые стероиды). При этом происходит мобилизация жиров из депо, аминокислот – преимущественно из мышечной ткани и активация глюконеогенеза. Дополнительные нарушения белкового обмена являются следствием либо недостаточного всасывания нутриентов (мальабсорбция), либо их патологической потери.
Отличительные особенности первичной
и вторичной кахексии
Несмотря на общность механизмов формирования кахексии между первичной и вторичной формами существуют некоторые отличия. При первичном голодании адаптивная реакция приводит к уменьшению потребностей внутренних органов в кислороде, при вторичном потребность в кислороде увеличивается. Здесь нет известной стадийности использования запасов энергии. Активируются сразу все процессы катаболизма. Именно этим объясняется преимущественное потребление мышечного белка по сравнению с жировой тканью.
Диагностика питательной
недостаточности
Пациенты с недостаточностью питания встречаются в клинической практике ежедневно, однако ее диагностика достаточно часто осуществляется только на поздних стадиях, когда имеются уже необратимые изменения. Виной тому и недостаточное внимание врачей к питательному статусу, и скрытое течение гипотрофии на начальных этапах.
В современной клинической практике методы оценки питательного статуса подразделяются на несколько групп:
1) клинико–анамнестические;
2) антропометрические;
3) лабораторные.
Антропометрические методы
1) Измерение массы тела (МТ) и индекса массы тела (ИМТ). МТ сравнивается с рекомендуемой МТ в соответствии с формулой Европейской ассоциации нутрициологов:
РМТ (мужчины) = Р – 100 – (Р – 152)*0,2
РМТ (женщины) = Р – 100 – (Р – 152)*0,4
(Р – рост в см).
2) Оценка потери МТ проводилась согласно анамнестическим данным
Потеря считается выраженной, если величина отклонения фактической массы тела от предыдущей составляет: за неделю >2%, за 1 мес. >5%, за 6 мес. >6,5%.
3) ИМТ рекомендован как достоверный показатель состояния питания. ИМТ вычислялся по формуле:
ИМТ = вес (кг)/ рост2 (м2)
Интерпретация результатов проводилась по таблице 1, согласно данным которой, в зависимости от значения ИМТ выделяют несколько степеней недостаточности питания и ожирения.
4) Оценка компонентного состава тела позволяет оценить отдельно мышечную (тощую) и жировую составляющие массы тела. Это особенно важно в ситуациях, когда потеря белка маскируется за избыточной жировой тканью.
Измерение тощей массы тела (ТМТ) производят калиперметрическим методом. С помощью калипера (адипометра) измеряются кожно–жировые складки (КЖС) в 4 стандартных точках: на уровне средней трети плеча над бицепсом, над трицепсом, на уровне нижнего угла лопатки, в правой паховой области на 2 см выше средней пупартовой связки. Затем высчитывается сумма всех 4 складок и определяется жировая масса тела по расчетным формулам.
ТМТ подсчитывается путем вычитания из общей массы тела массы жировой ткани
Нормальным содержанием жира в организме считается для мужчин 15–25%, для женщин 18–30% от общей массы тела, хотя эти показатели могут варьировать. Скелетная мускулатура в среднем составляет 30% от ТМТ, масса висцеральных органов – 20%, костная ткань – 7%.
Лабораторные методы оценки
питательного статуса
Лабораторные исследования дают возможность достаточно полно выявлять нарушения метаболических процессов, т.к. позволяют оценивать как соматический, так и висцеральный пул белка
Определяют следующие показатели:
• альбумин;
• трансферрин;
• транстирретин;
• ретинолсвязывающий белок.
Наиболее информативными показателями являются последние три. Благодаря короткому периоду полураспада концентрация в плазме крови этих белков быстро изменяется в зависимости от направленности метаболических процессов.
Также определяют иммунологические показатели:
• абсолютное количество лимфоцитов;
• кожную реакцию на введение антигена.
Степень недостаточности питания оценивается в соответствии с рекомендациями Европейского общества парентерального и энтерального питания (ESPEN) (табл. 2).
Лечение кахексии
К сожалению, до сих пор не существует единого подхода к лечению кахексии. Были предприняты многочисленные попытки коррекции этого состояния, включающие в себя:
1) рекомбинантный гормона роста;
2) стимуляторы аппетита: антагонисты серотонина, прогестагены, дронабинол;
3) антицитокиновые препараты (ГКС, пентоксифиллин, мелатонин, талидомид);
4) ингибиторы глюконеогенеза (гидразина сульфат).
Практически все вышеуказанные препараты были изучены в крупных многоцентровых исследованиях, результаты которых оказались весьма противоречивы.
Нутритивная поддержка
Полноценное питание составляет основу жизнедеятельности организма человека и является важным фактором обеспечения резистентности к патологическим процессам различного генеза. Клинический опыт свидетельствует о том, что одно из центральных мест в лечении тяжелых хронических заболеваний занимает коррекция кахексии и полноценное обеспечение энергетических и пластических потребностей.
При этом поступление питательных веществ может осуществляться энтеральным или парентеральным путем.
1. Энтеральное питание (ЭП)
Энтеральное питание – система назначения питательных смесей, пищевых продуктов, подвергнутых предварительной обработке для обеспечения высокой усвояемости. Это наиболее физиологичный способ введения пищевых веществ в организм.
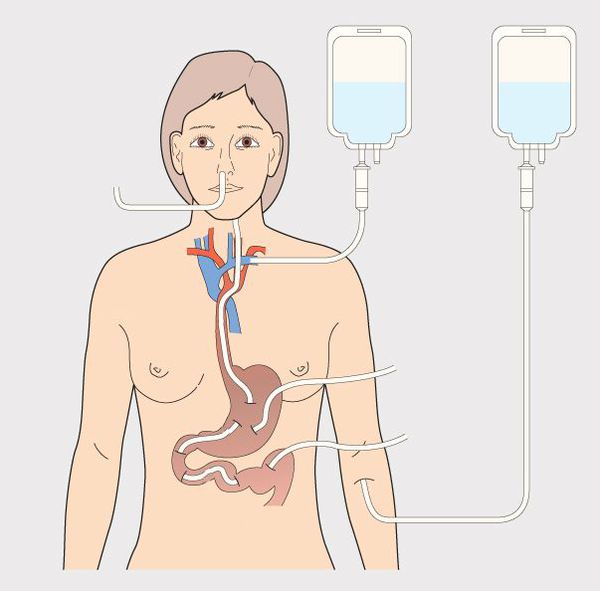
Проведение ЭП возможно per os, а также с использованием назогастрального или назоеюнального доступа. Выбор доступа определяется наличием у больного возможности самостоятельно питаться и отсутствием у него признаков дисфагии.
Смеси для ЭП
Современные смеси в зависимости от состава и предназначения можно разделить на несколько видов. [9].
Элементные диеты (химусоподобные), состоящие из мономеров – аминокислот, жирных кислот, глюкозы и фруктозы – и предназначенные для внутрикишечного введения. Недостатком этих смесей является их высокая осмолярность более 700 мосм/л, что приводит к осмотической диарее. Сейчас эти смеси применяются крайне редко.
Полуэлементные смеси, состоящие из белковых гидролизатов – олигопептидов, ди– и моносахаров, длинно– и среднецепочечных триглицеридов, а также микроэлементов и витаминов. Эти смеси быстро и полностью усваиваются и в отличие от элементных не приводят к развитию осмотической диареи.
Высокомолекулярные сбалансированные смеси. Это наиболее распространенные в настоящее время препараты. Содержат все компоненты питания, сбалансированные в соответствии с суточными потребностями. Углеводы обычно представлены мальтодекстрином и дисахаридами, жиры – соевым и другими растительными маслами, являющимися источником среднецепочечных триглицеридов. Белки – цельные или низкомолекулярные – казеинаты, молочный и яичный альбумин, соевые изоляты.
Смеси направленного действия – рассчитанные на определенный вид патологии; предназначаются для коррекции метаболических нарушений при почечной, печеночной, сердечной недостаточности, сахарном диабете и других состояниях.
Выбор смеси:
А) При сохранной функции ЖКТ (нарушения питательного статуса не являются критичными) предпочтение следует отдавать полуэлементным смесям. Они прекрасно переносятся и являются наиболее физиологичными.
Б) При патологии ЖКТ, когда частично нарушены процессы переваривания или всасывания, начинать коррекцию питания необходимо с олигомерных смесей, обладающих максимальной способностью к усвоению. Такая ситуация может сложиться при энтеритах, ХСН (венозный застой и фиброз кишечной стенки), болезнях печени и поджелудочной железы и др.
В) Вопрос о парентеральном питании ставится при выраженной кахексии, когда применение лишь энтеральных смесей недостаточно и неэффективно.
2. Парентеральное питание (ПП)
Парентеральное питание (ПП) – способ обеспечения больного питательными веществами, минуя ЖКТ. При этом специальные инфузионные растворы, способные активно включаться в обменные процессы организма, могут вводиться через периферическую или центральную вену.
Современные достижения в области ПП позволяют широко использовать этот метод не только для коррекции питательной недостаточности при нарушениях ЖКТ, но и для длительной поддержки питательного статуса у больных с соматическими, онкологическими, психическими или инфекционными заболеваниями, а также у получающих агрессивные методы лечения (химиолучевая терапия и т.д.).
Понимание единых механизмов развития кахексии, учет явлений гиперметаболизма позволили разработать современные смеси, содержащие необходимый набор ингредиентов не только для коррекции питательного статуса, но и для непосредственного воздействия на патогетические звенья кахексии Современные растворы для ПП обладают широким спектром фармакологического действия на системном, органном, клеточном и субклеточном уровнях. ПП может быть полным или частичным.
При полном ПП применяют препараты, обеспечивающие энергетические и пластические потребности организма – аминокислотные растворы, жировые эмульсии и растворы углеводов.
Частичное ПП носит вспомогательный характер, применяется для решения проблем недолгосрочной нутритивной поддержки организма, включает отдельные питательные компоненты
При ПП прежде всего необходимо введение аминокислот, которые участвуют в метаболизме белка, непрерывно подвергающегося обновлению. Показано, что ряд аминокислот, входящих в растворы для ПП, активно стимулируют органные метаболические процессы.
В зависимости от тяжести патологического процесса белки организма катаболизируются в количестве 75–150 г/сутки. Разрушение белков ведет к определенному дефициту незаменимых аминокислот, к отрицательному азотистому балансу, даже если потери белка компенсируются. Последствиями дефицита белков являются дисфункция органов и систем, замедленное выздоровление, ослабление репаративных процессов, снижение сопротивляемости организма к инфекциям, анемия.
Различают заменимые аминокислоты, недостаток которых может быть восполнен за счет эндогенного образования, и незаменимые аминокислоты, образования которых в организме не происходит и которые должны поступать в организм извне. Однако существуют так называемые условно незаменимые аминокислоты (аргинин и гистидин), которые оказывают значимое влияние на синтез белка.
В настоящее время созданы препараты, содержащие сбалансированную смесь незаменимых и заменимых аминокислот, которые при внутривенном введении включаются в биосинтез белков и устраняют белковый дефицит.
3. Смешанное питание
Основным недостатком ПП является развитие дистрофических изменений слизистой оболочки кишечника вследствие отсутствия поступления питательных веществ. Это увеличивает риск возникновения инфекционных осложнений на фоне синдрома транслокации бактерий. Возможным решением данной проблемы является использование комбинированной формы нутритивной терапии, когда на фоне полного парентерального питания сохраняется незначительное поступление питательных веществ через ЖКТ для предотвращения развития атрофических изменений слизистой оболочки кишечника.