Что такое мультифокальный рост опухоли щитовидной железы
Рак узлов щитовидной железы
«Клиника щитовидной железы» доктора А.В. Ушакова предлагает высоко профессиональную помощь в экспертной оценке рака щитовидной железы.
Рак щитовидной железы ― формирование нетипичной ткани внутри узлов железы, с изменением качественных признаков клеточного состава и его структуры. Злокачественный процесс в узлах образуется в результате нарушения в системе иммунного контроля при интенсивном размножении клеток. В результате складывается матричная ветвь клеток с совершенно другими свойствами. В зависимости от источника клеток и выраженности их отличия от основного здорового клеточного состава, различается несколько вариантов рака в щитовидной железе. Помните: рак бывает только в узлах железы, вне узлов рака нет.
Основные варианты рака щитовидной железы
Папиллярный рак ― наиболее часто встречающийся злокачественный процесс щитовидной железы. По данным разных исследователей, частота папиллярного рака составляет около 70-80% от всех случаев тиреоидной злокачественности. При этом папиллярный рак является наименее агрессивным. Узлы с таким раком могут многие годы присутствовать в железе, никак не проявляя себя и не распространяя свою ткань за пределы узловой границы. Метастазирование при этом раке не характерно.
Фолликулярный рак щитовидной железы встречается реже папиллярного (почти в 10-15% среди всех вариантов злокачественности). Это более активный тканевой процесс. При фолликулярном раке на стадиях активного развития может наблюдаться прорастание ткани из узла, а также присутствует вероятность метастазирования раковых клеток в лимфоузлы.
Медуллярный рак образуется, в отличие от двух первых вариантов, из С-клеток, участвующих в продукции кальцитонина ― гормона, регулирующего кальциевый обмен. Вот почему при выявлении узлов предлагается проведение анализа крови с оценкой концентрации кальцитонина. Это более агрессивная форма рака, но встречаемость его очень мала (1-3%). Медуллярному раку свойственно метастазирование.
Анапластический рак является самым активным и потому агрессивным. Встречается реже других вариантов рака. Метастазирование при этом случае рака значительно выражено.
Диагностика рака щитовидной железы
Рак щитовидной железы обычно не имеет симптомов. Содержание популярных статей вида «10 симптомов рака щитовидки», как правило, не соответствуют реальности. Лишь крайне редко и в очень запущенных случаях агрессивных вариантов рака щитовидной железы может быть охриплость голоса из-за раздражения возвратного нерва. Выступание наружу узла железы ― не признак рака.
Только 4% узлов щитовидной железы, выявляемых при УЗИ, оказываются раком. Тем не менее, каждый узел требует внимательного исследования для исключения или подтверждения злокачественного процесса.
В настоящее время распространены и применяются два способа диагностики рака узлов щитовидной железы ― УЗИ и цитологическое исследование после пункционной биопсии. Ультразвук служит для выявления узла и оценки его качеств. Результат УЗИ помогает определиться с показанием к диагностической пункции узла. При таком показании (в 80-90% случаях) пациенту рекомендуется пункция узла, получение элементов ткани (биопсия) и последующее цитологическое исследование под микроскопом (осуществляет врач-морфолог).
Кроме указанных способов, существует геномный способ диагностики щитовидного рака. Одним из вариантов этого исследования является методика Afirma Genomic Sequencing Classifier (GSC), позволяющий достовернее выявлять рак узлов щитовидной железе по сравнению с предшествовавшим вариантом ― Afirma Gene Expression Classifier (GEC).
Предполагается, что геномная диагностика рака подходит для тех случаев диагностики, когда после УЗИ и цитологического исследования биоптата был получен сомнительный вывод.
И всё же, геномная методика Afirma GSC не обладает 100% результатом. Её применение лишь на несколько процентов повысило вероятность подтверждающего ответа, достигнув лишь 91% по уровню чувствительности теста. В результате, среди узлов, «подозрительных» на вероятность рака, геномная методика окажет помощь с точностью до 68%.
TI-RADS в диагностике рака
УЗИ при раке щитовидной железы
УЗИ представляет не только первый, но и наиболее важный способ диагностики рака. Очень многое в этом исследовании зависит от знаний, опыта и внимания специалиста. Не следует пренебрегать возможностями УЗИ в пользу цитологической диагностики и полностью полагаться на последнее, которое часто бывает малоконкретным.
В настоящее время различают 5 ультразвуковых признаков злокачественности узла. Их выраженность, сочетание и количество в определенной мере будут указывать на вероятность рака.
1. Изменение границы узла. Врач должен внимательно во всех проекциях рассмотреть границу узла и оценить, насколько она заметная, равномерная и чёткая. При отсутствии явной границы (плавном переходе ткани узла в окружающую ткань), её извитости, присутствии заметных выступов и т.п. можно предположить активный внутриузловой процесс и прорастание ткани из узла.
2. Гипоэхогенная ткань в узле (темная ткань). Размножение клеток в узле (пролиферация) может приводить к формированию плотных клеточных масс, которые при УЗИ становятся заметны в виде гипоэхогенности, т.е. более темного фона. Это явление может быть вызвано совершенно иным, а именно доброкачественным процессом, исходящим от проникновения (инфильтрации) лимфоцитов или микрофолликулярной ткани аденомы. Важно обращать внимание на форму и границы этой гипоэхогенной зоны. При её плавном равномерном крае, постепенно переходящим в остальную ткань узла или ограниченной пределом узлового сегмента, процесс является доброкачественным. Важно не путать гипоэхогенность и анэхогенность.
3. Микрокальцинаты. Это явление заметно в виде множества мелких светлых точек среди ткани узла. Эти образования могут не распространять гипоэхогенную тень от ультразвукового датчика. Но не все светлые точки и линии являются микрокальцинатами. Помните, что врач должен суметь отличить их от мелких скоплений коллоида и от уплотнения соединительной ткани. Иначе, приняв последние два варианта за микрокальцинаты, может быть выявлена высокая вероятность рака и даже назначена операция.
4. Несоответствие формы узла форме доли. В этом случае при УЗИ щитовидной железы передне-задний размер узла будет больше его других размеров. Иначе говоря, наибольший размер узла будет располагаться не вдоль доли, а поперек. Такая особенность указывает на незакономерный рост клеток. Форма (соответственно и размеры) доброкачественных узлов стремится к правильной (сфере или эллипсу). Ткань в доброкачественных узлах разрастается или равномерно (способствуя сферичности), или в направлении полюсов доли (т.е. вдоль, а не поперек доли).
5. Неупорядоченный кровоток в узле. В допплеровских режимах УЗИ (при ЦДК или ЭДК) врач должен проверить особенности кровотока. Понятие «смешанный» кровоток не несет пользы в оценке рака узла. Смешанный кровоток (т.е. по краю и внутри узла) случается при всех узлах и поэтому не может указывать на вероятность злокачественности. Напротив, упорядоченность сосудистой сети узла может свидетельствовать как в пользу доброкачественности, так и ориентировать в вероятности рака узла. Под упорядоченностью кровотока понимается распределение сосудов преимущественно по границе сегментов (т.е. вокруг узла и внутри него в области перегородок между его частями).
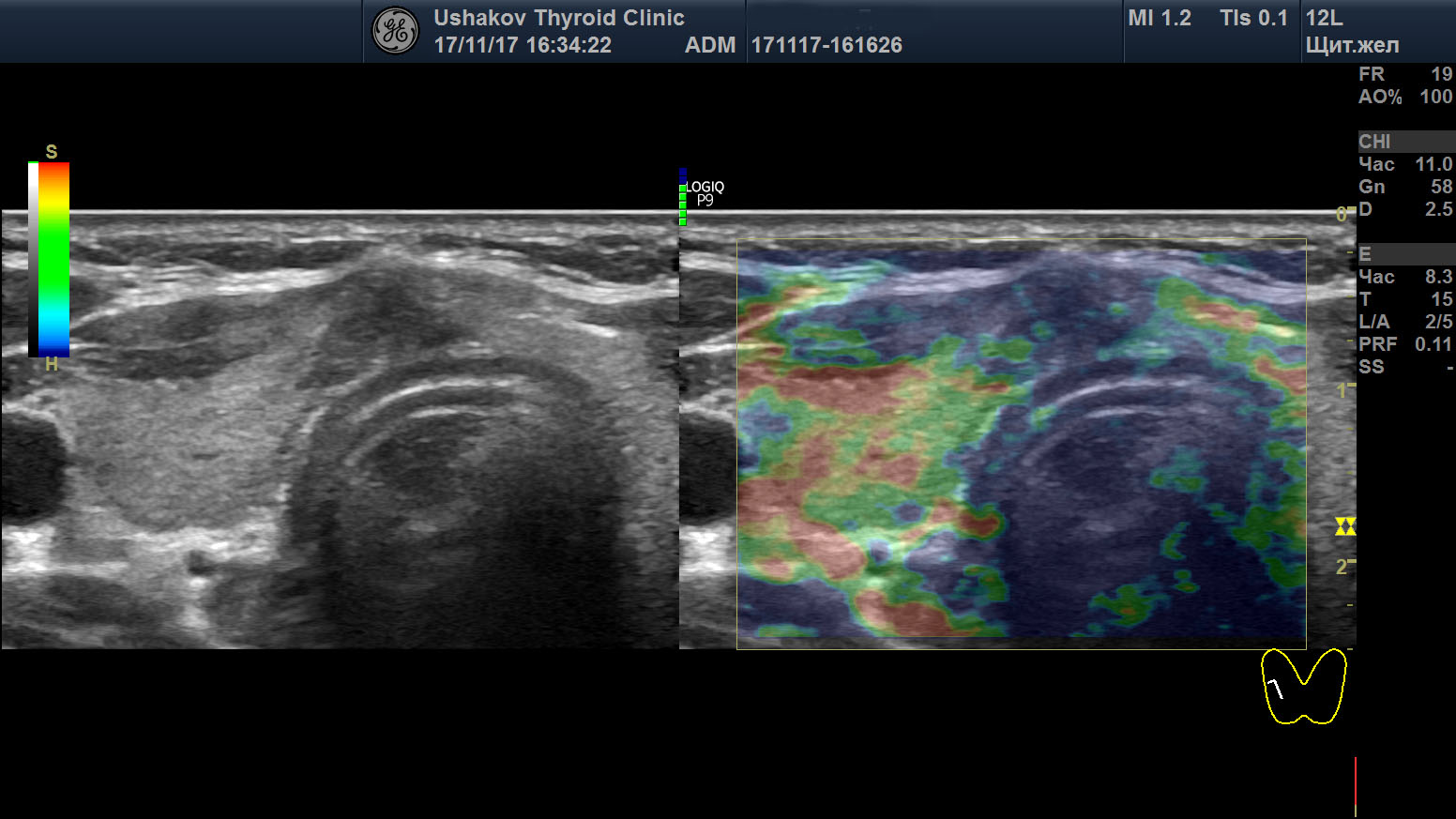
 |  |
| Рисунок 1. В правой части перешейка щитовидной железы узел с признаками рака: 1) неправильная форма, вытянут не вдоль, а поперёк перешейка, 2) содержит значительно гипоэхогенную ткань, 3) граница узла в некоторых участках прерывистая. Класс по TI-RADS соответствует 4С. | Рисунок 2. Этот же узел в режиме ЭДК. Кровоток узла значительной интенсивности с признаками неупорядоченности распределения сосудов. |
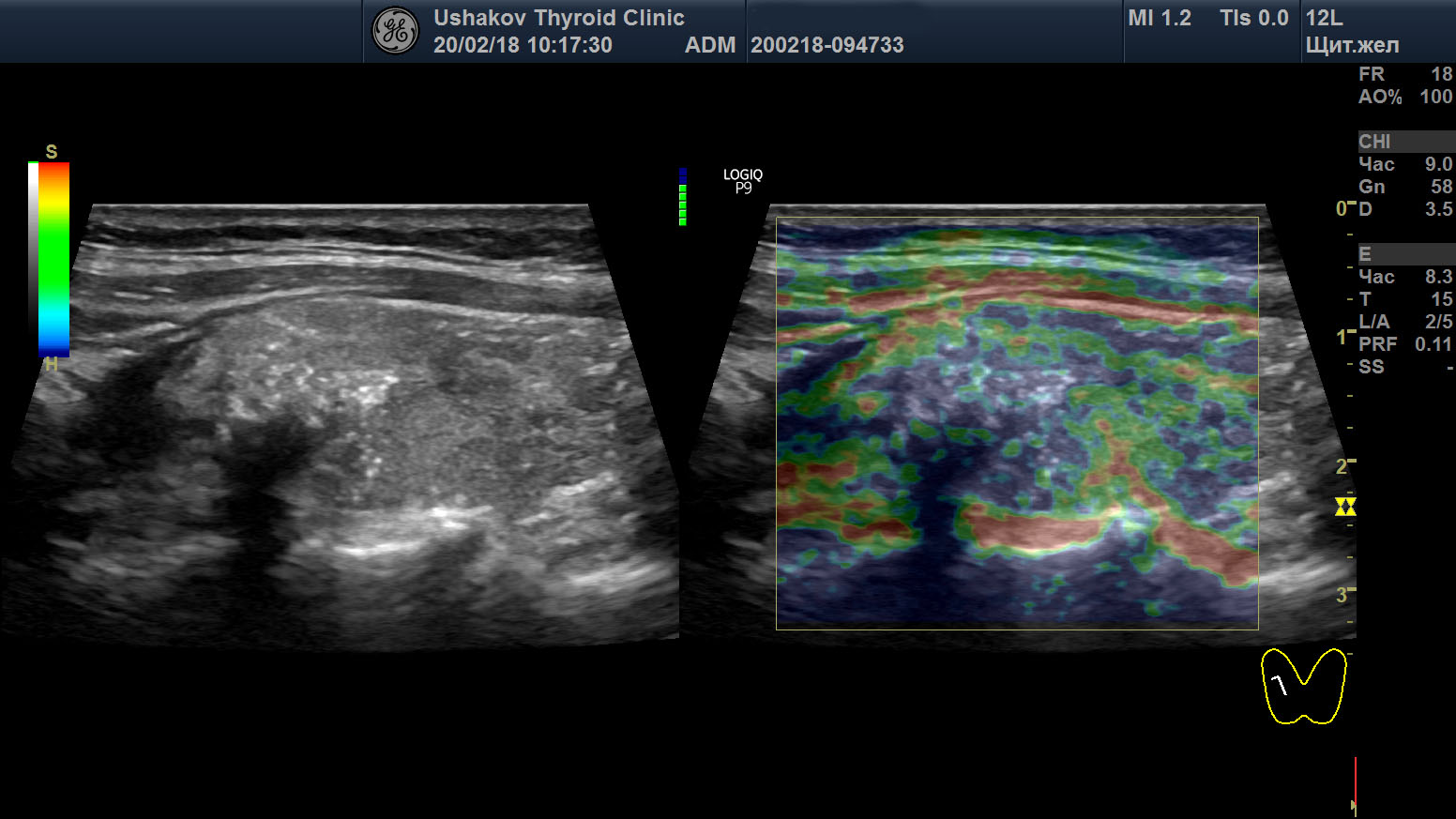
Рисунок 3. Этот же узел в режиме компрессионной эластографии. Значительно увеличена жесткость узловой ткани ― признак плотного расположения клеток в ткани узла (свойственно злокачественности).
Важные требования при УЗИ. При выявлении узла или узлов в щитовидной железе врач-сонолог должен внимательно исследовать все узлы, оценив их качества по указанным пяти признакам. В случае присутствия одного или большего количества таких признаков или в случае сомнений, а также при контрольном (проверочном) УЗИ после выявленного другим врачом «рака узла», специалист должен описать в «Протоколе УЗИ щитовидной железы» все 5 признаков (показав доброкачественные или злокачественные свойства). В разделе «Заключение» медицинского документа «Протокол УЗИ щитовидной железы» каждый узел должен быть оценён классом по системе TI-RADS.
Классификация узлов TI-RADS
Классификация узлов TI-RADS (по J.Y. Kwak et all., 2011) создана для определения показания к проведению пункционной биопсии. Диагностика узлов по TI-RADS ― не оценка рака и не «приговор», как могут думать пациенты. TI-RADS ― это интеллектуальный инструмент врача в: 1) характеристике узлов щитовидной железы с позиции вероятности рака в системе передачи информации от одного врачу другому и 2) формировании показания для пункционной биопсии.
| TI-RADS | Признаки | Вероятность рака |
| 1 | норма (макроструктурна полноценность) | 0% |
| 2 | доброкачественные | 0% |
| 3 | возможно доброкачественные | 0-4% |
| 4А | 1 признак рака | до 10% |
| 4В | 2 признака рака | 10-80% |
| 4С | 3 или 4 признака рака | 80% |
| 5 | 5 признаков рака | >80% |
| 6 | цитологическое подтверждение рака | >90% |
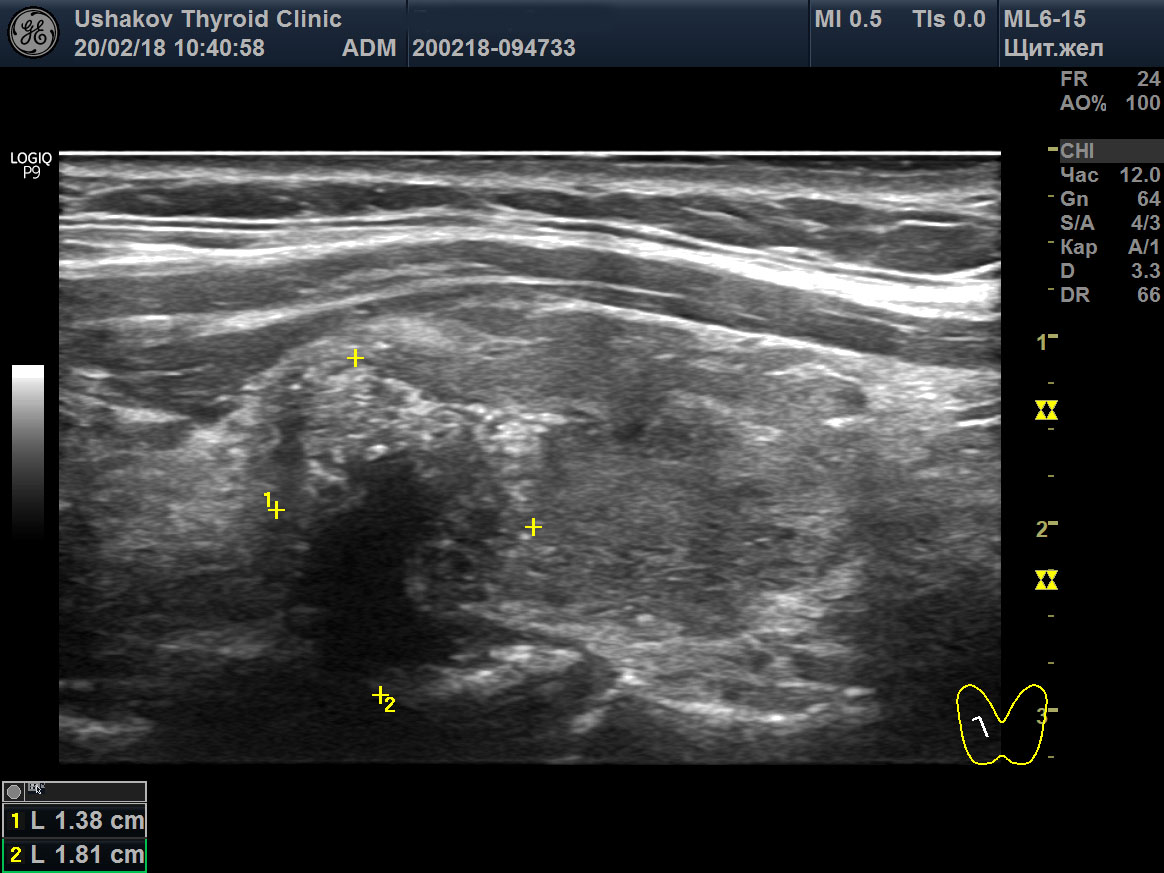 | 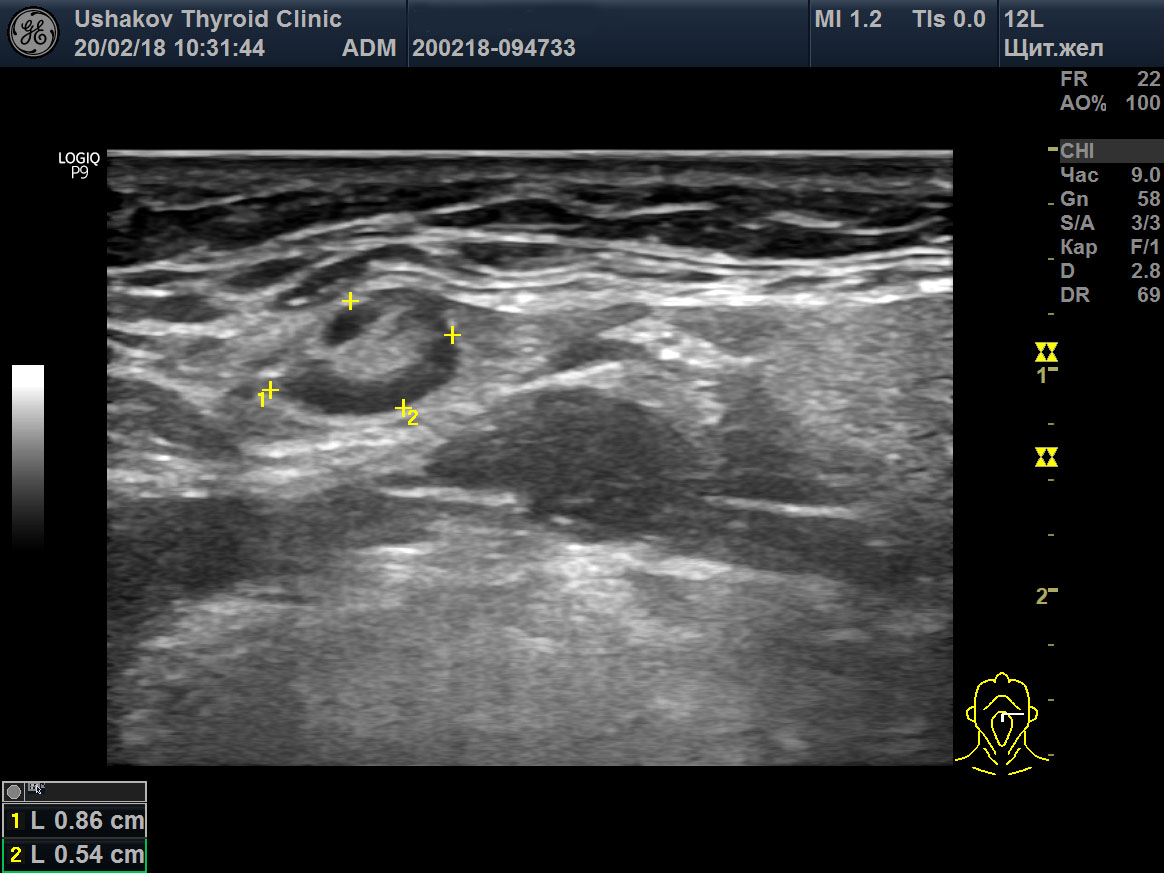 |
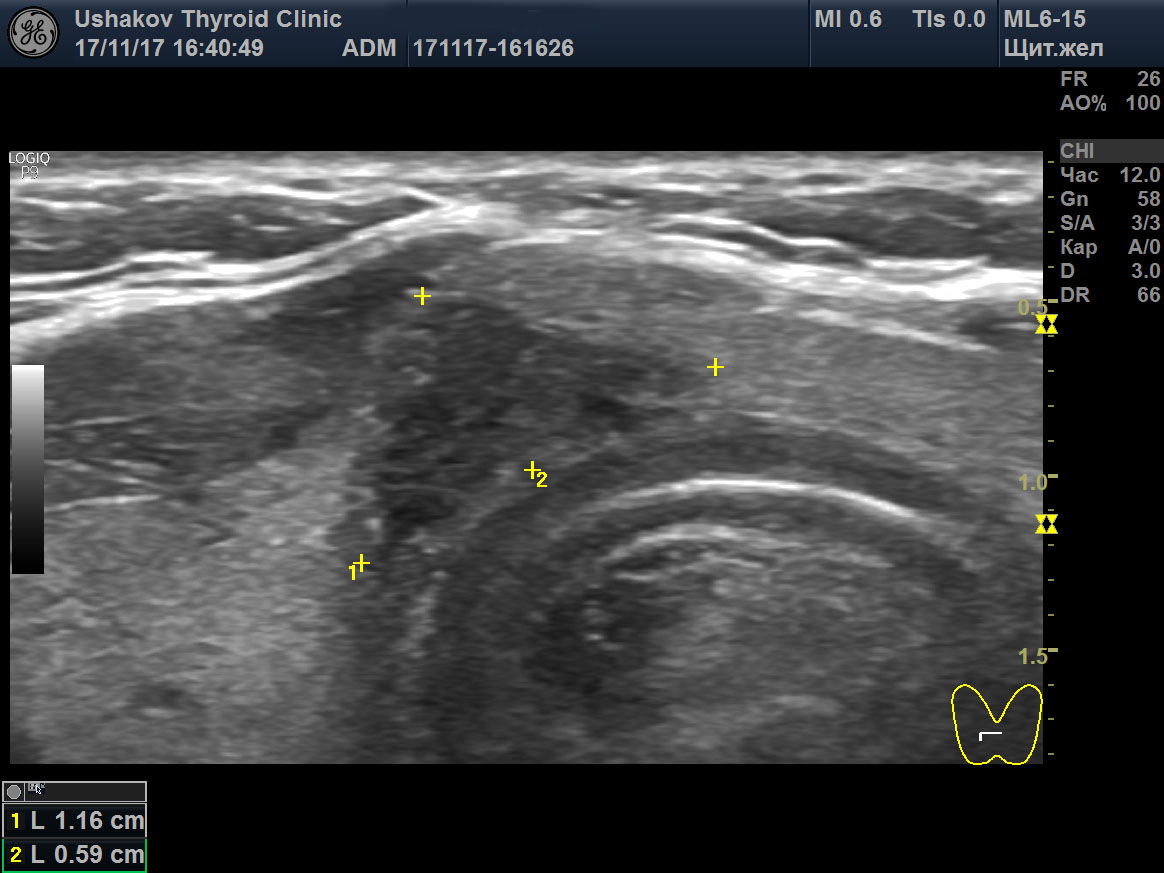
| Рисунок 4. Узел верхней (краниальной) части правой доли щитовидной железы (ограничен желтыми метками). Признаки рака узла: 1) неправильная форма, 2) неравномерный край узла, местами прерывистая граница, 3) значительно гипоэхогенная (темная) зона внутри узла, постепенно переходящая в остальную ткань, 4) микрокальцинаты. Класс по TI-RADS соответствует 4С. | Рисунок 5. Изменённый регионарный лимфатический узел. Отношение сторон меньше коэффициента 2 (округлый), внутри определяется значительное разрастание ткани (признак метастазирования). |
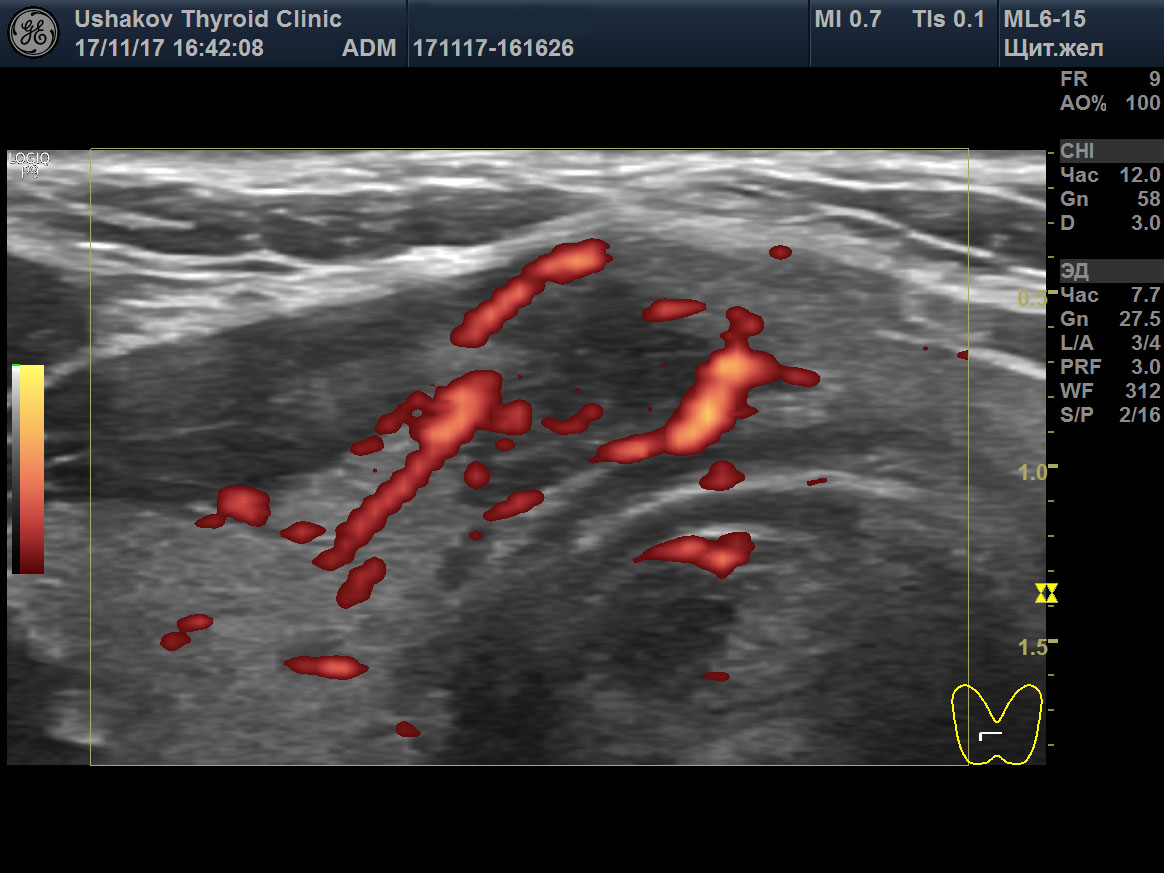
Рисунок 6. Этот же узел в режиме компрессионной эластографии. Значительно увеличена жесткость узловой ткани ― признак плотного расположения клеток в ткани узла и её разрушения с накоплением жидкости (свойственно злокачественности). Микрокальцинаты определяются в виде скоплений мелких белесых точек.
Цитологическая диагностика проводится после пункционной биопсии узла щитовидной железы (обязательно под контролем УЗИ!). В результате пациенту предоставляется медицинский документ «Протокол цитологического исследования». В этом документе, помимо анкетных данных и мест забора материала из узла или узлов, должны находиться два раздела ― «Описание» и «Заключение».
Протокол без «Описания» мало информативен и потому не имеет реальной клинической пользы. Дело в том, что только по данным подробного описания того, что врач-морфолог увидел в микроскоп, можно сделать вывод о реальности рака или его отсутствии. Из «Описания» следует краткий вывод ― «Заключение», но из «Заключения» никакое «Описание» не создать. Если в «Заключении» лишь предполагается рак (например, «фолликулярная опухоль» и/или класс Батесда 4), то оценить его реальность можно только по данным «Описания»! Требуйте от врача соблюдения оформления медицинской документации. Это в ваших собственных интересах.
Обращайте особое внимание на стиль текста «Протокола цитологического исследования. Есть уверенность ли предположение (подозрение)? На каких конкретных признаках основано одно или другое? Что это за признаки ― общие (неконкретные) или чётко указывающие на определённое изменение?
В случаях предположительности и неточности обязательна дополнительная диагностика. Лучше в другом медучреждении у другого специалиста. Впрочем, контрольную диагностику желательно проводить в любом случае, для того, чтобы убедиться в достоверности диагноза.
Восемь важных советов
2. Заранее поясняйте специалисту перед диагностической процедурой свои требования к результату исследования. Это относится к данным УЗИ и, особенно, ― к «Протоколу цитологического исследования биоптата щитовидной железы».
3. Во время УЗИ, в случае выявления узлов, специалист должен исследовать регионарные лимфатические узлы шеи. Обратите на это внимание.
4. Вместе с протоколом УЗИ, как минимум, обязательно должны быть представлены снимки узла (или узлов) в двух основных проекциях и в режиме ЦДК (или ЭДК). Это современное требование к формированию «Протокола УЗИ щитовидной железы» (себестоимость одного снимка мала; не превышает 10-15 руб.).
5. После получения диагностического «Протокола» внимательно изучите его. Проверьте присутствие в нем нужных пунктов и их содержание. Заранее изучите, что именно должно быть в разделах «Протокола».
6. Помните, что «атипичными клетками» могут являться доброкачественные клетки, измененные в результате перенапряжения.
7. Увеличение тиреоглобулина по данным анализа крови не является маркером рака. Поэтому не следует беспокоиться при увеличении значения этого показателя. Тиреоглобулин постоянно выделяется из щитовидной железы в кровь вместе с гормонами (Т4 и Т3). Увеличение концентрации тиреоглобулина ― признак интенсивной деятельности ткани или её разрушения. Может быть увеличена при разрушении ткани доброкачественного узла и при подостром тиреоидите.
8. Вы всегда можете получить второе профессиональное мнение. При необходимости, сделайте контрольное УЗИ щитовидной железы. Нередко случается, что врачи при УЗИ принимают за узлы очаговые диффузные образования (в таком случае пациенту напрасно проводится пункционная биопсия), или доброкачественные признаки трактуются как злокачественные.
«Клиника щитовидной железы» доктора А.В. Ушакова предлагает высоко профессиональную помощь в экспертной оценке рака щитовидной железы.
Что такое мультифокальный рост опухоли щитовидной железы
ФГУ Эндокринологический научный центр, Москва
Новая международная гистологическая классификация опухолей щитовидной железы
Журнал: Архив патологии. 2018;80(1): 37-45
Абросимов А. Ю. Новая международная гистологическая классификация опухолей щитовидной железы. Архив патологии. 2018;80(1):37-45.
Abrosimov A Iu. The new international histological classification of thyroid tumors. Arkhiv Patologii. 2018;80(1):37-45.
https://doi.org/10.17116/patol201880137-45
ФГУ Эндокринологический научный центр, Москва
В 2017 г. Международное агентство по изучению рака (МАИР) выпустило в свет новое 4-е издание Классификации ВОЗ опухолей эндокринных органов. Как и в предыдущем издании 2004 г., в новой классификации значительное внимание уделено новообразованиям щитовидной железы (ЩЖ). В номенклатуре опухолей ЩЖ произошли изменения, основанные на полученных за истекший период результатах клинических морфологических и молекулярно-генетических, исследований и соответствующих новых взглядах на злокачественный потенциал и прогноз ряда новообразований, которые следует учитывать патологоанатомам в повседневной диагностической практике. Целью настоящей публикации является представление новой классификации опухолей ЩЖ с акцентом на внесенные изменения.
ФГУ Эндокринологический научный центр, Москва
Новое издание Классификации ВОЗ опухолей эндокринных органов [1] отражает согласованное мнение 166 экспертов международной рабочей группы, принятое на заседании редакции МАИР в Лионе, Франция, 26—28 апреля 2016 г. Редакторами издания являются R.V. Lloyd, R.Y. Osamura, G. Klöppel, J. Rosai. В предисловии к главе, посвященной опухолям щитовидной железы (ЩЖ), J. Rosai процитировал всемирно известного патолога P. Masson [2], написавшего в своем научном труде «Human tumors», что «Нет более трудной задачи, чем разработка классификации карцином щитовидной железы…», и «…из всех карцином они (карциномы щитовидной железы), вероятно, преподносят гистопатологам самые большие уроки…».
Выход в свет нового издания классификации обусловлен научными достижениями последних лет по ряду направлений исследования тиреоидного канцерогенеза, главным из которых является раскрытие молекулярно-генетических особенностей высокодифференцированных опухолей ЩЖ, имеющих фолликулярное строение и развивающихся из фолликулярного эпителия. Понимание молекулярных механизмов опухолевого роста позволило пролить свет на различия, дающие теоретические и практические основания для выделения классификационных категорий папиллярного и фолликулярного, доброкачественного и злокачественного типов новообразований. Вместе с тем остаются дискуссионными вопросы относительной диагностической значимости формирования опухолью сосочковых структур и установления особых изменений ядер опухолевых клеток, характеризующих папиллярную карциному. Для высокодифференцированных инкапсулированных опухолей фолликулярного строения капсулярная и/или сосудистая инвазия остается главным диагностическим критерием злокачественности. Камнем преткновения прошлого издания классификации стали категории инкапсулированных опухолей фолликулярного строения, занимающих промежуточное положение между фолликулярными аденомами и фолликулярными карциномами («фолликулярные новообразования неопределенного злокачественного потенциала»), фолликулярными аденомами и фолликулярным вариантом папиллярного рака («высокодифференцированные новообразования неопределенного злокачественного потенциала»), которые были лишь упомянуты, но не рекомендованы в качестве категорий для широкого использования [3]. Напротив, эксперты ВОЗ справедливо рекомендовали проводить тщательное гистологическое исследование адекватного количества образцов опухолевой ткани, особенно периферических отделов инкапсулированных новообразований фолликулярного строения, с целью получения оснований для более категоричного заключения о доброкачественном и злокачественном характере опухоли. Вместе с тем категории пограничных опухолей («серой зоны», или опухолей неопределенного злокачественного потенциала) используют в классификациях новообразований других органов. В новой классификации опухолей ЩЖ принципиальный вопрос о том, являются ли пограничные опухоли отдельными категориями (должны ли быть классифицированы как карциномы или как новообразования с низким злокачественным потенциалом), получил свое дальнейшее развитие. В разделе классификации, озаглавленном «другие инкапсулированные опухоли щитовидной железы фолликулярного строения», после соответствующего предисловия, сделанного J.K.C. Chan, Y.E. Nikiforov, G. Tallini, выделены две категории опухолей неопределенного злокачественного потенциала («фолликулярная опухоль неопределенного злокачественного потенциала» и «высокодифференцированная опухоль неопределенного злокачественного потенциала») и одна новая категория пограничных опухолей, названная «неинвазивная фолликулярная опухоль с изменениями ядер опухолевых клеток папиллярного типа» (non-invasive follicular thyroid neoplasm with papillary-like nuclear features). Последней из перечисленных категорий в предыдущей гистологической классификации не было, в новой номенклатуре опухолей ей присвоен код 8349/1. Следует заметить также, что ранее гиалинизирующая трабекулярная опухоль была отнесена в группу аденом и аналогичных им опухолей с гистологическим кодом 8336/0, что означало доброкачественность новообразования. В новой классификации «гиалинизирующая трабекулярная опухоль» поименована отдельно после фолликулярной аденомы и имеет код 8336/1, что означает неуточненный, неопределенный злокачественный потенциал или пограничную опухоль. В табл. 1 представлена

Кроме выделения группы «другие инкапсулированные опухоли фолликулярного строения», состоящей из трех категорий с соответствующими классификационными кодами, а также изменения гистологического кода «гиалинизирующая трабекулярная опухоль», выделен ряд гистологических вариантов папиллярного, фолликулярного рака и отдельно онкоцитарных (Гюртле-клеточных) опухолей.
Представляется целесообразным остановиться подробнее на наиболее распространенных диагностических категориях, интерпретация которых претерпела изменения по сравнению с предыдущим изданием классификации.
Фолликулярная аденома определена как доброкачественная инкапсулированная неинвазивная опухоль, демонстрирующая признаки фолликулярно-клеточной дифференцировки при отсутствии изменений ядер опухолевых клеток, характерных для папиллярной карциномы. В отличие от гиперпластического неопухолевого узлового поражения фолликулярная аденома характеризуется моноклональным клеточным составом. В связи с тем что без молекулярно-генетического исследования установить клональность затруднительно, возникают трудности дифференциальной диагностики аденомы и гиперпластических неопухолевых узловых образований. Многие патологоанатомы при многоузловом поражении ЩЖ не ставят диагноз аденомы, а лишь констатируют наличие гиперпластического процесса и отсутствие признаков злокачественности. Гистологическое исследование позволяет установить опухоль, окруженную собственной фиброзной капсулой. Строение аденом широко варьирует: нормо-, макро-, микрофолликулярное, солидное и трабекулярное. В одной опухоли могут быть представлены несколько структурных компонентов. Редко аденомы имеют сосочковое и инсулярное строение. В пояснительном тексте новой классификации упомянуты следующие варианты аденом: гиперфункционирующая (токсическая или горячая) аденома, аденома с сосочковой гиперплазией, липоаденома (аденолипома), аденома с уродливыми ядрами, перстневидно-клеточная аденома, светлоклеточная аденома, веретеноклеточная аденома, черная фолликулярная аденома (у пациентов, получавших лечение миноциклином). В новой классификации нет упоминания о ранее использовавшемся и вводившем в заблуждение клиницистов термине «атипическая аденома». Онкоцитарные (Гюртле-клеточные) аденомы выделены в отдельную категорию Гюртле-клеточных опухолей (Гюртле-клеточная аденома и Гюртле-клеточная карцинома). При иммуногистохимическом исследовании опухолевые клетки иммунореактивны с антителами к цитокератинам, тиреоглобулину, TTF-1, PAX8, но негативны с антителами к кальцитонину, CEA, нейроэндокринным маркерам. Индекс мечения пролиферирующих клеток Ki-67 обычно составляет менее 5%. Реакции с антителами к галектину-3, HBME-1 и CITED редко бывают позитивными. Молекулярно-генетический профиль 30% аденом характеризуется соматическими мутациями генов семейства RAS. «Горячей точкой» мутаций NRAS и HRAS является кодон 61, менее часты соматические мутации гена KRAS. В отличие от фолликулярных карцином клетки аденом реже имеют структурные перестройки PAX8/PPARG. Мутации TSHR и GNAS обнаружены в клетках фолликулярных аденом с признаками повышенной функциональной активности.
Гиалинизирующая трабекулярная опухоль — новообразование, развивающееся из фолликулярного эпителия и состоящее из трабекулярных структур, образованных полигональными и вытянутой формы клетками. Трабекулы перемежаются с интра- и межтрабекулярно расположенным гиалиновым материалом, имеющим разную степень выраженности. В новой классификации опухоль отнесена к группе пограничных новообразований низкого или неопределенного злокачественного потенциала. Средний возраст пациентов составляет 50 лет, хотя описаны наблюдения у лиц 28—30-летнего возраста, при этом преобладают пациенты женского пола. Гиалинизирующая трабекулярная опухоль может возникать на фоне хронического тиреоидита, иногда встречается вместе с папиллярным раком, многоузловым зобом. Гистологическое исследование выявляет однотипное трабекулярно-альвеолярное строение опухоли, которая состоит из клеток вытянутой формы, среднего и крупного размера, с мелкогранулярной, ацидофильной или амфофильной цитоплазмой с наличием внеклеточного эозинофильного вещества (гиалина), характеризующегося положительной ШИК-реакцией. Ядра опухолевых клеток с узурами, псевдовключениями и мелкими ядрышками (похожи на ядра клеток папиллярного рака), митозы редки. Опухолевые трабекулы окружены нежной фиброваскулярной стромой. Окраска на амилоид отрицательная. Клетки опухоли экспрессируют тиреоглобулин, TTF-1, но не экспрессируют кальцитонин. Экспрессия маркеров, используемых для оценки злокачественного потенциала (галектин-3, цитокератин-19 и HBME-1), может наблюдаться в клетках до 50% опухолей. Характерной для гиалинизирующей трабекулярной опухоли является мембранная экспрессия MIB1 (Ki-67) в отличие от ядерной, обычно используемой для оценки индекса пролиферативной активности. Следует заметить, что мембранная экспрессия Ki-67 отмечена лишь при отсутствии высокотемпературной демаскирующей обработки срезов, применяемой с целью восстановления антигенных детерминант после воздействия фиксирующих растворов. Молекулярно-генетические исследования, установившие наличие структурных перестроек хромосом с формированием химерных генов RET/PTC1 в половине наблюдений гиалинизирующих трабекулярных опухолей, позволили высказать предположение о возможной связи с аналогичными молекулярными механизмами развития папиллярного рака, однако не было получено дальнейшего подтверждения указанной гипотезы, равно как пока не зарегистрировано мутаций BRAF или RAS в клетках гиалинизирующей трабекулярной опухоли. Несмотря на благоприятный прогноз у большинства пациентов после хирургического лечения, в англоязычной литературе представлены очень редкие описания метастазирования опухоли в регионарные лимфатические узлы и лишь одно наблюдение метастазов в ткань легкого [4].
Другие инкапсулированные опухоли фолликулярного строения (рис. 1).



Папиллярная карцинома — это злокачественная эпителиальная опухоль, демонстрирующая фолликулярно-клеточную дифференцировку и ряд признаков, касающихся изменений ядер опухолевых клеток (рис. 3).
Папиллярная карцинома с фиброматозом (фасциитоподобной стромой) отличается обильно развитым стромальным компонентом, настолько выраженным, что опухоль напоминает узловатый фасциит, фиброматоз и другие пролиферативные миофибробластические процессы. Солидно-трабекулярный вариант не является необычным для папиллярной карциномы, демонстрирует солидную и/или трабекулярную картину роста, чаще встречающуюся в опухолях детской возрастной группы. Термин «солидный вариант» должен быть использован, если вся или часть опухоли не относится к другим вариантам, имеющим солидную, трабекулярную или инсулярную картину роста. Солидный вариант составляет всего 1—3% папиллярного рака у взрослых лиц по сравнению с более высокими показателями распространенности среди карцином у детей, особенно подвергшихся действию радиации. Эти опухоли чаще ассоциированы с хромосомными аберрациями, приводящими к перестройкам типа RET/PTC3 в детских и облученных популяциях. Этот вариант должен быть отличим патологоанатомами от низкодифференцированной карциномы, которая имеет аналогичный тип роста, но характер клеток иной (отсутствуют признаки папиллярной карциномы), присутствуют некроз и высокая митотическая активность.
Веретеноклеточный вариант папиллярной карциномы. Изредка папиллярная карцинома демонстрирует наличие очагов веретеноклеточной метаплазии. Эпителиальная природа этих клеток подтверждается иммуноэкспрессией цитокератинов и TTF-1. Веретенообразные клетки не связаны с кровоизлиянием или гемосидерином, и форма зоны опухолевого роста не имеет географически четкой конфигурации, что отличает истинные веретеноклеточные участки папиллярных карцином от реактивных изменений после тонкоигольных биопсий. В отличие от недифференцированного рака при веретеноклеточном варианте клетки выглядят менее злокачественно, отсутствуют некроз и фигуры митоза.
Светлоклеточный вариант — очень необычный, часто сочетается с оксифильно-клеточным. Этот вариант следует дифференцировать от светлоклеточного варианта медуллярной (С-клеточной) карциномы, интратиреоидной локализации гиперпластических процессов околощитовидной железы, метастазов светлоклеточного почечно-клеточного рака. Полезными иммуногистохимическими маркерами дифференциальной диагностики являются TTF-1, хромогранин А, синаптофизин, гормон околощитовидной железы, эпителиальный мембранный антиген, RCC. Уортино-подобный вариант папиллярной карциномы отличается увеличенными в размере клетками с эозинофильной цитоплазмой и выраженной лимфоидной инфильтрацией стромы. Опухоль возникает в ЩЖ с тиреоидитом Хашимото. Строение напоминает одноименную опухоль слюнной железы. Прогноз не отличается от такового при обычном классическом папиллярном раке с аналогичным размером опухоли и стадией опухолевого роста.
Фолликулярная карцинома — это злокачественная опухоль, возникающая из фолликулярного эпителия, в которой отсутствуют признаки изменений ядер опухолевых клеток, характерные для папиллярной карциномы. Опухоль обычно инкапсулирована и имеет признаки инвазивного роста. Онкоцитарные карциномы классифицируются отдельно. Выделены следующие категории фолликулярных карцином: минимально инвазивная; инкапсулированная ангиоинвазивная; и широкоинвазивная, которая имеет аналогичный с фолликулярной карциномой без дополнительного уточнения (БДУ) гистологический код. Непременным признаком фолликулярной карциномы является инвазивный рост. Для минимально инвазивной карциномы характерна лишь капсулярная инвазия. Большинство авторов капсулярной инвазией считают лишь пенетрацию опухоли сквозь всю толщу собственной капсулы. Неровные контуры внутренней границы капсулы, выпячивание структур опухоли в сторону собственной капсулы или наличие опухолевых гнезд среди волокон фиброзной капсулы не могут служить достаточными признаками инвазивного роста. Разрыв капсулы вследствие хирургических манипуляций, предоперационной тонкоигольной биопсии и/или перекручивание края опухоли по периферии гистологического среза не равнозначны инвазивному росту. Минимальная капсулярная инвазия, как правило, имеет грибовидную форму. Для инкапсулированной ангиоинвазивной карциномы должна быть установлена сосудистая инвазия, т. е. бесспорная инвазия с наличием связи опухолевых структур с сосудистой стенкой, присутствием эндотелиальных клеток на периферии опухолевых тромбов в просветах сосудов собственной капсулы или за ее пределами. Наличие свободно расположенных опухолевых клеток в просветах тонкостенных сосудов в толще опухоли не является признаком сосудистой инвазии и злокачественного потенциала. Полагают, что наличие в опухоли менее 4 очагов сосудистой инвазии ассоциировано с лучшим прогнозом по сравнению с опухолями, имеющими более распространенную сосудистую инвазию. Широкоинвазивные карциномы демонстрируют распространенную инвазию в окружающую ткань ЩЖ и экстратиреоидный рост в прилежащие мягкие ткани. Широкоинвазивные карциномы, особенно с солидным и трабекулярным типами роста, по сравнению с инкапсулированными ангиоинвазивными имеют менее благоприятный прогноз. Тем не менее следует отличать этот вариант от низкодифференцированных карцином, равно как от солидно-трабекулярного варианта папиллярной карциномы. В новой классификации фолликулярных карцином выделен светлоклеточный вариант (с наличием более 50% светлых клеток). Появление светлых клеток в опухоли связывают с накоплением в их цитоплазме гликогена, липидов, муцина, тиреоглобулина или с расширением и гипертрофией митохондрий и комплекса Гольджи. К другим вариантам отнесены перстневидно-клеточный вариант, фолликулярная карцинома с гломерулярным типом роста, веретеноклеточный вариант.
Гюртле-клеточные (онкоцитарные) опухоли — опухоли (обычно инкапсулированные) состоят из онкоцитов. Неинвазивные онкоцитарные опухоли классифицируют как Гюртле-клеточные аденомы, а при наличии капсулярной и/или сосудистой инвазии — как Гюртле-клеточные карциномы.
Низкодифференцированная карцинома — фолликулярно-клеточная опухоль, занимающая морфологически и по своим биологическим особенностям промежуточное положение между дифференцированным (фолликулярным и папиллярным) и недифференцированным (анапластическим) раком. Алгоритм диагностики низкодифференцированной карциномы предложен на международном рабочем совещании патологов в Турине, Италия, в 2007 г. Кратко он состоит в том, что злокачественные опухоли ЩЖ из фолликулярного эпителия, имеющие солидное, трабекулярное или инсуляр