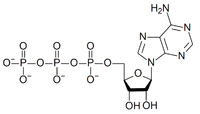
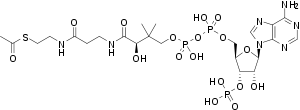
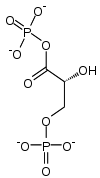
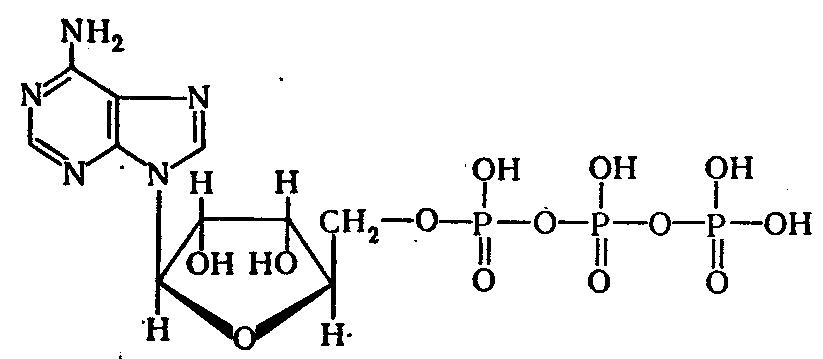
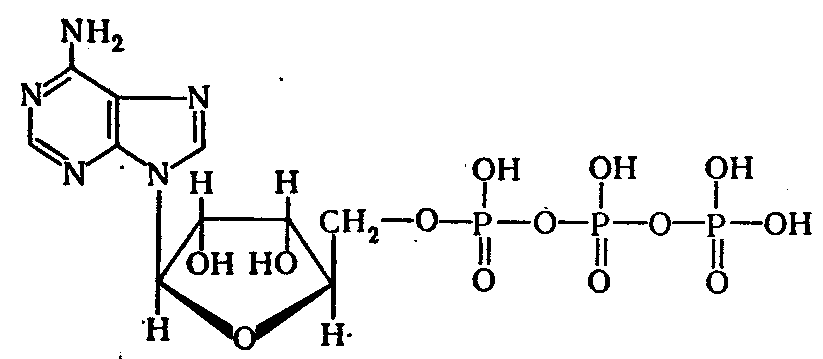
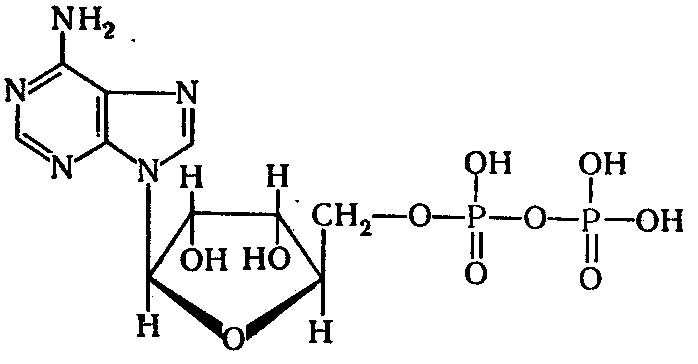
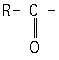какие соединения содержат макроэргические связи
Макроэргические соединения
макроэргические соединения — высокоэнергетические соединения – соединения, содержащие богатые энергией (макроэргические) связи. К ним относят АТФ и вещества, способные образовывать АТФ в ферментативных реакциях переноса преимущественно фосфатных групп. М. с. занимают… … Словарь микробиологии
МАКРОЭРГИЧЕСКИЕ СОЕДИНЕНИЯ — (от макро. и греч. ergon деятельность работа), органические соединения живых клеток, содержащие богатые энергией, или макроэргические, связи. Образуются в результате фотосинтеза, хемосинтеза и биологического окисления. К макроэргическим… … Большой Энциклопедический словарь
макроэргические соединения — (от макро. и греч. érgon деятельность, работа), органические соединения живых клеток, содержащие богатые энергией, или макроэргические, связи. Образуются в результате фотосинтеза, хемосинтеза и биологического окисления. К макроэргическим… … Энциклопедический словарь
Макроэргические соединения — Макроэргические молекулы (макроэрги) биологические молекулы, которые способны накапливать и передавать энергию в ходе реакции. При гидролизе одной из связей высвобождается более 20 кДж/моль. По химическому строению макроэрги чаще… … Википедия
Макроэргические соединения — (от Макро. и греч. érgon деятельность, работа) высокоэргические, высокоэнергетические соединения, природные соединения, содержащие богатые энергией, или макроэргические, связи; присутствуют во всех живых клетках, участвуя в процессах… … Большая советская энциклопедия
МАКРОЭРГИЧЕСКИЕ СОЕДИНЕНИЯ — (от макро. и греч. ergon деятельность, работа), органич. соединения живых клеток, содержащие богатые энергией, или макроэргические, связи. Образуются в результате фотосинтеза, хемосинтеза и биол. окисления. К М. с. относятся… … Естествознание. Энциклопедический словарь
макроэргические соединения — (макро + греч. ergon работа, действие; син. высокоэргические соединения) органические соединения, расщепление которых сопровождается выделением большого количества свободной энергии; в М. с. аккумулируется энергия, расходуемая организмом в… … Большой медицинский словарь
Макроэргические соединения — (от греч. макро + ergon деятельность, работа) при всех типах энергетического обмена энергия запасается в живой клетке в виде макроэрги ческих соединений, соединений содержащих богатые энергией химические связи. К макроэргическим соединениям… … Начала современного естествознания
МАКРОЭРГИЧЕСКИЕ СОЕДИНЕНИЯ — макроэргические соединения, органические соединения, при гидролизе которых освобождается значительное количество энергии, используемой для осуществления различных функций организма. Ведущее положение среди М. с. занимают аденозинтрифосфорная и… … Ветеринарный энциклопедический словарь
Макроэргические соединения
Макроэргические молекулы (макроэрги) — биологические молекулы, которые способны накапливать и передавать энергию в ходе реакции. При гидролизе одной из связей высвобождается более 20 кДж/моль. По химическому строению макроэрги — чаще всего ангидриды фосфорной и карбоновых кислот, а также слабых кислот, какими являются тиолы и енолы.
Классификация макроэргов по связям
Примечания
Полезное
Смотреть что такое «Макроэргические соединения» в других словарях:
МАКРОЭРГИЧЕСКИЕ СОЕДИНЕНИЯ — высокоэнергетические соединения, природные соединения, содержащие богатые энергией, или макроэргические, связи; присутствуют во всех живых клетках, участвуют в накоплении и превращении энергии. К М. с. относят гл. обр. АТФ и вещества, способные… … Биологический энциклопедический словарь
макроэргические соединения — высокоэнергетические соединения – соединения, содержащие богатые энергией (макроэргические) связи. К ним относят АТФ и вещества, способные образовывать АТФ в ферментативных реакциях переноса преимущественно фосфатных групп. М. с. занимают… … Словарь микробиологии
МАКРОЭРГИЧЕСКИЕ СОЕДИНЕНИЯ — (от макро. и греч. ergon деятельность работа), органические соединения живых клеток, содержащие богатые энергией, или макроэргические, связи. Образуются в результате фотосинтеза, хемосинтеза и биологического окисления. К макроэргическим… … Большой Энциклопедический словарь
Макроэргические соединения — I Макроэргические соединения (греч. makros большой + ergon работа, действие; синоним: высокоэргические соединения, высокоэнергетические соединения) группа природных веществ, молекулы которых содержат богатые энергией, или макроэргические, связи;… … Медицинская энциклопедия
макроэргические соединения — (от макро. и греч. érgon деятельность, работа), органические соединения живых клеток, содержащие богатые энергией, или макроэргические, связи. Образуются в результате фотосинтеза, хемосинтеза и биологического окисления. К макроэргическим… … Энциклопедический словарь
Макроэргические соединения — (от Макро. и греч. érgon деятельность, работа) высокоэргические, высокоэнергетические соединения, природные соединения, содержащие богатые энергией, или макроэргические, связи; присутствуют во всех живых клетках, участвуя в процессах… … Большая советская энциклопедия
МАКРОЭРГИЧЕСКИЕ СОЕДИНЕНИЯ — (от макро. и греч. ergon деятельность, работа), органич. соединения живых клеток, содержащие богатые энергией, или макроэргические, связи. Образуются в результате фотосинтеза, хемосинтеза и биол. окисления. К М. с. относятся… … Естествознание. Энциклопедический словарь
макроэргические соединения — (макро + греч. ergon работа, действие; син. высокоэргические соединения) органические соединения, расщепление которых сопровождается выделением большого количества свободной энергии; в М. с. аккумулируется энергия, расходуемая организмом в… … Большой медицинский словарь
Макроэргические соединения — (от греч. макро + ergon деятельность, работа) при всех типах энергетического обмена энергия запасается в живой клетке в виде макроэрги ческих соединений, соединений содержащих богатые энергией химические связи. К макроэргическим соединениям… … Начала современного естествознания
МАКРОЭРГИЧЕСКИЕ СОЕДИНЕНИЯ — макроэргические соединения, органические соединения, при гидролизе которых освобождается значительное количество энергии, используемой для осуществления различных функций организма. Ведущее положение среди М. с. занимают аденозинтрифосфорная и… … Ветеринарный энциклопедический словарь
Макроэргическая связь
Макроэргические связи — это ковалентные связи, которые гидролизуются с выделением значительного количества энергии: 30 кДж/моль и более (свободная энергия гидролиза).
Вообще термин «макроэргическая связь» используется исключительно для связей, энергия которых используется в метаболизме и не указывает на истинную величину энергии связей.
Обычно это относится к макроэргическим молекулам — биологическим молекулам, которые способны накапливать и передавать энергию в ходе реакции. При гидролизе одной из связей высвобождается более 20 кДж/моль. По химическому строению макроэрги — чаще всего ангидриды карбоновой и фосфорной кислот, а также других слабых кислот. Примеры макроэргических соединений — молекулы АТФ, ГТФ и НАД.
Полезное
Смотреть что такое «Макроэргическая связь» в других словарях:
Клетка — Начиная знакомство с животным миром, необходимо сначала в самых общих чертах остановиться на строении и отправлениях клетки. Клетка представляет собой структурную и функциональную единицу, лежащую в основе строения и развития… … Биологическая энциклопедия
ГЛУТАМИНСИНТЕТАЗА — [L глутамат: аммиак лигаза (образующая АДФ)], фермент класса лигаз, катализирующий в присут. ионов двухвалентных металлов включение NH3 в орг. соединение: HOOCCH2CH2CH(NH2)COOH + NH3 + АТФ H2NCOCH2CH2CH(NH2)COOH + АДФ + Н 3 РО 4, где АТФ… … Химическая энциклопедия
Макроэргические соединения
В живом организме нет прямого перехода энергии от источника (энергогенерирующего процесса) к потребителю (биологическому преобразователю энергии). Непосредственное использование потенциальной химической энергии, содержащейся в молекулах пищевых веществ, невозможно потому, что при разрыве внутримолекулярных связей выделяется такое огромное количество энергии, что она не может быть аккумулирована внутриклеточными ферментными системами и способна вызвать повреждение этих систем. Для процессов, совершающихся в живом организме, характерно ступенчатое освобождение свободной энергии с одновременным преобразованием ее в химическую энергию макроэргических соединений или электрохимический потенциал на клеточных мембранах.
Макроэргические соединения это соединения, содержащие макроэргическую связь. Макроэргическими называются химические связи, свободная энергия гидролиза которых составляет не менее 21 кДж/моль. Эти связи обозначают знаком
(тильда). Говоря об энергии макроэргических связей, в биохимии имеют в виду не действительную энергию ковалентной связи между атомами, как это принято в физической химии, а лишь разность между значениями свободной энергии (∆G) исходных реагентов и продуктов реакций гидролиза макроэргических соединений. «Энергия связи» в этом смысле, строго говоря, не локализована в данной связи, а характеризует реакцию в целом. Поэтому правильнее говорить не о возникновении макроэргической связи, а об образовании в процессе химического сопряжения нового макроэргического соединения.
Универсальной формой запасания свободной энергии для всего живого мира является энергия макроэргических связей АТФ: все преобразования энергии в процессах жизнедеятельности осуществляются через аккумуляцию энергии в этих связях и её использование при их разрыве. Значение ∆G для этих реакций представляет собой как бы «биологический квант» энергии, т.к. все преобразования энергии в организмах происходят порциями, примерно равными ∆G. При ферментативном гидролизе АТФ в клетке отщепляющаяся фосфатная группа переносится на субстрат, запас энергии в котором оказывается в результате больше, чем в исходном соединении.
Величина изменения свободной энергии в реакциях переноса зависит как от природы переносимой группы, так и от природы молекулы акцептора. При сравнении потенциала переноса групп различных соединений необходимо пользоваться единым стандартным акцептором. В качестве такого акцептора обычно принимают молекулу воды и выражают потенциал переноса в виде свободной энергии реакции гидролиза данного соединения.
Потенциал переноса измеряется в кДж на 1 моль групп донора, переносимых на стандартный акцептор при стандартных (одномолярных) концентрациях. В таблице 1 представлены величины ∆G 0 (при рН=7, Т=25 0 С) основных макроэргических соединений и органических соединений с нормальными связями.
Таблица 1. Свободная энергия гидролиза некоторых соединений.
Сопоставляя величины потенциалов переноса, можно выяснить, является ли определенная комбинация реакций термодинамически вероятной. В условиях стандартных концентраций происходит самопроизвольный перенос групп от соединений, у которых потенциал переноса высок, к соединениям, у которых он ниже. Так, АТФ, находящаяся в середине шкал значений потенциала переноса групп, способна акцептировать фосфорную группу от тех соединений, которые в реакциях энергетического метаболизма выполняют роль первичных макроэргов и имеют более высокий потенциал переноса. Вместе с тем АТФ может переносить фосфорные группы на молекулы соединений, относящихся к «низкоэнергетическим» фосфатам, у которых потенциал переноса групп ниже, чем у АТФ.
Большинство макроэргических соединений представляют собой ангидриды фосфорной кислоты и какой-либо другой кислоты, или фосфорные эфиры енолов. Первично возникающие в ходе реакций химического сопряжения макроэргические соединения отличаются высокой нестабильностью в водной среде. Они легко подвержены гидролизу, что ведет к рассеиванию энергии окисления в виде тепла. Поэтому для того, чтобы сохранить энергию и использовать ее в процессах, идущих с потреблением энергии, первично возникшая макроэргическая связь должна быть перенесена на молекулу соединения, обладающего достаточно высокой устойчивостью в водной среде. В большинстве случаев макроэргические фосфорные соединения при участии фосфотрансфераз переносят фосфатную группу на молекулу АДФ, выполняющую в клетке роль универсального акцептора высокоэнергетического фосфата. Образующаяся в итоге подобных реакций переноса АТФ выступает затем как специфический донор фосфатных групп в других ферментативных реакциях.
Количество освобождаемой энергии зависит от рН среды, концентрации неорганического фосфата, а также соотношения концентраций АТФ и АДФ в клетке. При отщеплении второй фосфатной группы образуется аденозинмонофосфат и выделяется примерно такое же количество энергии:
Молекула АМФ может снова фосфорилируоваться до АДФ второй молекулой АТФ при участии особого фермента аденилаткиназы, и образующийся пирофосфат гидролизуется пирофосфатазой до ортофосфорной кислоты:
Наличие двух путей гидролитического расщепления АТФ обусловливает дополнительную гибкость адениловой системы в функции посредника между процессами аккумуляции и использования энергии.
АТФ может функционировать в клетках не только как фосфорилирующий агент, переносящий фосфат на соответствующий акцептор, но и как донор, переносящий на акцептор неорганический пирофосфат, и как аденилирующий агент, переносящий на акцептор свою аденилатную группу (например, при образовании аминоациладенилатов).
Аденилатная система клетки включает: АДФ, АТФ и АМФ. Сумму этих компонентов в клетке практически постоянная величина. Энергетический статус клетки в каждый определенный момент зависит от относительных концентраций всех трех компонентов. Если вся система представлена в форме АТФ, то клетка находится в максимально высоком энергетическом состоянии; если же в форме АМФ, то клетка лишена богатых энергией компонентов и находится в низшем энергетическом состоянии. Для оценки энергетических состояний пользуются показателем энергетического заряда аденилатной системы, который равен половине общего числа макроэргических фосфатных групп, приходящихся на остаток аденозина.
В живой клетке величина «энергетического заряда» поддерживается пределах от 0,7 до 0,9. Изменение энергетического заряда приводит к большим изменениям скорости процессов, замедлению или ускорению действия ферментов. Таким образом, система адениловых нуклеотидов осуществляет регуляцию процессов, ответственных за поставку и утилизацию энергии в клетке, и поддерживает оптимальный уровень функционирования, требующий наименьших затрат энергии.
В клетках есть несколько метаболических путей, ведущих к синтезу АТФ в сопряженных реакциях. Эти пути различаются по характеру катаболических превращений, приводящих к образованию доноров электронов, по типу окислительного процесса, в ходе которого высвобождается потенциальная свободная энергия, и по способу сопряжения энергоподающей реакции с образованием макроэргических соединений. Каждый из этих процессов приспособлен к обработке определенного вида «топлива», и каждый из них имеет свои пределы эффективности преобразования энергии окисления при синтезе АТФ.
Макроэргические связи
Макроэргические соединения, их биологическая роль, классификация. Принцип энергетического сопряжения реакций. Гормональная регуляция уровня глюкозы в крови. Механизм гипергликемического действия адреналина. Метаболические пути окислительного распада.
| Рубрика | Химия |
| Вид | контрольная работа |
| Язык | русский |
| Дата добавления | 25.01.2014 |
| Размер файла | 2,4 M |
Отправить свою хорошую работу в базу знаний просто. Используйте форму, расположенную ниже
Студенты, аспиранты, молодые ученые, использующие базу знаний в своей учебе и работе, будут вам очень благодарны.
Размещено на http://www.allbest.ru/
Вопрос 1. Макроэргические соединения, их биологическая роль, классификация. Центральная роль АТФ в энергетике клетки
Вопрос 2. Общие аспекты биоэнергетики: законы термодинамики, экзергонические и эндергонические реакции. Принцип энергетического сопряжения реакций
Вопрос 3. Гормональная регуляция уровня глюкозы в крови. Гипер- и гипогликемические гормоны. Объясните механизм гипергликемического действия адреналина
Вопрос 4. Перечислите 4 основные метаболические пути окислительного распада глюкозы в клетках, приведите схемы этих метаболических реакций
Вопрос 5. Пентозный цикл окисления углеводов: химизм окислительной фазы, суммарная реакция, биологическая роль
Задача. Сколько молей АТФ может быть образовано при полном окислении 1 моля уксусной кислоты? При полном окислении 1 моля глюкозы? Приведите реакции в виде схемы с указанием всех участников процесса
Вопрос 1. Макроэргические соединения, их биологическая роль, классификация. Центральная роль АТФ в энергетике клетки
Ведущее положение среди макроэргических соединений занимают аденозинтрифосфорная и аденозиндифосфорная, играющие основную роль в энергетическом обмене организма. К макроэргическим соединениям относятся также креатинфосфат, аргининфосфат, 1,3-дифосфоглицериновая кислота, ацетилфосфат, фосфоенолпировиноградная кислота.
Открыты макроэргические соединения, в состав которых вместо аденина входят гуанин, урацил, цитозин: гуанозиндифосфорная (ГДФ), гуанозинтрифосфорная (ГТФ), урндиндифосфорная (УДФ), уридинтрифосфорная (УТФ), цитидиндифосфорная (ЦДФ), цитидинтрифосфорная (ЦТФ) кислоты.
Макроэргические соединения принимают участие в реакциях трансфосфорилирования, при биосинтезе белка, нуклеиновых кислот и фосфатидов. макроэргический энергетический глюкоза
От макроэргических соединений следует отличать фосфорильные, ацильные и другие соединения, не имеющие макроэргических связей и потому не способные образовывать АТФ в реакциях переноса фосфорильных и ацильных групп: нуклеозидмонофосфорные кислоты, нуклеиновые кислоты, фосфосахара, фосфолипиды и другие.
Однако окисление некоторых из этих соединений может вести к образованию макроэргических соединений.
АТФ играет выдающуюся роль в энергетике клетки. Cистеме АТФ принадлежит центральное место в процессах переноса химической энергии. АТФ образуется в реакциях субстратного фосфорилирования и мембранзависимого фосфорилирования.
При субстратном фосфорилировании источником образования АТФ служат реакции двух типов:
Ф + АДФ обратимо переходит в субстрат + АТФ,
«, введенный американским биохимиком Ф.Липманом (F.Lipmann), служит для обозначения макроэргической связи;
Х + АДФ + Фн обратимо переходит в субстрат + X +АТФ,
В реакциях первого типа осуществляется перенос высокоэнергетической фосфатной группы от молекулы-донора на АДФ, катализируемый соответствующими киназами. Реакциями такого типа являются реакции субстратного фосфорилирования на пути анаэробного превращения сахаров.
АТФ образуется также за счет энергии дельта мю Н+ в процессе мембранзависимого фосфорилирования.
Молекула АТФ содержит две макроэргические фосфатные связи, при гидролизе которых высвобождается значительное количество свободной энергии:
Отщепление последней фосфатной группы от молекулы АМФ приводит к значительно меньшему высвобождению свободной энергии:
Молекула АТФ обладает определенными свойствами, которые и привели к тому, что в процессе эволюции ей была отведена столь важная роль в энергетическом метаболизме клеток. Термодинамически молекула АТФ нестабильна, что вытекает из большой отрицательной величины дельта G ее гидролиза. В то же время скорость неферментативного гидролиза АТФ в нормальных условиях очень мала, т.е. химически молекула АТФ высокостабильна. Последнее свойство обеспечивает эффективное сохранение энергии в молекуле АТФ, поскольку химическая стабильность молекулы препятствует тому, чтобы запасенная в ней энергия бесполезно рассеивалась в виде тепла. Малые размеры молекулы АТФ позволяют ей легко диффундировать в различные участки клетки, где необходим подвод энергии извне для выполнения химической, осмотической, механической работы.
Аденозинмонофосфорная кислота ( АМФ ) входит в состав всех РНК; при присоединении еще двух молекул фосфорной кислоты (Н3РО4) она превращается в АТФ и становится источником энергии, которая запасается в двух последних остатках фосфатов.
Как во всякий нуклеотид, в АТФ входит остаток азотистого основания (аденин), пентоза (рибоза) и остатки фосфорной кислоты (у АТФ их три). Из состава АТФ под действием фермента АТФ-азы отщепляются остатки фосфорной кислоты. При отщеплении одной молекулы фосфорной кислоты АТФ переходит в АДФ (аденозиндифосфорная кислота), а если отщепляются две молекулы фосфорной кислоты, АТФ переходит в АМФ (аденозинмонофосфорная кислота). Реакции отщепления каждой молекулы фосфорной кислоты сопровождаются освобождением 419 кДж/моль.
Для того чтобы подчеркнуть высокую энергетическую «стоимость» фосфорно-кислородной связи в АТФ, ее принято обозначать знаком и называть макроэргической связью. В АТФ имеются две макроэргические связи.
Значение АТФ в жизни клетки велико, она играет центральную роль в клеточных превращениях энергии. В реакциях с участием АТФ она, как правило, теряет одну молекулу фосфорной кислоты и переходит в АДФ. А далее АДФ может присоединить остаток фосфорной кислоты с поглощением 419 кДж/моль, восстановив запас энергии.
Основной синтез АТФ происходит в митохондриях.
Роль АТФ в клеточной энергетике можно определить следующим образом:
1. химическая энергия, освобождаемая в процессе катаболизма, запасается путем фосфорилирования AДФ с образованием АТФ;
2. энергия АТФ затем используется после расщепления макроэргических связей АТФ в ходе эндергонических реакций синтеза и других процессов, требующих затрат энергии, например активного транспорта.
Вопрос 2. Общие аспекты биоэнергетики: законы термодинамики, экзергонические и эндергонические реакции. Принцип энергетического сопряжения реакций
Первое начало термодинамики является законом сохранения энергии для систем, в которых существенное значение имеют тепловые процессы (поглощение или выделение тепла). Согласно первому началу термодинамики, термодинамическая система (напр., пар в тепловой машине) может совершать работу только за счет своей внутренней энергии. Первое начало термодинамики часто формулируют как невозможность существования вечного двигателя первого рода, который совершал бы работу, не черпая энергию из некоторого источника.
Первое начало термодинамики вводит представление о внутренней энергии системы как функции состояния. При сообщении системе некоторого количества теплоты Q происходит изменение внутренней энергии системы DU и система совершает работу А:
Первое начало термодинамики утверждает, что каждое состояние системы характеризуется определенным значением внутренней энергии U, независимо от того, каким путем приведена система в данное состояние. В отличие от значений U значения A и Q зависят от процесса, приведшего к изменению состояния системы.
Если начальное и конечное состояния бесконечно близки, первое начало термодинамики записывается в виде:
Это означает, что бесконечно малое изменение внутренней энергии dU является полным дифференциалом функции состояния, т.е. интеграл
тогда как бесконечно малые кол-ва теплоты и работы не являются дифференциальными величинами, т.е. интегралы от этих бесконечно малых величин зависят от выбранного пути перехода между состояниями а и b.
Первое начало термодинамики позволяет рассчитать максимальную работу, получаемую при изотермическом расширении идеального газа, изотермическом испарении жидкости при постоянном давлении.
Если система обменивается со средой не только энергией, но и веществом, изменение внутренней энергии системы при переходе из начального состояния в конечное включает помимо работы А и теплоты Q еще и т. наз. энергию массы Z. Бесконечно малое количество энергии массы в процессе определяется химическим потенциалом k каждого из компонентов системы:
В случае процесса, при котором система в каждый момент времени находится в равновесии с окружающей средой, первое начало термодинамики в общем виде имеет математическое выражение:
где p и k равны соответствующим значениям для окружающей среды (индекс е при Xi обычно опускают).
Второе начало термодинамики устанавливает существование энтропии как функции состояния макроскопической системы. Утверждает, что все процессы, протекающие с конечной скоростью, в принципе необратимы, и дает термодинамический критерии для определения направленности процессов.
Существует несколько различных формулировок второго начала термодинамики и способов его обоснования, однако все они взаимосвязаны и в конечном счете эквивалентны.
Согласно наиболее общей формулировке второго начала термодинамики, бесконечно малое кол-во тепла, переданное системе в обратимом процессе, отнесенное к абсолютной температуре Т, является полным дифференциалом функции состояния, называемого энтропией.
Для обратимых процессов dS; для необратимых 0 значение ДS > 0.
Из третьего начала термодинамики следует, что абсолютного нуля температуры нельзя достигнуть ни в каком конечном процессе, связанном с изменением энтропии, к нему можно лишь приближаться, поэтому третье начало термодинамики иногда формулируют как принцип недостижимости абсолютного нуля температуры.
Из третьего начала термодинамики вытекает ряд термодинамических следствий: при T > 0 должны стремиться к нулю теплоёмкости при постоянном давлении и при постоянном объёме, коэффициенты теплового расширения и некоторые аналогичные величины. Справедливость третьего начала термодинамики одно время подвергалась сомнению, но позже было выяснено, что все кажущиеся противоречия (ненулевое значение энтропии у ряда веществ при Т = 0) связаны с метастабильными состояниями вещества, которые нельзя считать термодинамически равновесными.
Третье начало термодинамики часто нарушается в модельных системах. Так, при энтропия классического идеального газа стремится к минус бесконечности. Это говорит о том, что при низких температурах идеальный газ должен вести себя не по уравнению Менделеева-Клапейрона.
Таким образом, третье начало термодинамики указывает на недостаточность классической механики и статистики и является макроскопическим проявлением квантовых свойств реальных систем.
Эндергонические и экзергонические реакции
Направление химической реакции определяется значением ДG. Если эта величина отрицательна, то реакция протекает самопроизвольно и сопровождается уменьшением свободной энергии. Такие реакции называют экзергоническими.
Если при этом абсолютное значение ДG велико, то реакция идёт практически до конца, и её можно рассматривать как необратимую.
Если ДG положительно, то реакция будет протекать только при поступлении свободной энергии извне; такие реакции называют эндергоническими.
Если абсолютное значение ДG велико, то система устойчива, и реакция в таком случае практически не осуществляется. При ДG, равном нулю, система находится в равновесии.
Сопряжение экзергонических и эндергонических процессов в организме.
В биологических системах термодинамически невыгодные (эндергонические) реакции могут протекать лишь за счёт энергии экзергонических реакций.
Такие реакции называют энергетически сопряжёнными. Многие из этих реакций происходят при участии аденозинтрифосфата (АТФ), играющего роль сопрягающего фактора.
Рассмотрим подробнее энергетику сопряжённых реакций на примере фосфорилирования глюкозы.
Реакция фосфорилирования глюкозы свободным фосфатом с образованием глюкозо-6-фосфата является эндергонической:
(1) Глюкоза + Н3РО4 > Глюкозо-6-фосфат + Н2О (ДG = +13,8 кДж/моль)
Для протекания такой реакции в сторону образования глюкозо-6-фосфата необходимо её сопряжение с другой реакцией, величина свободной энергии которой больше, чем требуется для фосфорилирования глюкозы.
При сопряжении процессов (1) и (2) в реакции, катализируемой гексокиназой, фосфорилирование глюкозы легко протекает в физиологических условиях; равновесие реакции сильно сдвинуто вправо, и она практически необратима:
Рис. 2.1 Энергетическое сопряжение
Сопряжение двух реакций возможно при наличии общего промежуточного продукта.
Вопрос 3. Гормональная регуляция уровня глюкозы в крови. Гипер- и гипогликемические гормоны. Объясните механизм гипергликемического действия адреналина
Регуляция уровня глюкозы в крови
В среднем уровень глюкозы в крови здорового человека колеблется от 2,7 до 8,3 ммоль/л, однако сразу после приёма пищи концентрация резко возрастает на короткое время.
Две группы гормонов противоположно влияют на концентрацию глюкозы в крови:
2. Гипергликемические гормоны (такие как глюкагон, гормон роста и адреналин), которые повышают содержание глюкозы в крови.
В состоянии гипергликемии увеличивается поступление глюкозы как в печень, так и в периферические ткани. Как только уровень глюкозы зашкаливает, поджелудочная железа начинает вырабатывать инсулин.
Гипогликемия
Гормоны прямого действия.
Основные механизмы действия инсулина:
1. Инсулин повышает проницаемость плазматических мембран для глюкозы. Этот эффект инсулина является главным лимитирующим звеном метаболизма углеводов в клетках.
2. Инсулин снимает тормозящее действие глюкокортикостероидов на гексокиназу.
3. На генетическом уровне инсулин стимулирует биосинтез ферментов метаболизма углеводов, в том числе ключевых ферментов.
Регуляция секреции инсулина в кровь происходит с участием нейро-рефлекторных механизмов. В стенках кровеносных сосудов есть особые хеморецепторы, чувствительные к глюкозе. Повышение концентрации глюкозы в крови вызывает рефлекторную секркцию инсулина в кровь, глюкоза проникает в клетки и ее концентрация в крови снижается.
Остальные гормоны вызывают повышение концентрации глюкозы в крови.
Относится к белково-пептидным гормонам. Обладает мембранным типом взаимодействия с клеткой-мишенью. Эффект оказывает через аденилатциклазную систему.
1. Вызывает повышение активности гликоген-фосфорилазы. В результате ускоряется распад гликогена. Так как глюкагон оказывает эффект только в печени то можно сказать, что он «гонит глюкозу из печени».
2. Понижает активность гликоген-синтетазы, замедляя синтез гликогена.
3. Активирует липазу в жировых депо.
Относятся к стероидным гормонам, поэтому обладают внутриклеточным типом взаимодействия с клеткой-мишенью. Проникая в клетку-мишень, они взаимодействуют с клеточным рецептором и обладают следующими эффектами:
2. Данные гормоны обеспечивают процесс гликонеогенеза субстратами.
3. На генетическом уровне усиливают биосинтез ферментов катаболизма белков.
Гормоны косвенного действия.
1. Усиливает выделение глюкагона, поэтому наблюдается ускорение распада гликогена.
2. Вызывает активацию липолиза, поэтому способствует утилизации жира в качестве источника энергии.
Йодсодержащие гормоны щитовидной железы
Трийодтиронин (Т3). Тироксин (Т4)
Под действием адреналина увеличивается содержание глюкозы в крови. В основе этого эффекта лежат следующие механизмы:
а) активация гликогенолиза в печени. Она связана с активацией аденилатциклазной системы гепатоцитов и образованием, в конечном итоге, активной формы фосфорилазы;
в) угнетение поглощения глюкозы инсулинозависимыми тканями с одновременной активацией липолиза в жировой ткани;
б) активация гликогенолиза в мышцах с последующей активацией глюконеогенеза в печени. При этом молочная кислота, освобождающаяся из мышечной ткани в кровь, идет на образование глюкозы в гепатоцитах;
г) подавление секреции инсулина и стимуляция секреции глюкагона клетками островков поджелудочной железы.
Вопрос 4. Перечислите 4 основные метаболические пути окислительного распада глюкозы в клетках, приведите схемы этих метаболических реакций
Гексозобисфосфатный путь распада углеводов
2. Только ГБФ-путь дает клетке энергию в виде АТФ. Это основной источник получения энергии в клетке.
3. Это самый длинный путь распада углеводов.
ГБФ-путь состоит из 3 этапов.
1-й этап протекает в цитоплазме, дает 8 молекул АТФ при распаде 1 молекулы глюкозы или 9АТФ при распаде одного глюкозного фрагмента гликогена. Заканчивается образованием 2-х молекул пирувата (ПВК).
В 3-й этап вступает молекула АцетилКоА, который образуется в результате 2-го этапа. Этот 3-й этап называется циклом трикарбоновых кислот (ЦТК) (смотрите лекции “Митохондриальное окисление”). В этом цикле АцКоА полностью расщепляется до СО2 и Н2О. При этом образуется 12 АТФ в расчете на молекулу АцКоА, вступившую в цикл. Если рассчитать на 1 молекулу глюкозы, то на 3-м этапе образуется 24 АТФ.
1-й этап проходит 10 промежуточных стадий. В ходе первой части этого этапа молекула глюкозы расщепляется пополам до 2-х молекул фосфоглицеринового альдегида (ФГА).
Особенности первой части 1-го этапа:
Гексокиназа (ГК) работает, чтобы ослабить прочную молекулу глюкозы:
На 3-й стадии фруктозо-6-фосфат еще более ослабляется фосфофруктокиназой (ФФК) и образуется фруктозо-1,6-бисфосфат:
Избыток АТФ и избыток цитрата сильно ингибируют ФФК. В этих условиях лимитирующим ферментом ГБФ-пути вместо гексокиназы становится ФФК. Из-за угнетения ФФК накапливаются глюкозо-6-фосфат (Г-6-Ф) и фруктозо-6-фосфат(Ф-6-Ф). Г-6-Ф ингибирует гексокиназу, уменьшая утилизацию глюкозы клеткой и одновременно активирует гликогенсинтетазу.
Если нет избытка АТФ и цитрата, а есть избыток АДФ, то АДФ активирует ФФК, и тогда скорость всего ГДФ-пути лимитируется опять гексокиназой.
В результате фосфофруктокиназной реакции молекула фруктозо-1,6-бисфосфата дестабилизируется (ослабляется) настолько, что сразу распадается на 2 триозы при участии фермента альдолазы (4-я реакция):
В следующую (шестую) реакцию ГБФ-пути вступает только ФГА. В результате уменьшается его концентрация и равновесие 5-й реакции сдвигается в сторону образования ФГА. Постепенно весь ФДА переходит в ФГА, и поэтому количество АТФ, синтезировавшееся в последующих реакциях ГБФ-пути, мы учитываем в расчете на 2 молекулы ФГА и других промежуточных метаболитов, которые из него образуются.
Эта реакция катализируется ферментом «глицеральдегидфосфатдегидрогеназа». Отщепляемый водород передается на НАД с образованием НАДН2. Энергии, которая выделяется при этом окислении, хватает и на то, чтобы одновременно обеспечить присоединение фосфата к альдегидной группе. Присоединяется фосфат макроэргической связью. В результате образуется 1,3-дифосфоглицериновая кислота (1,3-бисфосфоглицерат).
7-я реакция: субстратное фосфорилирование.
Фосфат с макроэргической связью передается на АДФ с образованием АТФ. В результате 7-й стадии в молекуле фосфоглицериновой кислоты остается 1 остаток фосфорной кислоты.
8-я реакция: Фосфат переносится из 3-го во второе положение и образуется 2-фосфоглицериновая кислота.
От 2-фосфоглицериновой кислоты отнимается Н2О. Это приводит к перераспределению молекулярной энергии. В результате на фосфате во втором положении накапливается энергия и связь становится макроэргической. Получается фосфоенолпируват(ФЕП).
10-я реакция: Субстратное фосфорилирование. Фосфат переносится на АДФ с образованием АТФ. ФЕП переходит в ПВК (пировиноградную кислоту).
На этом 1-й этап ГДФ-пути заканчивается, ПВК уходит в митохондрию и вступает во второй этап ГДФ-пути.
Итоги 1-го этапа: 10 реакций, из которых первая, третья и десятая реакции необратимы. Сначала расходуется 2 АТФ на 1 молекулу глюкозы. Потом окисляется ФГА. Энергия реализуется в ходе 2-х реакций субстратного фосфорилирования: в каждой из них образуется по 2 АТФ. Следовательно, на каждую молекулу глюкозы (на 2 молекулы ФГА) получается 4 АТФ путем субстратного фосфорилирования.
Суммарно все 10 стадий можно описать следующем уравнением:
В расчете на одну молекулу глюкозы образуется 2НАДН2.
Если эти 8 АТФ добавить к 30 молекулам АТФ, которые образуются на 2-м и 3-м этапах, то суммарный энергетический итог всего ГБФ-пути составит 38 АТФ на каждую молекулу глюкозы, расщепленную до СО2 и Н2О. В этих 38 АТФ заключено 65 процентов энергии, которая выделилась бы при сжигании глюкозы на воздухе. Это доказывает очень высокую эффективность работы ГБФ-пути.
Из 38 АТФ основная их часть образуется на 2-м и 3-м этапах. Каждый из этих этапов абсолютно необратим и требует обязательного участия кислорода, так как окислительные стадии этих этапов сопряжены с митохондриальным окислением (без него невозможны). Весь ГБФ-путь от глюкозы или гликогена до СО2 и Н2О называют: АЭРОБНЫЙ РАСПАД УГЛЕВОДОВ.
Ключевые ферменты первого этапа ГБФ-пути: ГЕКСОКИНАЗА и ФОСФОФРУКТОКИНАЗА.
Ключевые ферменты ЦТК: цитратсинтетаза и изоцитратдегидрогеназа. Оба фермента угнетаются избытком АТФ и избытком НАДН2. Изоцитратдегидрогеназа активируется избытком АДФ.
АТФ ингибирует эти ферменты по-разному: изоцитратдегидрогеназа ингибируется АТФ намного сильнее, чем цитратсинтаза. Поэтому при избытке АТФ накапливаются промежуточные продукты: цитрат и изоцитрат. В этих условиях цитрат может выходить в цитоплазму по градиенту концентраций.
1-й этап отделен от 2-го и 3-го этапов митохондриальной мембраной.
Поэтому 1-й этап может выполнять свои особенные функции. Эти функции связаны с двумя особенностями 1-го этапа.
Вопрос 5. Пентозный цикл окисления углеводов: химизм окислительной фазы, суммарная реакция, биологическая роль
Метаболические пути окисления глюкозы, главными из которых являются:
а) аэробное расщепление до углекислого газа и воды;
б) анаэробное окисление до лактата;
в) пентозный путь окисления;
г) окисление с образованием глюкуроновой кислоты.
Пентозофосфатный цикл начинается с окисления глюкозо-6-фосфата и последующего окислительного декарбоксилирования продукта (в результате от гексозофосфата отщепляется первый атом углерода). Это первая, так называемая окислительная, стадия пентозофосфатного цикла. Вторая стадия включает неокислительные превращения пентозофосфатов с образованием исходного глюкозо-6-фосфата (рис. 5.1). Реакции пен-тозофосфатного цикла протекают в цитозоле клетки.
Рис. 5.1 Пентозофосфатный путь окисления углеводов
Задача 6. Сколько молей АТФ может быть образовано при полном окислении 1 моля уксусной кислоты? При полном окислении 1 моля глюкозы? Приведите реакции в виде схемы с указанием всех участников процесса
В процессе аэробного окисления углеводов освобождается 2880 кДж/моль глюкозы. Если суммировать общий выход АТФ в этом процессе, то он составит 38 моль АТФ (рис. 6.1.). Процесс окисления глюкозы включает следующие этапы:
1) Аэробный гликолиз
2) Окислительное декарбоксилирование пирувата
3) Цикл Кребса (2 оборота)
СН3-СО-S-koA+2Н2О+3НАД++ФАД+ГДФ+Н3РО4 > koA-SH+ 2СО2 + 3НАДН + ФАДН2 + ГТФ
2 * 3НАДН > 2 * 9АТФ>18АТФ
2 ФАДН2 > 2 * 2АТФ > 4АТФ
В итоге: 2+6+6+18+4+2 = 38АТФ
Уксусная кислота активируется под действием фермента ацетил-КоА-синтетазы. Реакция протекает с использованием кофермента А и молекулы АТФ:
KoA + АТФ > СН3-СО-S-КoA +АДФ +Н2О.
СН3-СО-S-КoA+2Н2О+3НАД++ФАД+ГДФ+Н3РО4 > koA-SH+ 2СО2 + 3НАДН + ФАДН2 + ГТФ
В итоге: 9+2+1 = 12АТФ
1. Биологическая химия: Уч. для фармац. ин-тов и фармац фак мед ин-тов- М:Высш шк, 1986-474с.
2. Биохимия: Учебник/ под ред. Е.С. Северина-2-е изд., испр-М.:ГЭОТАР-МЕД,2004.-784С.:ил (серия «ХХ1 век»)
Размещено на Allbest.ru
Подобные документы
Углеводы, их химический состав, биологическая роль, характеристика классов, процесс обмена в организме при мышечной деятельности, расщепление в процессе пищеварения и их всасывание в кровь. Уровень глюкозы в крови, его регуляция и влияние на организм.
реферат [4,1 M], добавлен 18.11.2009
Понятие о гормонах, механизм их действия и классификация по химической природе и по выполняемым функциям. Гормональная регуляция обмена веществ и гипоталамо-гипофизарная система. Взаимопревращение гликоген-фосфорилазы. Гормоны периферических желез.
презентация [5,9 M], добавлен 29.10.2014
Основные параметры водно-солевого гомеостаза. Симпатическая и гормональная регуляция. Механизм действия вазопрессина. Нарушение выработки гормона. Ренин-ангиотензин-альдостероновая система. Синтез и секреция альдостерона клетками клубочковой зоны.
презентация [487,7 K], добавлен 02.12.2016
Значение ионофоров в исследовании функционирования биологических мембран, их химическая природа и классификация. Стадии механизма переноса ионов. Препараты, функционально разобщающие окислительное фосфорилирование, их назначение и механизм действия.
доклад [496,3 K], добавлен 16.12.2009
Химическая кинетика и ее значение в управлении химическими процессами. Классификация реакций по средам протекания, их отличительные черты. Скорость химических реакций, зависимость ее от температуры среды и наличия света. Принцип действия катализаторов.
реферат [152,7 K], добавлен 29.05.2009
Общее понятие о химической реакции, ее сущность, признаки и условия проведения. Структура химических уравнений, их особенности и отличия от математических уравнений. Классификация и виды химических реакций: соединения, разложения, обмена, замещения.
реферат [773,3 K], добавлен 25.07.2010
Строение углеводов. Механизм трансмембранного переноса глюкозы и других моносахаридов в клетке. Моносахариды и олигосахариды. Механизм всасывания моносахаридов в кишечнике. Фософорилирование глюкозы. Дефосфорилирование глюкозо-6-фосфата. Синтез гликогена.
презентация [1,3 M], добавлен 22.12.2014