какие страны признали нашу вакцину
Разработчик «Спутника V» рассказал о ходе регистрации вакцины в ВОЗ
Диалог по регистрации российской вакцины от коронавируса «Спутник V» во Всемирной организации здравоохранения (ВОЗ) находится на финишной прямой. Об этом сообщил в среду, 27 октября, руководитель лаборатории механизмов популяционной изменчивости патогенных микроорганизмов Центра имени Гамалеи Владимир Гущин в прямом эфире в рамках просветительской кампании «Разберемся в вакцинах вместе», организованной обществом «Знание» совместно с общероссийской акцией «Мы вместе».
«Вопрос ВОЗ — это фактически вопрос подачи документов и принятия той процедуры, которая у нас налажена в РФ, признания ее ВОЗ. Сейчас мы уже фактически находимся на финишной прямой, диалог построен — понятно, что нужно подготовить для того, чтобы в ближайшее время ВОЗ зарегистрировала вакцину», — отметил Гущин.
По его словам, в ближайшее время препарат получит регистрацию ВОЗ.
Ранее в этот день директор Национального исследовательского центра эпидемиологии и микробиологии имени Гамалеи Александр Гинцбург рассказал, что вакцинация «Спутником V» защитит от всех вариантов коронавируса, включая новый вид штамма «Дельта» AY.4.2. Он также отметил, что новые варианты «Дельты» по распространению не превышают десятой доли процента от общего числа случаев коронавируса, во всяком случае в Москве.
21 октября пресс-секретарь президента России Дмитрий Песков рассказал, что Минздрав РФ и Российский фонд прямых инвестиций (РФПИ) работают сейчас над регистрацией отечественной вакцины «Спутник V» в Европе. По его словам, в Европе заявили, что российская сторона передала неполный набор документов.
20 октября в РФПИ заявили, что ВОЗ возобновила рассмотрение заявки на одобрение «Спутника V». Отмечалось, что группа инспекторов ВОЗ должна вскоре посетить Россию, чтобы собрать все необходимые данные по вакцине.
13 октября помощник генерального директора ВОЗ Марианджела Симао заявила, что сроки рассмотрения заявки на регистрацию российской вакцины «Спутник V» зависят от юридических процедур, связанных с препаратом.
2 октября министр здравоохранения России Михаил Мурашко по итогам переговоров с председателем ВОЗ Тедросом Гебрейесусом сообщил, что все барьеры, препятствовавшие признанию организацией «Спутника V», устранены.
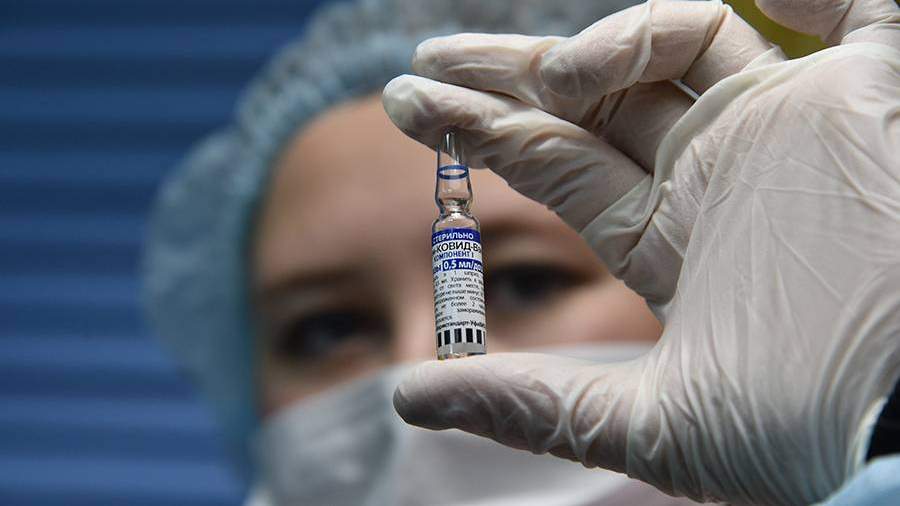
«Спутник V» разработали специалисты Центра имени Гамалеи. Он был зарегистрирован в августе 2020 года и стал первой в РФ и мире вакциной от COVID-19.
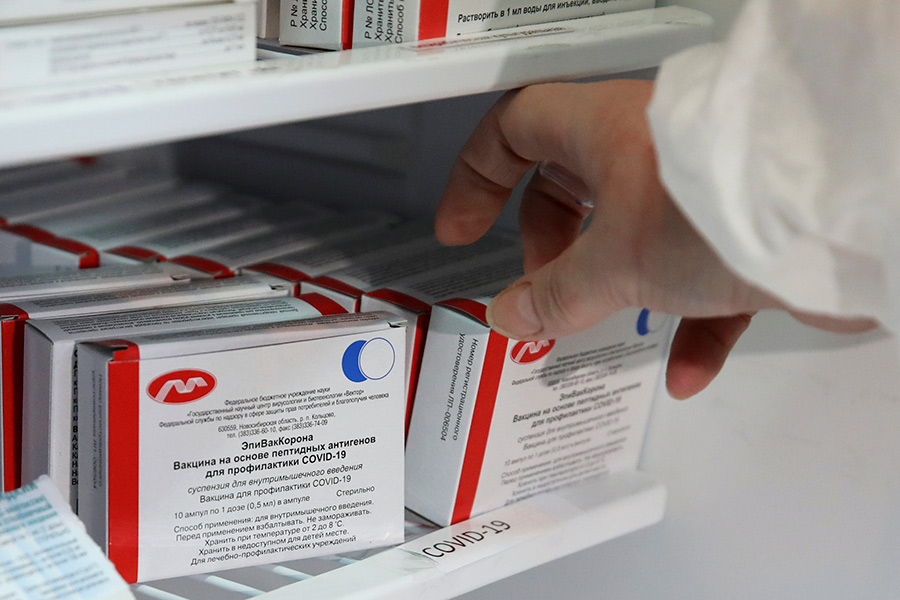
На фоне ухудшения эпидемиологической ситуации российские власти призывают граждан вакцинироваться, чтобы обезопасить свое здоровье и позаботиться о своих близких. Граждан прививают бесплатно. В стране зарегистрировано пять вакцин от коронавируса: «Спутник V», ставший первой в РФ и мире вакциной от COVID-19, а также «Спутник Лайт», «ЭпиВакКорона», «ЭпиВакКорона-Н» и «КовиВак».
Вся актуальная информация по ситуации с коронавирусом доступна на сайтах стопкоронавирус.рф и доступвсем.рф, а также по хештегу #МыВместе. Телефон горячей линии по вопросам коронавируса: 8 (800) 2000-112.
Раскрыта причина непризнания вакцины «Спутник V» в Евросоюзе
Чиновники Европейского медицинского агентства (ЕМА) и Всемирной организации здравоохранения (ВОЗ) предпочитают не замечать успехов вакцинации препаратом от коронавирусной инфекции «Спутник V», заявил директор Национального исследовательского центра эпидемиологии и микробиологии имени Гамалеи Александр Гинцбург в беседе с «Вечерней Москвой».
Материалы по теме
Путин объявил о нерабочих днях с 30 октября по 7 ноября.
В Москве ввели новые ограничения из-за коронавируса.
Специалист считает, что признание российского препарата пошло бы быстрее, если бы этот процесс основывался на результатах ее практического использования. По его словам, прививочная кампания показала, что вакцина справляется с защитой организма от широкого спектра штаммов COVID-19. «Однако чиновники EMA и отчасти ВОЗ не хотят этого видеть», — отметил он.
Гинцбург считает, что одной из вероятных причин также могут быть различия в европейском и российском законодательствах, порождающие задержки. «Еще надо учесть, что практически ни один российский препарат не был признан европейским сообществом», — сказал он.
Специалист добавил, что из-за таких «шероховатостей» находятся поводы придраться к российскому препарату.
Ранее Александр Гинцбург заявил, что комплекс мер, состоящий из иммунизации «Спутником V» и ревакцинации назальной вакциной, может защитить от коронавируса на 100 процентов. Он пояснил, что при использовании назальной вакцины образуется независимый барьер для проникновения вируса в организм человека на уровне местного иммунитета.
Какие страны принимают российские вакцины
Многие страны уже открыты для путешественников. Однако для въезда всё ещё требуется ПЦР-тесты, справка о вакцинации или же справка о перенесённом заболевании COVID-19. Разбираемся, куда можно отправиться туристам, привившимся российской вакциной.
Информация актуальная на момент публикации статьи.
Албания
С 1 сентября российским путешественникам для въезда в страну необходимо предоставить сертификат о вакцинации любым препаратом, зарегистрированным в РФ.
Привитые путешественники освобождаются от необходимости предъявления справки с отрицательным результатом ПЦР-теста по прибытии в страну.
Болгария
Вакцинированные «Спутником V» туристы освобождены от предъявления справки с отрицательным результатом ПЦР-теста по прибытии в страну.
Однако тем, кто привит другими российскими вакцинами, необходимо при посадке на борт самолёта предоставить результат ПЦР-теста, сделанного не ранее чем за 72 часа, или тест на антигены не старше 48 часов.
Венгрия
С 27 июля 2021 года гражданам России разрешен въезд при условии, что они прошли вакцинацию от коронавируса (признаны все российские вакцины). В этом случае никаких дополнительных тестирований не потребуется.
Греция
В Греции признаются сразу три российские вакцины — «Спутник V», «КовиВак» и «ЭпиВакКорона». Однако для всех туристов (в том числе вакцинированных) обязательным условием для въезда остаётся ПЦР-тест не старше 72 часов или тест на антигены не старше 48 часов.
В стране принимается только сертификат о вакцинации «Спутником V»: привитые им туристы освобождены от ПЦР-теста перед вылетом.
Привитые другими российскими вакцинами на Кипре проходят как невакцинированные, поэтому для въезда в страну должны предоставить ПЦР-тест не старше 72 часов и пройти повторное тестирование по прибытии.
Северная Македония
Как и в Болгарии, вакцинированные «Спутником V» туристы освобождены от предъявления справки с отрицательным результатом ПЦР-теста по прибытии в страну.
Привитым другими вакцинами необходимо предоставить результат ПЦР-теста, сделанного не ранее чем за 72 часа до въезда в страну, или тест на антигены не старше 48 часов.
Турция
В стране признаются все российские вакцины. Для въезда в Турцию без ПЦР-теста необходимо при посадке на борт самолета, а также на погранконтроле предъявить сертификат о полной вакцинации.
Хорватия
С тех пор как 26 июля 2021 года Хорватия ужесточила условия въезда в страну, все туристы вне зависимости от статуса вакцинации должны предоставить результат ПЦР-теста, сделанного не ранее чем за 72 часа до пересечения границы, или тест на антигены не старше 48 часов.
В стране признается только «Спутник V», но никаких послаблений это не даёт.
Черногория
С 21 августа 2021 года прибывающим туристам необходимо иметь сертификат вакцинации одной или обеими дозами «Спутника V».
Российский «Спутник V» также признан в ряде других стран: Армения, Бахрейн, Грузия, Египет, Иордания, Киргизия, Маврикий, Марокко, Молдова, Монголия, Оман, Португалия (только Мадейра), Таджикистан, Таиланд, Эстония.
Кривая траектория «Спутника»: почему российская вакцина не получила одобрение ВОЗ
Ирина Мишина
Речь идет о нарушениях, которые ВОЗ обнаружила в ходе проверки на заводе «Фармстандарт-Уфа Вита». Специалисты ВОЗ выразили опасения, связанные с осуществлением на предприятии «адекватных мер по снижению рисков перекрестного загрязнения вакцины» и относительно «контроля за асептическими условиями на линиях по ее розливу» и соблюдением стандартов производства. Что кроется за этими обтекаемыми фразами, мы попросили пояснить молекулярного биолога из США Ольгу Матвееву. Ответ оказался лаконичным.
Шумиха вокруг уфимского «Фармстандарта» и клинических испытаний «Спутника V» возникла не сегодня. Еще летом стало известно, что в Уфе, на предприятии, которое производит вакцину от коронавируса, привились меньше половины его сотрудников. Больше 60% «Фармстандарта» от вакцинации отказались по неизвестным причинам.
Справедливости ради стоит заметить, что возможные эффекты после вакцинации «Спутником» указаны в инструкции Минздрава, выпущенной в начале года. Среди них перечислены «гриппоподобный синдром» (повышение температуры, озноб, боль в мышцах, слабость и общее недомогание) и местные реакции на прививку (боль и отек в месте инъекции). Но у многих прививка проходит вообще бессимптомно. Автор этих строк перенесла и первый, и второй компонент вакцины «Спутник V» без какой-либо побочной реакции. Совсем.
В мае в связи с проверкой хода клинических испытаний российской вакцины «Спутник» грянул еще один скандал. Авторитетный научный журнал «Ланцет» (Lancet) 12 мая 2021 года опубликовал статью о российской вакцине «Спутник V». В ней создателей вакцины обвиняли в фальсификации данных и отчётов клинических испытаний. Несоответствия были найдены, в частности, в статистических отчетах о клинических испытаниях. В статье говорится: «Данные для вакцинированной группы на 20-й день относятся к бОльшему количеству людей, чем на 10-й день… Рисунок 2 был официально исправлен 20 февраля 2021 года, но в заявлении об исправлении не указаны причины, приведшие к такому исправлению… Количество участников, представленных в разных вакцинированных возрастных когортах, не соответствует заявленному общему количеству (n = 338 против n = 342). При таких несоответствиях мы сомневаемся в точности представленных данных». Также авторы научного журнала задавались вопросом, почему в группе из 9-и испытуемых уровень антител у всех совпадал на протяжении 21 дня.
СМИ объяснили все эти нестыковки нежеланием допускать российскую вакцину на международные рынки, поскольку она могла составить конкуренцию производителям других вакцин. Надеюсь, не надо объяснять, что производство вакцин от коронавируса – это сегодня бизнес, причем весьма прибыльный.
Мы попытались прояснить подробности скандального запрета ВОЗ на сертификацию вакцины «Спутник V» у наиболее авторитетных вирусологов страны: у профессора кафедры инфектологии и вирусологии Института профессионального образования Первого Московского государственного медицинского университета им.Сеченова Анатолия Альштейна и у академика Петра Чумакова, заведующего лабораторией пролиферации клеток Института молекулярной биологии.
«Со стороны ВОЗ речь идет не о претензиях к вакцине. Это претензии к ее производству в соответствии с надлежащей межгосударственной производственной практикой GMP. Это очень сложные правила, в мире они применяются в производстве с 60-х годов прошлого века, в России начали внедряться только с 90-х, и то с трудом. Это определенные характеристики помещения, оно должно быть стерильным, требования к одежде, к воздуху, правила контроля. На наших предприятиях, к сожалению, это соблюдается далеко не всегда. Возможно, претензии к уфимскому предприятию были в связи с несоблюдением стандартов GMP. Комиссия проверяла три площадки производителей, к двум претензий нет, только к Уфе. Если эти нарушения не исправят, производство вакцины на этой площадке станет проблематичным. Могут не дать дальше производить. Что касается конкуренции, то Россия не так уж сильно заинтересована в экспорте «Спутника V», он требуется в России, страна у нас большая, вакцины нужно много», — рассказал «НИ» профессор кафедры инфектологии и вирусологии Института профессионального образования Первого Московского государственного медицинского университета им.Сеченова Анатолий Альштейн.
Многие эксперты склонны видеть в претензиях ВОЗ к производителю «Сутника V» политический подтекст. Возможно, доля истины в этом есть, учитывая, что заказы на поставку вакцин исчисляются миллиардами. Так, журналисты агентства Reuters подсчитали: стоимость 300 миллионов доз вакцины Pfizer, о планах купить которые заявляла глава Европейской комиссии Урсула фон дер Ляйен, составит 4,6 миллиарда евро. Представители Pfizer отметили, что сделка с ЕС — самый крупный контракт компании на поставку препарата.
Не проходит и дня, чтобы российский государственный фонд РФПИ не сообщил с ликованием о том, в какой стране земного шара только что снова одобрили финансируемую им вакцину «Спутник V». Ведь «V» значит «победа». Но до победы, как выяснилось, далековато. Из более, чем 60 стран, одобривших, по данным РФПИ, «Спутник V», заказ на вакцину оформили 45 государств. При этом половина заказов приходится на четыре страны: Турцию, Мексику, Аргентину и Венесуэлу.
Да и в самой России отношение к «Спутнику» неоднозначное. Согласно исследованию Credit Suisse, доверие к вакцинации в России значительно ниже по сравнению с другими странами: в Китае пройти вакцинацию готовы около 90% респондентов, в Бразилии 80%, в Индии около 70% и около 60% в Турции. В России же этот показатель составил всего 40%».
Так или иначе, проблемы с производством «Спутник V» отрицать уже просто нелепо. В общем-то нам не привыкать: мы были первыми и в космосе, и в балете, и с прививками тоже все быстро вышло. Но потом наступили горькие будни. И выяснилось, что за бодрыми рапортами кроется масса недочетов. Может, стоит уже перестать пытаться обогнать кого-то и подумать о качестве? Тем более, когда речь идет о здоровье миллионов людей.
Какие вакцины от коронавируса используют в мире
В России массовая вакцинация от COVID-19 началась 18 января. В мире на конец марта прививают население уже в 141 стране. Какие вакцины используют — в обзоре РБК
«Спутник V», разработанная Центром эпидемиологии и микробиологии имени Н.Ф. Гамалеи, получила госрегистрацию Минздрава в августе. Вакцину зарегистрировали после второй фазы испытаний, а третий финальный этап стартовал в сентябре.
Эффективность «Спутника V» разработчики оценили выше, чем в 95%. Эти данные были получены при исследовании добровольцев, получивших две инъекции препарата. «Спутник V» разработан в двух видах: замороженном (жидкая «Гам-КОВИД-Вак» хранится при температуре не выше минус 18 °С) и лиофилизированном (порошок «Гам-КОВИД-Вак-Лио» хранится при температуре от плюс 2 до 8 °С). Препарат вводится двукратно с интервалом в три недели. В ФАС заявили, что стоимость инъекции «Спутником V» не превысит 1 тыс. руб.
5 декабря Москва стала первым российским регионом, начавшим масштабную вакцинацию «Спутником V», а с 18 января началась массовая вакцинация во всей России. Первой среди зарубежных стран, зарегистрировавших российский препарат, стала Белоруссия. Такое же решение приняли власти Аргентины, Венесуэлы и некоторых других стран
Немецкая компания BioNtech разработала вакцину совместно с американской Pfizer. На третьей фазе клинических испытаний препарат показал эффективность на уровне 95%. У вакцины есть обязательное условие использования: ее нужно хранить при температуре не выше минус 70 градусов Цельсия, а после разморозки она пригодна в течение пяти дней. Разработка Pfizer-BioNTech вводится в два приема с промежутком в три недели. Великобритания стала первой страной, одобрившей применение Pfizer и BioNTech, за ней последовали Канада, США и страны Европы и Ближнего Востока. Массовая вакцинация в США и Канаде началась 14 декабря, а в европейских странах — 27 декабря
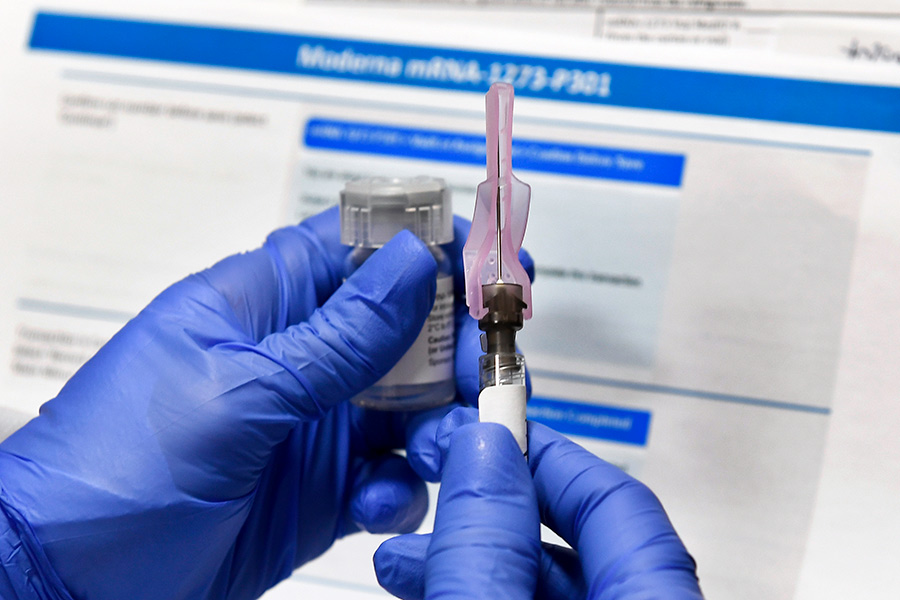
Эффективность вакцины американской фармацевтической компании Moderna составила 94,5%, а при тяжелых случаях заболевания — 100%. Вакцин вводят в два приема с интервалом в четыре недели. Препарат можно до 30 дней хранить при 2–8 градусах Цельсия. В этом году Moderna планирует выпустить 600 млн доз.
18 декабря США одобрили использование Moderna и заказали 200 млн доз с возможностью покупки еще 300 млн. Следом разрешение на использование она получила в Канаде, Израиле, Великобритании и Швейцарии. 6 января Европейский регулятор одобрил препарат американского производства
Вакцина, разработанная британской компанией AstraZeneca вместе с Оксфордским университетом, показала эффективность на уровне 70%, а при одном из способов введения (сначала вводят половину дозы, а через месяц — полную) — 90%.
Великобритания первой в мире разрешила использовать AstraZeneca и заказала 100 млн доз. Препарат получил разрешение на использование в Индии, Аргентине, Доминиканской Республике, Сальвадоре, Мексике и Марокко.
В марте 2021 года вокруг препарата AstraZeneca разразился скандал. Более 15 стран Европы, в том числе Германия, Франция, Испания, и некоторые страны Азии и Африки частично или полностью отказались от препарата. Такое решение власти приняли на фоне сообщений об образовании тромбов у привившихся и смертельных исходах.
В самой компании указывают на отсутствие доказательств, что к смерти пациентов привела именно вакцинация. 18 марта вышло заключение Европейского агентства лекарственных средств (EMA) о том, что AstraZeneca не увеличивает риски по образованию тромбов. ВОЗ также продолжает рекомендовать использование препарата. После этих заявлений европейские страны, кроме некоторых скандинавских, возобновили иммунизацию AstraZeneca.
Пептидная вакцина новосибирского научного центра «Вектор» «ЭпиВакКорона» получила регистрационное удостоверение в октябре 2020 года. Она, как и «Спутник V», была зарегистрирована после двух стадий клинических испытаний.
Вакцину вводят двукратно внутримышечно с интервалом в две-три недели. Препарат можно хранить при температуре от 2 до 8 градусов выше нуля. В Роспотребнадзоре отмечают, что вакцина подходит для пожилых и людей с хроническими заболеваниями. В центре «Вектор» заявили, что стоимость препарата будет эквивалента стоимости «Спутника V», то есть около 1 тыс. руб.
Глава Роспотребнадзора Анна Попова сообщала, что «ЭпиВакКорона» поступила в гражданский оборот в пяти городах — Москве, Санкт-Петербурге, Ростове-на-Дону, Туле и Новосибирске. После завершения пострегистрационных клинических испытаний в 2021 году может начаться массовая вакцинация «ЭпиВакКороной»
Инактивированная вакцина CoronaVac, разработанная китайской Sinovac Biotech, хранится в холодильнике при плюс 2–8 градусах Цельсия. В Sinovac заявили, что обеспечат производство 300 млн доз в год. Для иммунизации требуется две дозы, а это означает, что CoronaVac смогут привиться 150 млн человек — чуть больше десятой части населения Китая.
Данные об эффективности вакцины от Sinovac разнятся. Последние испытания в Бразилии показали 50,4% эффективности, а в Индонезии и Турции — 65,3% и 91,5% соответственно.
Вакцина была одобрена для экстренного применения в группах высокого риска в Китае с июля. Использование этой вакцины 13 января разрешили власти Турции. Несколько азиатских стран — Сингапур, Малайзия и Филиппины, а также Бразилия и Украина подписали соглашения о закупках CoronaVac
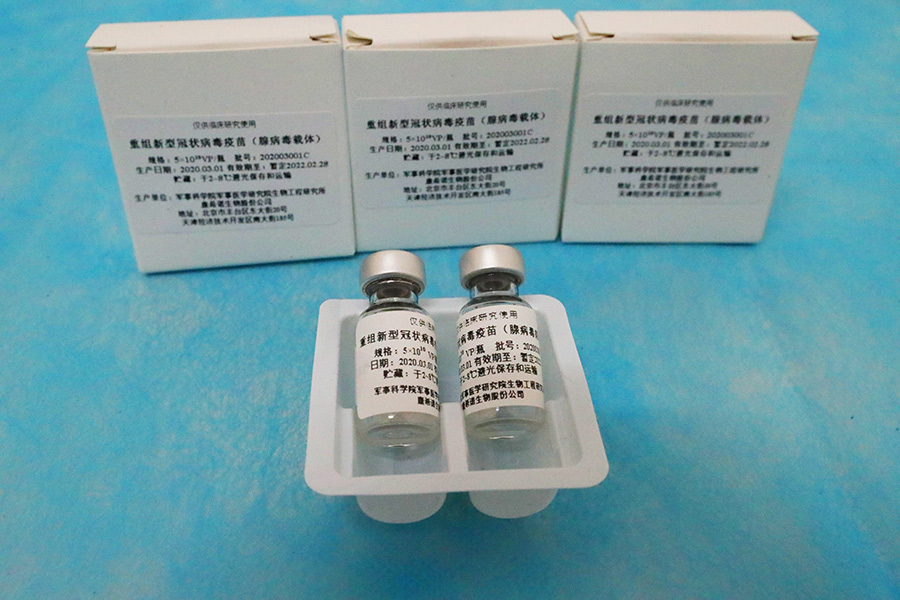
Еще одна китайская вакцина Ad5-nCoV («Конвидеция»), на основе человеческого аденовируса типа 5, разработана фармкомпанией CanSino Biologics. Преимуществом этого препарата является однократное введение, а также возможность хранения при температуре от плюс 2 до плюс 8 градусов Цельсия.
В ноябре 2020 года были поданы документы в Минздрав России для регистрации вакцины. В декабре Минздрав выдал разрешение на проведение третьего международного этапа клинического исследования Ad5-nCov. В случае, если вакцина покажет высокую эффективность и безопасность, CanSino Biologics с российским «Петроваксом» организуют ее производство в России.
Согласно промежуточным результатам третьей фазы клинических испытаний в России, Ad5-nCoV показала эффективность в 92,5%. Окончательные результаты исследования появятся в середине 2021 года
Другую китайскую инактивированную вакцину разработала China National Biotec Group (CNBG) (подразделение Sinopharm). Она не требует отрицательной температуры хранения и вводится двумя дозами с интервалом в две недели.
30 декабря Sinopharm объявила, что на третьем этапе испытаний препарат показал эффективность на 79%. Однако Объединенные Арабские Эмираты, которые одобрили вакцину Sinopharm в этом месяце, заявили, что эффективность вакцины составила 86%. Кроме Китая и ОАЭ вакцина Sinopharm проходит клинические испытания в Бахрейне, Иордании, Перу и Аргентине.
В Китае препарат Sinopharm с июля используется в рамках программы по экстренному вакцинированию, а 31 декабря Государственное управление по лекарственным средствам Китая одобрило препарат для широкого использования
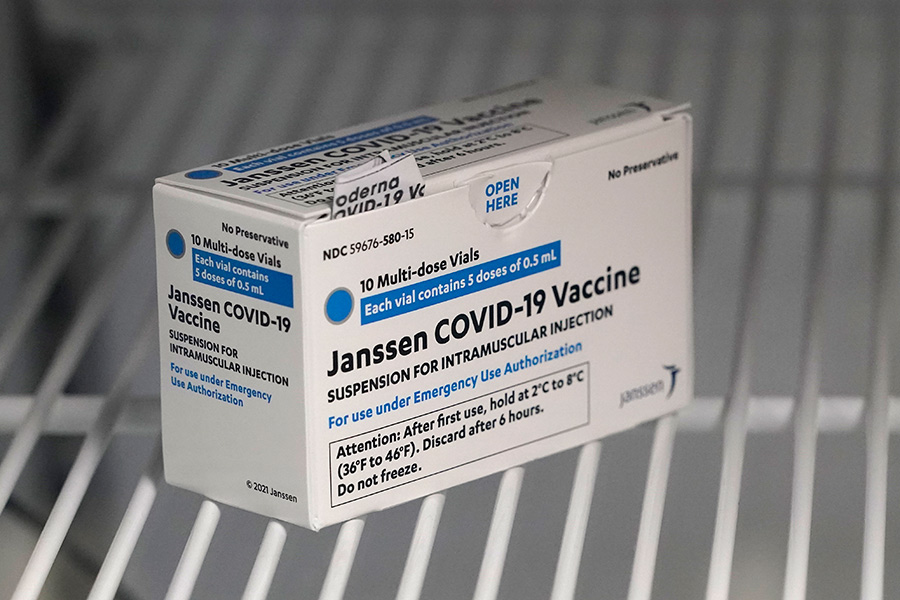
Вакцину Janssen американской корпорации Johnson & Johnson 11 марта одобрил ЕС. Чуть раньше экстренное применение препарата разрешило Управление США по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA). Препарат также включен в список для экстренного применения ВОЗ.
В ходе клинических испытаний с участием 44 тыс. человек из США, Южной Африки и стран Латинской Америки препарат показал эффективность в 67%.