какие связи в хлориде аммония
Основные понятия о соединении
О том, что представляет собой рассматриваемая химическая связь, можно понять уже по одной только структурной формуле хлорида аммония — NH4CL, притом что это вещество реально получить не только посредством искусственного синтезирования, но и в природной среде, в которой он представляется в виде минерального нашатыря. При нормальном температурном режиме являет собой белые кристаллы без запаха и присутствия соли.
Физические свойства NH4CL
Объем одной кубической сингонии хлористого аммония, под которой подразумевается элементарная ячейка кристалла, определяется по актуальной для простейшего геометрического куба формуле, где a возводится в третью степень. Чтобы вычислить эту величину рассматриваемого соединения, достаточно просто знать, чему равно a, которое является константой, соответствуя 0,38758 нанометра при z=1. Что касается остальных физических свойств и параметров, то среди ключевых из них стоит выделить:
Среди прочих особенностей NH4CL стоит выделить его высокую степень растворимости как в холодной, так и в горячей воде. К примеру, при нулевой температуре жидкости в ее 100 граммах растворяется 29,4 грамма вещества, тогда как в кипятке расходится уже 77,3 грамма. Стоит отметить, что, помимо обычной воды, соединение легко растворяется в жидком аммиаке, а также в безводных растворителях, но только при условии использования связи в порошкообразном виде, а не в концентрированном водном растворе.
В этом случае в 100 граммах этанола удастся растворить до 0,6 грамма кристаллов, а в метаноле до 3,3 грамма. Если же использовать водные растворы, то в процессе гидролиза, подразумевающего собой сольволиз водой, в них будет неизменно наблюдаться слабокислая реакция.
Что касается температуры кипения таких растворов, то она превышает стандартные 100 градусов, достигая на столбике термометра отметки в 116 градусов Цельсия.
Химические особенности связи
Вещество имеет множество химических особенностей, среди которых — вступление в реакцию со щелочными соединениями. К примеру, с тем же нитритом натрия хлористый аммоний начинает реагировать при достижении 100-градусной температуры, образуя не только воду и азот, но и новое соединение хлорида и натрия. Среди прочих свойств связи стоит необходимо обозначить:
Гидролиз хлорида аммония происходит только по катиону при устойчивом поддержании кислой среды. В этом случае актуальным будет следующее уравнение: NH4Cl + H2O ↔ NH4OH +HCl.
Помимо прочего, связь имеет свойство вступать в реакцию с азотнокислым серебром (NH4CL+AgNO3 → AgCl ↓ +NH4NO3) и нитритом натрия (NH4CL+NaNO2 → NaCl+N2 ↑ +2H20). В первом случае в качестве реакции можно наблюдать выпадение хлористого серебра в виде характерного белого осадка, который моментально темнеет при воздействии естественных источников света, тогда как для второго актуальным остается разложение на натрия хлорид, воду и азот.
Получение и практическое применение
Удивительно, но хлористый аммиак научились добывать еще древние греки и египтяне, соскребавшие ценное вещество со стен застывших вулканических пород. Естественно, сегодня технологии таковы, что использовать подобные природные образования для того, чтобы получать нашатырь, не приходится.
Синтезирование вещества
В настоящее время хлорид аммония добывают в промышленных масштабах для разных нужд, используя для этого такой универсальный метод, как нагревание и упаривание маточного раствора, для получения которого приходится добиваться других химических реакций. Речь идет о выработке сырьевых остатков, образующихся в процессе разложения соединения гидрокарбоната натрия, а попросту пищевой соды, для чего необходимо пропустить диоксид углерода (углекислый газ) через раствор натрия хлорида и аммиака.
Если же на повестке дня стоит вопрос синтезирования соединения в лабораторных условиях, то тогда можно ограничиться более простыми решениями, которые чаще всего сводятся к соединению хлорводорода с аммиаком, предварительно пропускаемых через раствор натрия хлорида. Кроме того, вполне реально вывести связь посредством прямого контакта таких элементов, как аммиак и хлор.
Стоит отметить, что в современной химической промышленности активно используются всевозможные производные соединения, будь то диметиламмоний, метиламмоний, этиламмоний и прочие вариации. Объясняется такой спрос довольно просто, ведь они получили широкое применение в фармакологии, легкой и пищевой промышленности, виноделии и других производственных сегментах, продолжая находить для себя новые сферы использования.
Использование хлорида аммония
В Древнем Египте хлористый аммоний использовался в качестве ароматных курений для божества по имени Аммоний, откуда, собственно, и пошло наименование самого вещества. Чуть позже его применение освоили и на Востоке, так как название «нашатырь» имеет арабское происхождение. Научно-технический прогресс расширил сферы применения соединения, продолжая открывать для него новые горизонты. Так, в настоящее время NH4CL активно используется в следующих сферах с соблюдением всех соответствующих ГОСТов:
Соединение имеет довольно широкую область применения и во многих других сферах. К примеру, сегодня его активно используют для изготовления красителей в легкой промышленности, печати на ситце и других тканях, в лужении, для проведения лабораторных исследований, для дымообразования, проявления фотографических пленок, так как связь прекрасно фиксирует изображение, и пр.
Роль в медицине
Нельзя не отметить и фармакологические свойства вещества, которое обладает довольно мощным отхаркивающим и диуретическим эффектом. В виде медикаментозного препарата хлористый аммоний быстро абсорбируется стенками кишечника, проникая в общий кровяной ток, и метаболизируется в печени до состояния мочевины, после чего наступает период полураспада и вывод из организма. При этом может наблюдаться подкисление урины и учащенное мочеиспускание без изменений выделяемого объема в меньшую сторону. Во время каждого такого мочеиспускания происходит обильное выведение калийных ионов.
Действие препаратов неизменно сопровождается антисептическим эффектом и умеренным раздражением для некоторых органов и систем. Применение медикаментов на основе NH4CL способствует разжижению и выходу мокроты из верхних и нижних дыхательных путей. Что касается выраженности диуретического эффекта, то не последнюю роль в этом вопросе играет состояние почек пациента и характер текущего заболевания. Если же говорить о назначении лекарственного средства, то оно становится актуальным в следующих случаях:
Препараты на основе хлористого аммония запрещены к приему в случаях ярко выраженных отклонений в работе печени и почек, при обильном выделении соляной кислоты в урине на фоне устойчивого развития дефицита натрия, а также во время беременности и лактации. Кроме того, возможны патологические проявления, которые могут выражаться в виде расстройств диспептического характера, повышенного потоотделения, общей слабости, изменения цвета кожных покровов на более бледные, мышечного тремора, брадикардии, чреватой переходом в коматозное состояние, и общей интоксикации организма.
Химические связи
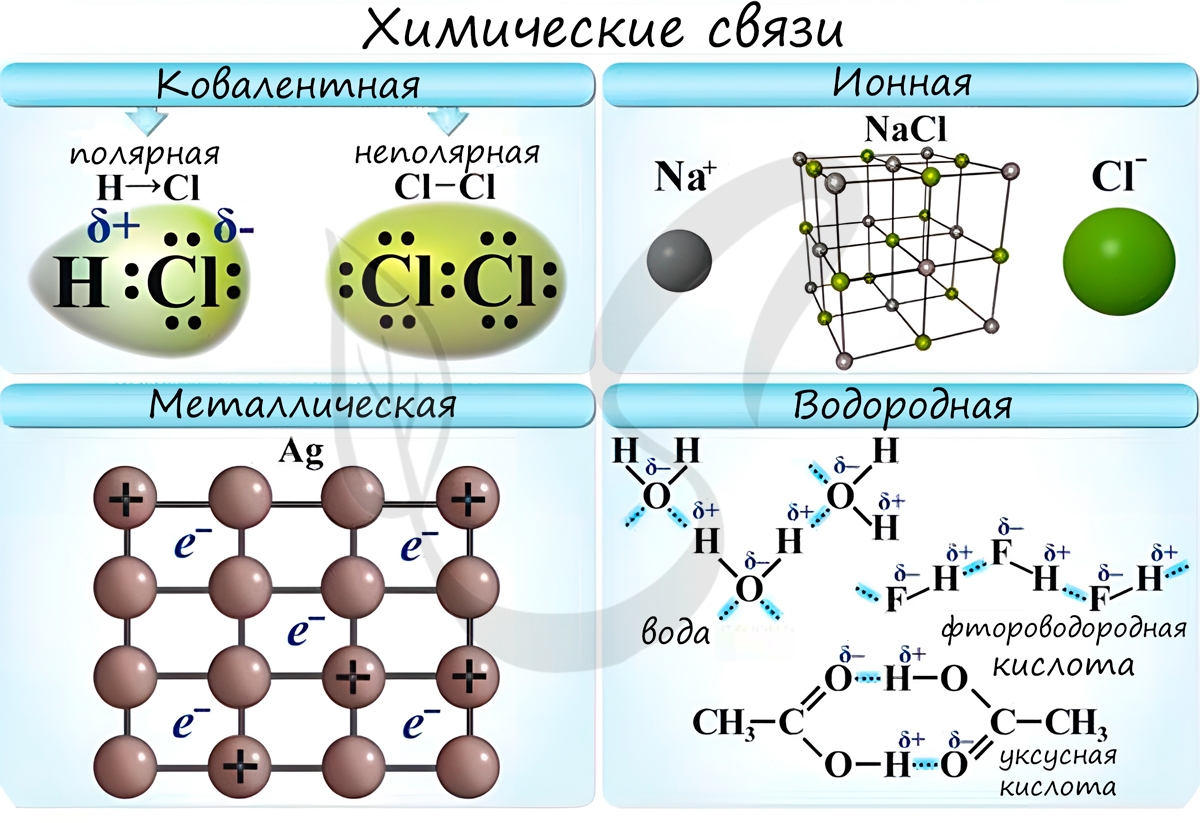
Различают несколько типов химических связей: ковалентная, ионная, металлическая, водородная.
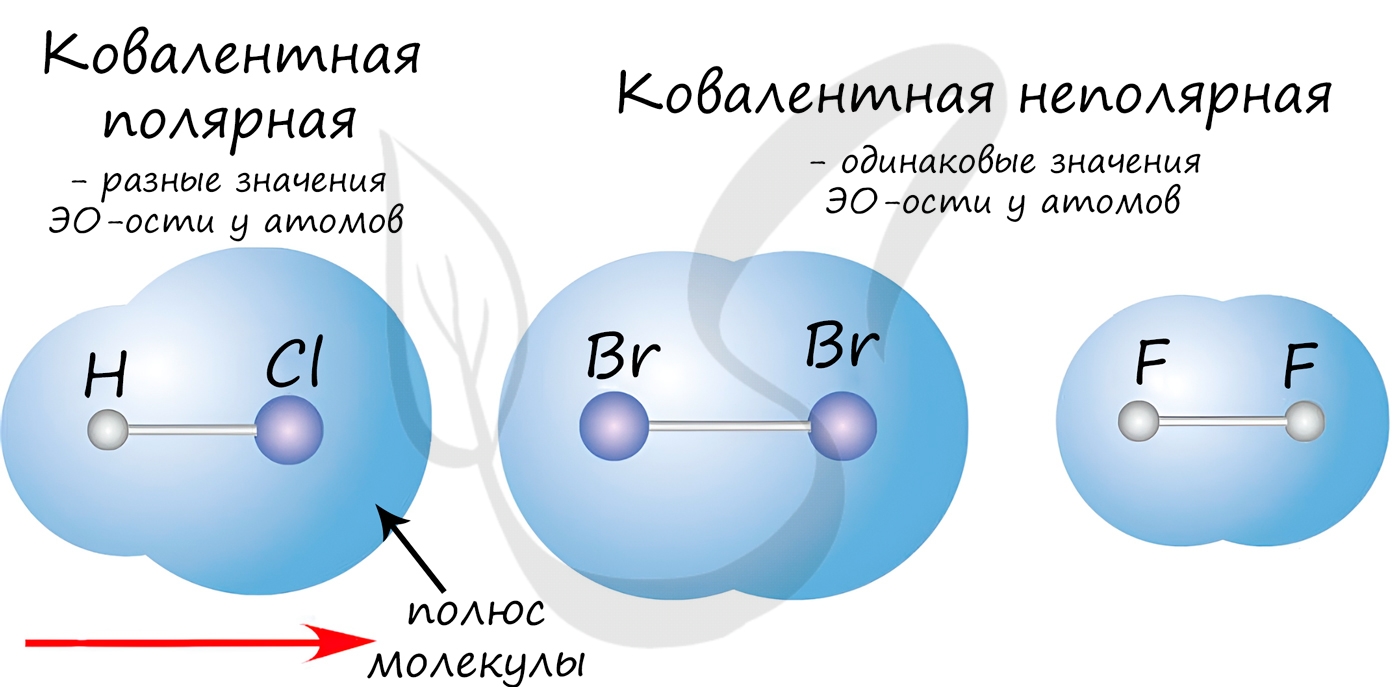
Ковалентная связь возникает между двумя атомами по обменному механизму (обобществление пары электронов) или донорно-акцепторному механизму (электронов донора и свободной орбитали акцептора).
Ковалентной связью соединены атомы в молекулах простых веществ (Cl2, Br2, O2), органических веществ (C2H2), а также, в общем случае, между атомами неметалла и другого неметалла (NH3, H2O, HBr).
Существует донорно-акцепторный механизм образования ковалентной связи, при котором один атом выступает в качестве донора неподеленной электронной пары. Другой атом не тратит свои электроны, а только лишь предоставляет орбиталь (ячейку) для этой электронной пары.
Ионная связь
В наиболее частом случае ионная связь образуется между типичным металлом и типичным неметаллом. Примеры:
Большой подсказкой служит таблица растворимости, ведь все соли имеют ионные связи: CaSO4, Na3PO4. Даже ион аммония не исключение, между катионом аммония и различными анионами образуются ионные связи, например в соединениях: NH4I, NH4NO3, (NH4)2SO4.
Часто в химии встречаются несколько связей внутри одной молекулы. Рассмотрим, например, фосфат аммония, обозначив тип каждой связи внутри этой молекулы.
Металлическая связь
«Облако» электронов в металлах способно приходить в движение под различным воздействием. Именно оно является причиной электропроводности металлов.
Водородная связь
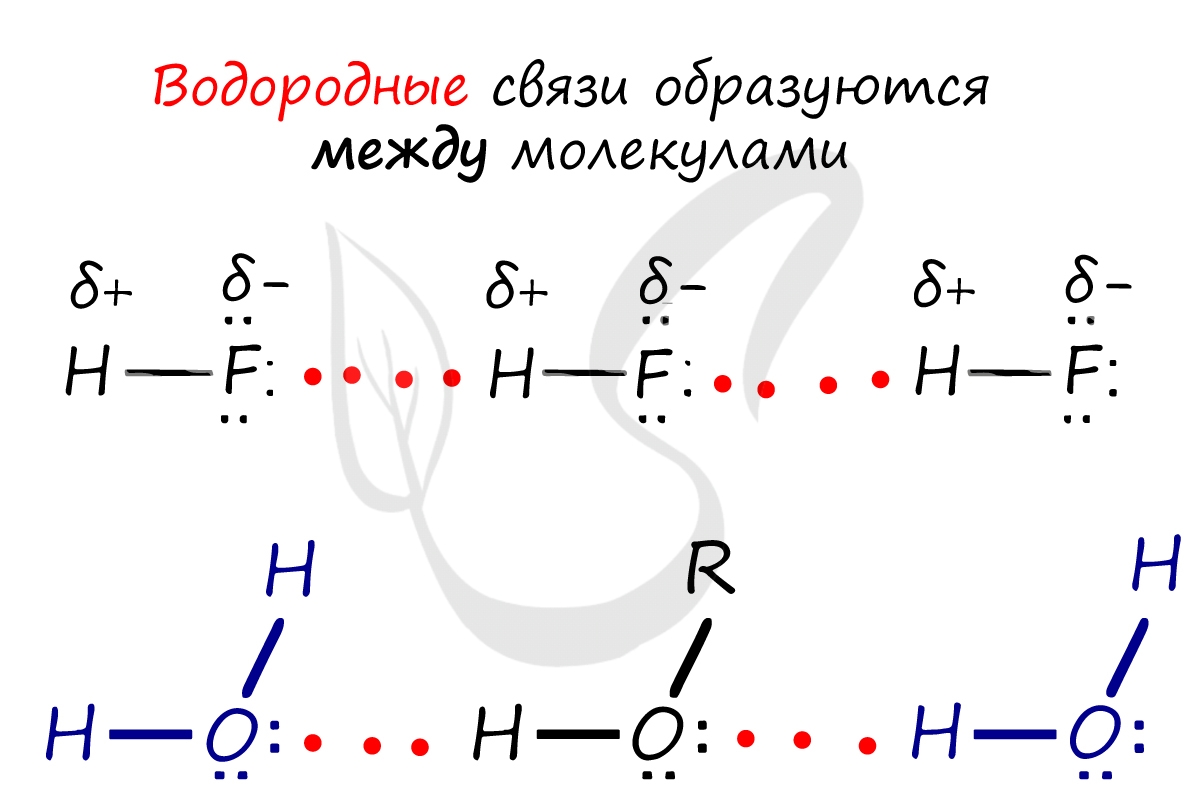
Водородные связи возникают между атомом водорода и другим более электроотрицательным атомом (O, S, N, C).
Отчасти за счет водородных связей наблюдается то самое исключение, связанное с усилением кислотных свойств в ряду галогеноводородных кислот: HF → HCl → HBr → HI. Фтор является самым ЭО-ым элементов, сильно притягивает к себе атом водорода другой молекулы, что снижает способность кислоты отщеплять водород и снижает ее силу.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Какие связи в хлориде аммония
На своем сайте я выкладываю уникальные, адаптивные, и качественные шаблоны. Все шаблоны проверяются на всех самых популярных браузерх.
Раньше я занимался простой вёрсткой одностраничных, новостных и т.п. шаблонов на HTML, Bootstrap. Однажды увидев сайты на DLE решил склеить пару шаблонов и выложить их в интернет. В итоге эта парочка шаблонов набрала неплохую популярность и хорошие отзывы, и я решил создать отдельный проект.
Кроме шаблонов я так же буду выкладывать полезную информацию для DataLife Engin и «статейки» для веб мастеров. Так же данный проект будет очень полезен для новичков и для тех, кто хочет правильно содержать свой сайт на DataLife Engine. Надеюсь моя работа вам понравится и вы поддержите этот проект. Как легко и удобно следить за обновлениями на сайте?
Достаточно просто зарегистрироваться на сайте, и уведомления о каждой новой публикации будут приходить на вашу электронную почту!
Задание 1
Какие два механизма образования ковалентной связи вы знаете? Обменный и донорно-акцепторный.
Чем отличается один механизм от другого? При обменном механизме для образования общей электронной пары каждый атом представляет в совместное пользование определённые электроны, а при донорно-акцепторном — один из атомов предоставляет электронную пару (он выступает донором электронной пары), а другой — вакантную орбиталь (его называют акцептором).
Задание 2
Что называется кратностью ковалентной связи? Кратностью ковалентной связи называется число электронных пар, обобществлённых между двумя соседними атомами.
Запишите молекулярные и структурные формулы органических и неорганических веществ с ковалентной связью различной кратности.
| Кратность связи | Молекулярная формула | Структурная формула |
| Одинарная связь | HCl | H–Cl |
| C2H6 | H3C–CH3 | |
| Двойная связь | O2 | O=O |
| C2H4 | H2C=CH2 | |
| Тройная связь | N 2 | N≡N |
| C2H2 | HC≡CH |
Задание 3
Какие типы кристаллических решёток соответствуют веществам с ковалентной связью? Молекулярные и атомные кристаллические решётки.
Сравните свойства веществ с молекулярной и ионной кристаллическими решётками. Вещества с молекулярной кристаллической решёткой легкоплавкие, летучие, часто обладают запахом, а вещества с ионной кристаллической решёткой тугоплавкие, не летучие, в основном не обладают запахом.
Задание 4
Охарактеризуйте атомные кристаллические решётки. В узлах атомных кристаллических решёток располагаются отдельные атомы, связанные между собой очень прочными ковалентными связями. Для веществ с атомными кристаллическими решётками характерны тугоплавкость и высокая твёрдость.
Какие два типа веществ (по составу) их образуют? Простые и сложные вещества.
Сравните вещества с атомными и ионными кристаллическими решётками. Вещества с ионными кристаллическими решётками хрупкие, тугоплавкие, нелетучие, многие растворимы в воде, а с атомными кристаллическими решётками тугоплавкие, очень твердые, не растворимые в воде.
Какие виды химической связи в хлориде аммония?
Ионные уравнения для второй задачи приведены без учёта диссоциации слабых электролитов на ионы.
1) Вода реагирует со многими металлами с выделением водорода:
2Na + 2H2O = H2 + 2NaOH (бурно)
2K + 2H2O = H2 + 2KOH (бурно)
3Fe + 4H2O = 4H2 + Fe3O4 (только при нагревании)
Не все, а только достаточно активные металлы могут участвовать в окислительно-восстановительных реакциях этого типа. Наиболее легко реагируют щелочные и щелочноземельные металлы I и II групп.Из неметаллов с водой реагируют, например, углерод и его водородное соединение (метан). Эти вещества гораздо менее активны, чем металлы, но все же способны реагировать с водой при высокой температуре:
C + H2O = H2 + CO (при сильном нагревании)
CH4 + 2H2O = 4H2 + CO 2 (при сильном нагревании)
2) Вода разлагается на водород и кислород при действии электрического тока. Это также окислительно-восстановительная реакция, где вода является одновременно и окислителем, и восстановителем:
3) Вода реагирует со многими оксидами неметаллов. В отличие от предыдущих, эти реакции не окислительно-восстановительные, а реакции соединения:
SO2+H2O=H2SO3SO3+H2O=H2SO44) Некоторые оксиды металлов также могут вступать в реакции соединения с водой. Примеры таких реакций мы уже встречали:
CaO+H2O=Ca(OH)2Не все оксиды металлов способны реагировать с водой. Часть из них практически не растворима в воде и поэтому с водой не реагирует. Мы уже встречались с такими оксидами. Это ZnO, TiO2, Cr2O3, из которых приготовляют, например, стойкие к воде краски. Оксиды железа также не растворимы в воде и не реагируют с ней.
5) Вода образует многочисленные соединения, в которых ее молекула полностью сохраняется. Это так называемые гидраты. Если гидрат кристаллический, то он называется кристаллогидратом. Например: CuSO4+5H2O=CuSO4.5H2O6) Особая реакция воды – синтез растениями крахмала (C6H10O5)n и других подобных соединений (углеводов), происходящая с выделением кислорода:(10-11 класс)6nCO2 + 5nH2O = (C6H10O5)n + 6n O2 (при действии света)
Все больше вроде как нет.
Хлорид аммония (нашатырь, Е510): описание, реакции, применение
Хлорид аммония – это неорганическое азотсодержащее вещество, имеющее минеральную природу. Нашатырь, как часто называют хлорид аммония, обладает высокой химической активностью, поэтому используется во многих сферах. В пищевой промышленности хлористому аммонию присвоен статус пищевой добавки Е510, но применение ограничено в связи с неприятным вкусом и запахом. Может вноситься в почву в качестве удобрения, содержащего азот и хлор. Также его применяют в медицине, металлургии и фотографии. Вещество обладает отхаркивающими, мочегонными свойствами, назначается для откашливания мокроты при заболеваниях дыхательных путей, а также в качестве натурального диуретика.
Что такое хлорид аммония, формула
Хлорид аммония – это собой среднюю хлористую соль аммония с химической формулой NH4Cl. В нормальных условиях хлористый аммоний имеет вид белого или желтоватого крупнодисперсного порошка, состоящего из кристаллов прямоугольной формы. Гигроскопичность слабая, не имеет запаха.
Вещество переходит из твёрдого состояния в газообразное при температуре 337,6 °С, в жидком состоянии кипит при очень высокой температуре (520°С). Хорошо растворим в органических растворителях, особенно в спиртах: в метаноле больше, чем в этаноле. Растворяется в воде и жидком аммиаке, при повышении температурного режима растворимость медленно возрастает, наибольшая наблюдается при 100°С.
Насыщенные водные растворы нашатыря имеют меньшую точку кипения (116 °С), проявляют слабокислую реакцию в результате сольволиза водой, поскольку происходит отделение большого количество протонов водорода (H + ).
В природе хлорид аммония встречается в виде минерала нашатыря, имеющего сходную химическую формулу, но с примесями железа (Fe), йода (I) и брома (Br). Обладает жёсткой кубической кристаллической решеткой. Кристалл белого, желтоватого, сероватого или коричневатого цвета, со стеклянным блеском, обладает низкой хрупкостью, режущийся, минимальной твёрдости по шкале Мооса. При раскалывании нашатырь образует раковистый излом.
Минерал формируется в естественных условиях в результате вулканической активности или в районе горячих источников. Имеет вид налётов, корочек, редко образуя массивные скопления. Чаще всего его находят в залежах разложившегося помёта верблюдов, летучих мышей, морских птиц. Нашатырь имеет неприятный резкий горько-солёный вкус, достаточно токсичен, запах едкий, отрезвляющий, в прошлом использовался как компонент нюхательной соли: водным раствором минерала пропитывали углеаммонивые соли.
Молекула хлорида аммония
Реакции с хлоридом аммония
Хлористый аммоний проявляет сходные с другими солями аммония химические свойства. При взаимодействии с водой начинается реакция гидролиза – разложение вещества с образованием воды и ионов. При этом разрушается остаток основания (NH4OH), т.е. сольволиз протекает по катиону:
При нагревании образуется аммиак и соляная кислота:
Химическое разложение происходит под воздействием концентрированной серной кислоты:
а также при взаимодействии с щелочами щелочно-земельных металлов:
При этом обязательно выделяется хлороводородная кислота или аммиак.
Хлорид аммония реагирует с металлами с выделением нитрида водорода:
Взаимодействие с оксидами протекает тяжело, требует подогревания или участия катализаторов. Так, при температуре около 300°С идёт реакция с окисью меди:
При этом образуется молекулярный азот и выпадает чистая медь.
При слабом подогревании (60-70°С) или пропускании электрического тока нашатырь взаимодействует с хлором, образуя маслянистую летучую жидкость – трёххлористый азот:
Активно идут реакции с различными нитратами, например, с нитратом серебра:
Формирующийся осадок хлорида серебра белого цвета темнеет на свету.
Хлорид аммония реагирует и с нитритами: нитритом натрия, калия и других металлов:
История использования
Хлорид аммония – это вещество, которое было известно со времен до нашей эры. Впервые его использовали в Египте, получая путём возгонки (перехода из твёрдого состояния в газ). Печи топились верблюжьим навозом, в котором в изобилии был аммиак. В результате образовывалась сажа, из которой добывалось вещество. Нередко минерал находили в пустынях, в местах оазисов, где скапливался кал и моча ездовых животных. Резко пахнущие кристаллы использовали в мистических практиках жрецы бога Амона. Вдыхая едкий запах, люди ощущали рефлекторную стимуляцию дыхательного центра, онемение. Эти эффекты связывались с религиозным общением. Хлориду аммония дали название «нушадир», что в переводе с арабского означает «аммиак».
Спустя столетия, в период Средних веков, алхимики экспериментировали с хлористой солью аммония. Смешивая аммиак с летучий хлористоводородной кислотой, они видели образование густого белого дыма. Активную реакцию нейтрализации аммиака (основания) кислотой (HCl) они объясняли также с точки зрения мистики: считалось, что газы представляют собой богов, в результате сражения которых появляется дым и белый налёт на предметах.
По мере развития науки химики стали использовать кристаллы нашатыря в медицинских целях. Из него готовили водный раствор, в котором смачивали платки или марли для приведения в чувства людей, упавших в обморок. Порошок применялся в качества нюхательной соли при головных болях, в стрессовых ситуациях, при заболеваниях верхних и нижних дыхательных путей, для успокоения при истерических припадках. Безводный хлорид аммония не имеет запаха, однако со временем постепенно разлагается, выделяя аммиак, который и даёт местно-раздражающий эффект.
Сначала нашатырь импортировался в страны Европы и в Россию из Индии и Египта, затем учёные стали синтезировать его самостоятельно. Повсеместное активное применение вещества началось в 1710-1800 годах. В 1710 году в России был построен первый завод по производству хлористого аммония.
Получение и производство
В лабораторных условиях хлорид аммония получают взаимодействием аммиака с хлором:
Первые производственные методы получения хлористого аммония были основаны на нейтрализации водного раствора аммиаком соляной кислоты.
Сегодня большое количество Е510 производится как побочный продукт при выпуске пищевой соды. Общее уравнение реакции:
Производство проходит в несколько этапов:
Так поступают заводы, специализирующиеся на производстве двууглекислого натрия. Для них наиболее экономически выгодно совмещать выпуск двух продуктов, поскольку в наличии изначально есть все необходимые реактивы.
Иногда получение хлорида аммония может быть не связано с пищевой содой. Для этого используют самую первую технологию – взаимодействие раствора аммиака и хлористоводородной кислоты. При этом производство идёт с участием крупного и дорогостоящего оборудования.
Исходный метод был усовершенствован, т.к. имел некоторые недостатки: выпаривание водного раствора для выделения нужного соединения происходило с затратами тепла, сопровождалось сильной коррозией выпарных устройств, в результате производитель нёс убытки. Поэтому было решено заменить водный раствор аммиака насыщенным растворов – таким, в котором концентрация вещества наибольшая, а содержание воды – наименьшее. Последовательность стадий производства:
Выход вещества при таком способе довольно большой. Однако производитель сталкивается с токсичными и опасными реактивами, во время синтеза есть вероятность образования взрывоопасного трихлорида азота (Cl3N). Поэтому чаще всего вещество, поступающее в продажу, производится вместе с пищевой содой.
Воздействие на организм
При правильном применении хлорид аммония не оказывает негативного воздействия на организм. Нужно строго следовать рекомендациям лечащего врача, если вещество было назначено в качестве мочегонного, отхаркивающего средства.
Вред для организма, противопоказания, побочные эффекты
Частое или интенсивное вдыхание паров нашатыря может привести к ожогу слизистой, головным болям. Злоупотребление пищевыми продуктами, в состав которых входит Е510, может привести к отравлению, тошноте и болям в животе, аллергии.
Главное противопоказание к применению хлористого аммония – индивидуальная непереносимость. Она может выражаться в отёках, развитии тяжёлых аллергических реакций. Вещество противопоказано следующим группам лиц:
Среди побочных эффектов после использования нашатыря головокружение, головная боль, тошнота, временная потеря или притупление вкусовой чувствительности, обоняния, а также сыпи, кашель.
Полезные свойства
Хлористый аммоний обладает выраженной фармакологической активностью. Воздействуя через рецепторы носа на дыхательный центр, он производит мощный раздражающий эффект. При этом активизируются базовые защитные рефлексы: кашель и чихание. Средство улучшает отхождение мокроты из нижних дыхательных путей при бронхите, пневмонии, способствует сужению сосудов полости носа (избавляет от насморка).
Хлорид аммония проявляет мочегонные свойства. При этом его принимают перорально в виде слабого раствора, который быстро всасывается в желудочно-кишечном тракте. Он вызывает отток жидкостей из тканей в кровь, а затем усиливает выделение и формирование мочи в почках, ускоряет процесс перехода первичной мочи во вторичную, вывод её из организма. Благодаря диуретикоподобному действию хлористый аммоний способствует устранению отёков и нормализации водно-щелочного баланса.
Допустимые нормы потребления хлорида аммония
Предельно допустимая доза хлористого аммония в сутки составляет 12 г в сутки для взрослых людей и 2,5 г в день для детей. Вещество разрешено к применению во многих странах мира, в том числе в США, Канаде, России.
Применение хлорида аммония
Хлорид аммония используется во многих сферах. Сегодня его значение в некоторых областях несколько уменьшилось (сельское хозяйство, пищевая промышленность), поскольку его заменили более совершенные вещества.
Применение хлорида аммония в пищевой промышленности
Пищевая добавка Е510 действует как эмульгатор. Добавка позволяет смешивать исходно трудно растворимые друг в друге соединения, стабилизирует и улучшает их структуру. При производстве хлебобулочной продукции хлористый аммоний добавляется как улучшитель муки. Пищевую добавку Е510 можно встретить в составе и других продуктов:
Применение хлористого аммония в пищевой промышленности ограничивается, поскольку иногда он даёт неприятный вкус и запах. Ему предпочитают безвкусные стабилизаторы. Однако в лакричной карамели аммиачный привкус пищевой добавки Е510 ценится.
Применение хлорида аммония в медицине
Хлорид аммония выпускается в виде желатиновых капсул, а также дозированного порошка для приготовления растворов. Препараты на основе этого вещества назначаются при следующих патологических состояниях:
Благодаря мягкому мочегонному действию хлористый аммоний может назначаться как индивидуально, так и в составе комплексной терапии для усиления других диуретиков. Важно не превышать предельно допустимую дозировку и обязательно консультироваться о возможности приёма средства с врачом.
Применение хлорида аммония в сельском хозяйстве
Иногда хлористый аммоний может использоваться в качестве прикорневого удобрения сельскохозяйственных культур. Для этого необходим порошок, содержащий не менее 25% азота. Внесение в почву данного вещества улучшает рост и развитие растений, плодоношение, повышает их продуктивность. В качестве подкормки используют водный раствор.
Недостаток удобрения в том, что более 65% в составе занимает хлор. Этот элемент токсичен для многих видов растений. Поэтому хлорид аммония чаще всего используют для подкормки малочувствительных к хлору культур:
При применении данного удобрения нужно стараться вносить его при перекопке грунта осенью, тогда есть вероятность, что большинство хлора вымоется осадками. В связи с этими трудностями в использовании, хлористый аммоний чаще всего заменяют более безопасными для сельскохозяйственных растений азотными удобрениями.
Применение хлорида аммония в других сферах
При перепайке различных устройств хлорид аммония удаляет оксиды с поверхности металлов, что улучшает эффективность спаивания.
За счёт высокой способности к сольволизу водой нашатырь используется как источник электрического тока в гальванических элементах. Также может быть источником обильного дымообразования, что необходимо в пиротехнических составах.
В лабораториях хлористый аммоний используется для исследования состава крови. Соединение приводит к гемолизу эритроцитов, в результате чего их оболочка разрывается, и гемоглобин выходит наружу, становится доступным для изучения.
Хлорид аммоний раньше применялся в фотографии как компонент фиксирующей жидкости.
Где купить и сколько стоит хлорид аммония
Хлористый аммоний продаётся оптом заводами-производителями. Цена варьирует от 25 до 28 рублей за 1 кг. Удобрение на основе этого вещества продаётся в магазинах, ориентированных на товары для сада и огорода. Стоимость пакета, содержащего 500 грамм порошка, около 95-100 рублей. Хлорид аммония продаётся в аптеках, стоимость порошкообразного препарата от 95 до 200 рублей.
Заключение
Хлорид аммония – это неорганическое вещество, насыщенное азотом и хлором, которое издревле применяется в медицинских целях. Оно обладает мочегонным и отхаркивающим действием. Вещество используют как пищевую добавку Е510 для эмульгирования и стабилизации состава ряда продуктов. Хлористым аммонием можно удобрять почву, улучшая азотное питание растений. Он высоко химически активен, образует устойчивые водные растворы, способные проводить электричество, которые применяются также в промышленности, фотографии, пиротехнике.