лпонп и лпнп чем отличается
Хороший, плохой, злой холестерин
Хороший, плохой, злой холестерин
Нарушение жирового обмена является основным фактором развития атеросклероза и связанных с ним осложнений (ишемическая болезнь сердца, инфаркт, инсульт, облитерация сосудов нижних конечностей и пр.). При этом наиболее важным фактором повышенного риска атеросклероза является повышение содержания в крови атерогенных липопротеинов.
Автор
Редакторы
Статья на конкурс «био/мол/текст»: Вряд ли сейчас найдется человек, который не слышал, что высокий холестерин — это плохо. Однако столь же мала вероятность встретить человека, который знает, ПОЧЕМУ высокий холестерин — это плохо. И чем определяется высокий холестерин. И что такое высокий холестерин. И что такое холестерин вообще, зачем он нужен и откуда берется.
Конкурс «био/мол/текст»-2012
Эта статья представлена на конкурс научно-популярных работ «био/мол/текст»-2012 в номинации «Лучший обзор».
Спонсор конкурса — дальновидная компания Thermo Fisher Scientific.
Довольно подробно о роли холестерина в работе биомембран рассказывается в статье «Липидный фундамент жизни» [12]. — Ред.
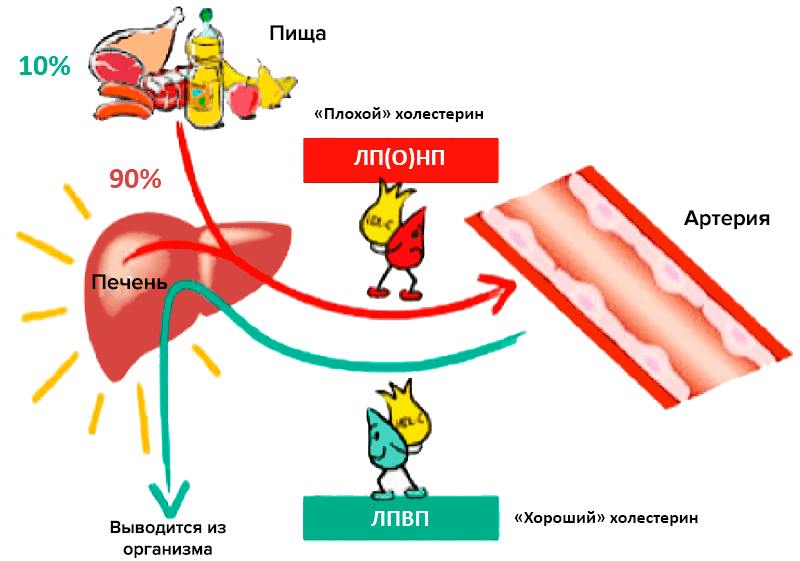
Главный липидный компонент пищевого жира и жировых отложений — это триглицериды, которые представляют собой эфиры глицерина и жирных кислот. Холестерин и триглицериды, будучи неполярными липидными веществами, транспортируются в плазме крови в составе липопротеиновых частиц. Частицы эти подразделяют по размеру, плотности, относительному содержанию холестерина, триглицеридов и белков на пять больших классов: хиломикроны, липопротеины очень низкой плотности (ЛПОНП), липопротеины промежуточной плотности (ЛППП), липопротеины низкой плотности (ЛПНП) и липопротеины высокой плотности (ЛПВП) [2]. Традиционно ЛПНП считается «плохим» холестерином, а ЛПВП — «хорошим» (рис. 1).
Рисунок 1. «Плохой» и «хороший» холестерины. Участие различных липопротеиновых частиц в транспорте липидов и холестерина.
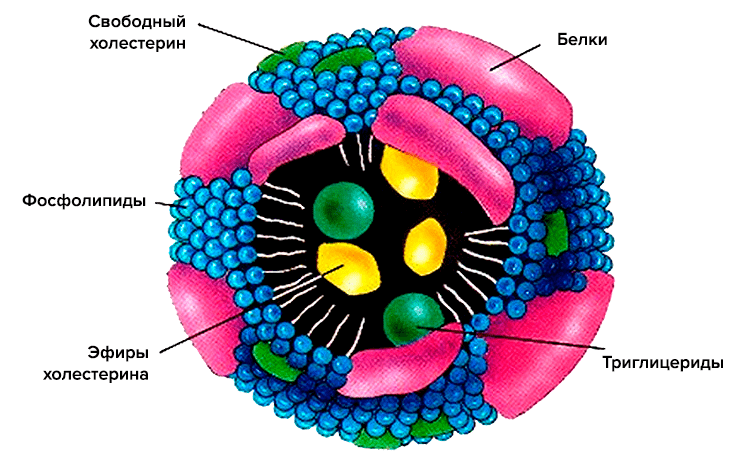
Схематично структура липопротеина включает неполярное ядро, состоящее по большей части из холестерина и триглицеридов, и оболочку из фосфолипидов и апопротеинов (рис. 2). Ядро — функциональный груз, который доставляется до места назначения. Оболочка же участвует в распознавании клеточными рецепторами липопротеиновых частиц, а также в обмене липидными частями между различными липопротеинами [3].
Рисунок 2. Схематическое строение липопротеиновой частицы
Баланс уровня холестерина в организме достигается следующими процессами: внутриклеточный синтез, захват из плазмы (главным образом из ЛПНП), выход из клетки в плазму (главным образом в составе ЛПВП). Предшественник синтеза стероидов — ацетил коэнзим А (CoA). Процесс синтеза включает, по крайней мере, 21 шаг, начиная с последовательного преобразования ацетоацетил CoA. Лимитирующая стадия синтеза холестерина в большой степени определяется количеством холестерина, абсорбируемого в кишечнике и транспортируемого в печень [4]. При недостатке холестерина происходит компенсаторное усиление его захвата и синтеза.
Транспорт холестерина
Систему транспорта липидов можно разделить на две большие части: внешнюю и внутреннюю.
Внешний путь начинается с всасывания в кишечнике холестерина и триглицеридов. Его конечный результат — доставка триглицеридов в жировую ткань и мышцы, а холестерина — в печень. В кишечнике пищевой холестерин и триглицериды связываются с апопротеинами и фосфолипидами, формируя хиломикроны, которые через лимфоток попадают в плазму, мышечную и жировую ткани. Здесь хиломикроны взаимодействуют с липопротеинлипазой — ферментом, который освобождает жирные кислоты. Эти жирные кислоты поступают в жировую и мышечную ткани для накопления и окисления соответственно. После изъятия триглицеридного ядра остаточные хиломикроны содержат большое количество холестерина и апопротеина Е. Апопротеин Е специфически связывается со своим рецептором в клетках печени, после чего остаточный хиломикрон захватывается и катаболизируется в лизосомах. В результате этого процесса освобождается холестерин, который затем преобразуется в желчные кислоты и выводится или участвует в формировании новых липопротеинов, образующихся в печени (ЛПОНП). При нормальных условиях хиломикроны находятся в плазме в течение 1–5 ч. после приема пищи [2], [3].
Внутренний путь. Печень постоянно синтезирует триглицериды, утилизируя свободные жирные кислоты и углеводы. В составе липидного ядра ЛПОНП они выходят в кровь. Внутриклеточный процесс формирования этих частиц схож с таковым для хиломикронов, за исключением различия в апопротеинах. Последующее взаимодействие ЛПОНП с липопротеинлипазой в тканевых капиллярах приводит к формированию остаточных ЛПОНП, богатых холестерином (ЛППП). Примерно половина этих частиц выводится из кровотока клетками печени в течение 2–6 ч. Остальные претерпевают модификацию с замещением оставшихся триглицеридов эфирами холестерина и освобождением от всех апопротеинов, за исключением апопротеина В. В результате формируются ЛПНП, которые содержат ¾ всего плазменного холестерина. Их главная функция — доставка холестерина в клетки надпочечников, скелетных мышц, лимфоцитов, гонад и почек [3]. Модифицированные ЛПНП (окисленные продукты, количество которых возрастает при повышенном содержании в организме активных форм кислорода, так называемом окислительном стрессе) могут распознаваться иммунной системой как нежелательные элементы. Тогда макрофаги их захватывают и выводят из организма в виде ЛПВП. При чрезмерно высоком уровне ЛПНП макрофаги становятся перегруженными липидными частицами и оседают в стенках артерий, образуя атеросклеротические бляшки.
Основные транспортные функции липопротеинов приведены в таблице.
| Класс | Размеры | Функция |
|---|---|---|
| ЛПВП | 4–14 нм | Транспорт холестерина от периферийных тканей к печени |
| ЛПНП | 20–22,5 нм | Транспорт холестерина, триглицеридов и фосфолипидов от печени к периферийным тканям |
| ЛППП | 25–35 нм | Транспорт холестерина, триглицеридов и фосфолипидов от печени к периферийным тканям |
| ЛПОНП | 30–80 нм | Транспорт холестерина, триглицеридов и фосфолипидов от печени к периферийным тканям |
| Хиломикроны | 75–1200 нм | Транспорт холестерина и жирных кислот, поступающих с пищей, из кишечника в периферические ткани и печень |
Регуляция уровня холестерина
Уровень холестерина в крови в большой степени определяется диетой. Пищевые волокна снижают уровень холестерина, а пища животного происхождения повышает его содержание в крови.
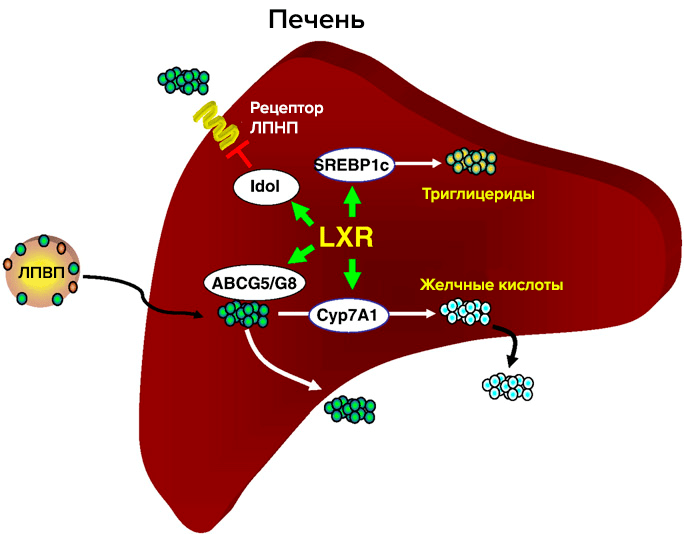
Один из основных регуляторов метаболизма холестерина — рецептор LXR (рис. 3). LXR α и β принадлежат к семейству ядерных рецепторов, которые образуют гетеродимеры с ретиноидным Х рецептором и активируют гены-мишени. Их естественные лиганды — оксистерины (окисленные производные холестерина). Обе изоформы идентичны на 80% по аминокислотной последовательности. LXR-α обнаружен в печени, кишечнике, почках, селезенке, жировой ткани; LXR-β в небольшом количестве обнаруживается повсеместно [6]. Метаболический путь оксистеринов быстрее, чем у холестерина, и поэтому их концентрация лучше отражает краткосрочный баланс холестерина в организме. Существует всего три источника оксистеринов: ферментативные реакции, неферментативное окисление холестерина и поступление с пищей. Неферментативные источники оксистеринов как правило минорные, но в патологических состояниях их вклад возрастает (окислительный стресс, атеросклероз), и оксистерины могут действовать наряду с другими продуктами перекисного окисления липидов [6]. Основное влияние LXR на метаболизм холестерина: обратный захват и транспорт в печень, вывод с желчью, снижение кишечного всасывания. Уровень продукции LXR различается на протяжении аорты; в дуге, зоне турбулентности, LXR в 5 раз меньше, чем в участках со стабильным течением. В здоровых артериях повышение экспрессии LXR в зоне сильного потока оказывает антиатерогенное действие [7].
Рисунок 3. Участие рецептора LXR в метаболизме холестерина в печени
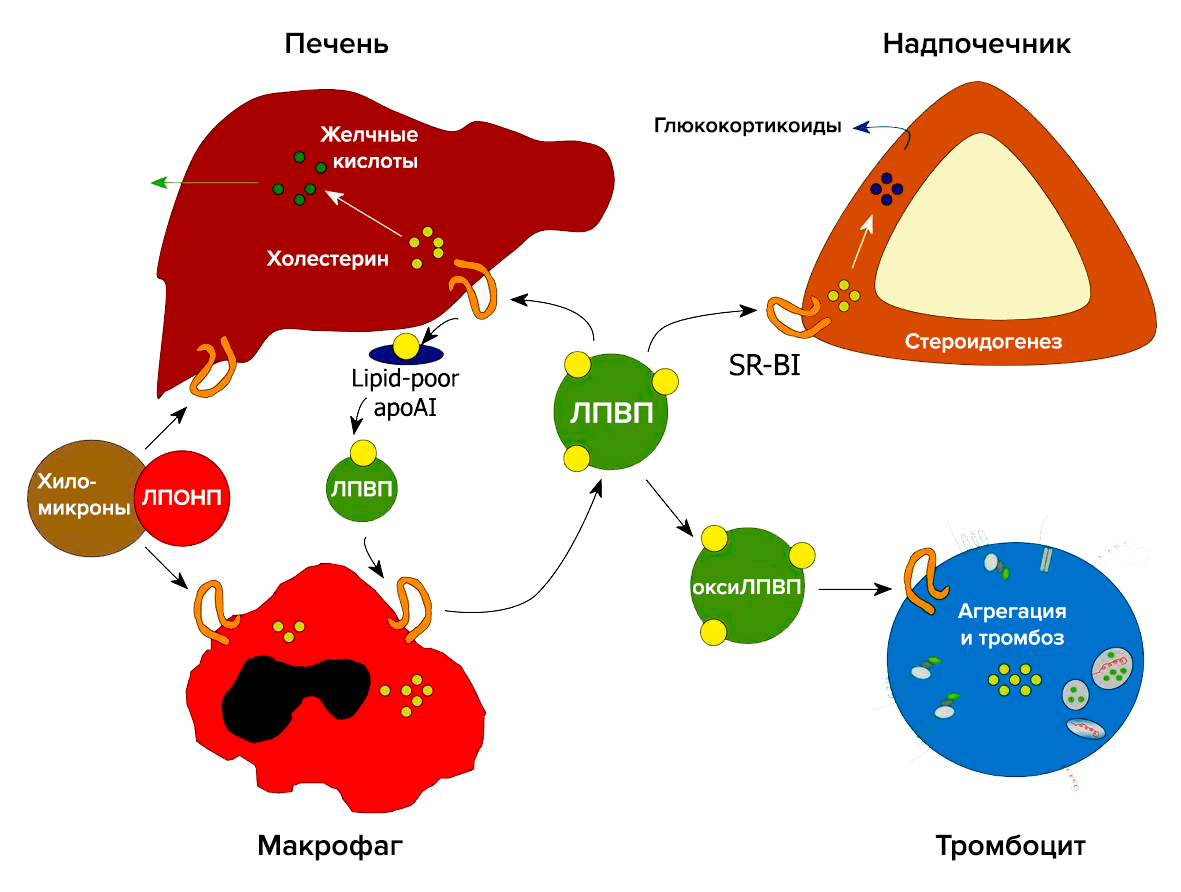
Важную роль в метаболизме холестерина и стероидов играет рецептор-«мусорщик» SR-BI (рис. 4). Он был обнаружен в 1996 году как рецептор для ЛПВП [8]. В печени SR-BI отвечает за избирательный захват холестерина из ЛПВП. В надпочечниках SR-BI опосредует избирательный захват этерифицированного холестерина из ЛПВП, который необходим для синтеза глюкокортикоидов. В макрофагах SR-BI связывает холестерин, что является первым этапом в обратном транспорте холестерина. SR-BI также захватывает холестерин из плазмы и опосредует его прямой выход в кишечник [9].
Рисунок 4. Участие рецептора SR-BI в метаболизме холестерина
Выведение холестерина из организма
Классический путь выведения холестерина: транспорт холестерина с периферии в печень (ЛПВП), захват клетками печени (SR-BI), экскреция в желчь и выведение через кишечник, где большая часть холестерина возвращается в кровь [10].
Основная функция ЛПВП — обратный транспорт холестерина в печень. Плазменные ЛПВП являются результатом комплекса различных метаболических событий. Состав ЛПВП очень различается по плотности, физико-химическим свойствам и биологической активности. Это сферические или дисковидные образования. Дисковидные ЛПВП в основном состоят из апопротеина A-I с вложенным слоем фосфолипидов и свободного холестерина. Сферические ЛПВП больше и дополнительно содержат гидрофобное ядро из эфиров холестерина и небольшого количества триглицеридов.
При метаболическом синдроме активируется обмен триглицеридов и эфиров холестерина между ЛПВП и триглицерид-богатыми липопротеинами. В результате содержание триглицеридов в ЛПВП повышается, а холестерина снижается (т.е. холестерин не выводится из организма) [11]. Отсутствие ЛПВП у людей встречается при болезни Tangier, главные клинические проявления которой — увеличенные оранжевые миндалины, роговичная дуга, инфильтрация костного мозга и мукозного слоя кишечника [3].
Восстановление этого баланса искусственным путем (например, на молекулярном уровне с использованием наночастиц) когда-нибудь станет основным способом лечения атеросклероза (см. «Наночастицами — по „плохому“ холестерину!» [13]). — Ред.
Все, что вы хотели знать о холестерине, но боялись спросить
Холестерин — жирообразное органическое вещество, входящее в состав клеточных мембран и необходимое для функционирования каждой клетки организма. Однако избыток холестерина в организме может быть опасен, так как считается одной из причин развития атеросклероза и сердечно-сосудистых заболеваний: ишемической болезни сердца, инфаркта, инсульта и т.д.
Большая часть необходимого для функционирования организма холестерина синтезируется в печени, но следует помнить о том, что он также поступает в организм с пищей. В сочетании с генетическими предрасположенностями и физиологическими особенностями организма избыточное употребление продуктов, богатых холестерином, приводит к повышению его уровня в крови и образованию излишков, которые оседают на стенках сосудов, формируя атеросклеротические бляшки. Эти образования сужают просвет сосуда и препятствуют нормальному кровотоку, затрудняя или вовсе перекрывая питание тканей и органов, и вызывают атеросклероз — причину большинства сердечно-сосудистых заболеваний, таких как инсульт и инфаркт миокарда, которые по статистке занимают лидирующее место среди причин смертности.
Наиболее богатыми холестерином являются насыщенные жиры (мясо, животный жир, яичный желток, молочные продукты) и трансжиры (образуются из нагретых растительных жиров, содержатся в большинстве готовых продуктов фабричного производства, маргаринах, выпечке, кондитерских изделиях и т. д.).
Чтобы знать свой уровень общего холестерина и контролировать его, можно сдавать анализ липидного профиля. Особенно важным является этот анализ для мужчин среднего возраста от 35 лет и пациентов, входящих в группу риска по атеросклерозу и сердечно-сосудистым заболеваниям.
Что включает в себя анализ липидного профиля
Общий холестерин — это общий уровень холестерина в крови.
ЛПНП — липопротеиды низкой плотности. Именно этот тип холестерина считается «вредным» из-за доказанной связи между высоким содержанием ЛПНП и развитием сердечно-сосудистых заболеваний. Главная цель при лечении в случае повышенного уровня холестерина состоит именно в снижении уровня ЛПНП.
ЛПВП — липопротеиды высокой плотности, иногда называют«полезным холестерином». Было установлено, что более высокий уровень ЛПВП снижает риск развития атеросклероза и сердечно-сосудистых заболеваний. ЛПВП помогают выводить часть холестерина из крови, возвращая его в печень. Следует стремиться к тому, чтобы уровень ЛПВП был выше 1,55 ммоль/л. Особенно это важно для пациентов, страдающих сердечно-сосудистыми заболеваниями.
Триглицериды — это частицы жира, уровень содержания которых в крови повышается при таких состояниях, как неконтролируемый диабет и ожирение.
Злоупотребление алкоголем и прием некоторых лекарственных препаратов также способны повысить уровень триглицеридов. Высокие уровни триглицеридов (свыше 1,7 ммоль/л) означают более высокий риск сердечно-сосудистых заболеваний.
Отношение общего холестерина к ЛПВП (коэффициент атерогенности, он же КА) — служит важным показателем риска развития сердечно-сосудистых заболеваний. В идеале этот показатель не должен превышать 3,5.
Как подготовиться к сдаче анализа на липидный профиль
Анализ на липидный профиль — один из вариантов биохимического анализа крови, однако для получения достоверного результата следует более тщательно подготовиться к этому тесту.
Для сдачи клинического анализа крови и оценки уровня общего холестерина достаточно не принимать пищу всего 3 часа, однако такие показатели, как ЛПВП, ЛПНП, триглицериды чувствительны к приему пищи, и для получения достоверного результата рекомендуется воздерживаться от еды в течение 10–12 часов непосредственно перед взятием крови. Также перед сдачей липидного профиля рекомендуют:
Кто входит в группу риска по атеросклерозу
Оценка результатов анализа
При выдаче результата анализа на бланке будет указано полученное значение, а также границы, к которым надо стремиться. Эти границы не средние для определенного пола и возраста интервалы, как обычно используют в референсных значениях. Врачи при ведении пациентов с рисками сердечно- сосудистых осложнений в первую очередь руководствуются не референсными значениями, а порогом принятия решений — целевыми значениями показателей липидного профиля, согласно Рекомендации третьего доклада экспертов NCEP ATP III (The National Cholesterol Education Program Adult Treatment Panel III). Эти цифры рассчитаны в соответствии с популяционными и клиническими критериями, подкреплены многочисленными статистическими данными и утверждены ВОЗ.
Критерии порога принятия решений являются очень важными диагностическими данными, исходя из которых врач, на ряду с результатами анализов пациента и полагаясь на свой опыт, знания и специальные методики расчетов риска, может определить наиболее вероятный прогноз и подобрать лечение для конкретного пациента.
Наиболее известной методикой, помогающей врачу определить степень риска для пациента, является так называемая шкала SCORE — Systematic COronary Risk Evaluation, позволяющая рассчитать риск смерти от сердечно-сосудистых заболеваний в зависимости от уровня холестерина и артериального давления пациента.
Пороги принятия решений
Для общего холестерина, по данным экспертов NCEP ATP III (The National Cholesterol Education Program Adult Treatment Panel III), оптимальное значение должно быть ниже 5,2 ммоль/л. Это усредненная верхняя граница, к которой надо стремиться. Значения в диапазоне 5,2–6,1 ммоль/л считаются пограничными. При значениях выше 6,1 ммоль/л можно говорить о серьезных рисках развития атеросклероза.
Для ЛПНП оптимальное значение составляет не более 2,6 ммоль/л. Пограничными считаются значения от 2,6 до 3,3 ммоль/л. Выше 3,3 ммоль/л — риск развития атеросклероза.
Значение уровня ЛПВП в норме должно быть не менее 1,03 ммоль/л для пациентов с низким риском развития атеросклероза. Для пациентов группы риска, а также для пациентов, уже страдающих атеросклерозом, целевой показатель выше — более 1,55 ммоль/л.
Для триглицеридов нормой считается значение до 1,7 ммоль/л. От 1,7 до 2,2 ммоль/л — пограничное значение, выше 2,2 ммоль/л — опасно повышенное, связанное с риском развития атеросклероза. Однако следует помнить, что само по себе повышение триглицеридов может и не быть признаком атеросклероза или нарушения липидного обмена. Так, это может быть связано с тем, что пациент неправильно подготовился к сдаче анализа (не выдержал 10–12-часового голодного перерыва) или иными патологическими процессами.
Важным показателем риска развития атеросклероза является коэффициент атерогенности (КА).
Формула его расчета следующая:
Нормальный уровень КА для молодых людей 20–30 лет составляет до 2,7.
Для лиц старше 30 лет значение может составлять до 3–3,5.
Показатель КА 4 и выше — признак начавшегося атеросклероза и риска развития сердечно-сосудистых заболеваний. В этом случае врач обычно назначает медикаментозную терапию, снижающую уровень холестерина.
Как можно улучшить свой липидный профиль
Изменение питания:
Другие изменения в образе жизни:
Лекарственные препараты для регулирования холестерина
Лекарственные препараты назначают пациентам, у которых изменения в рационе
и в образе жизни не вызвали улучшения в уровне холестерина. Их также
принимают пациенты с сердечно-сосудистыми заболеваниями или те, у кого высок риск такого заболевания. Ваш лечащий врач может определить, нуждаетесь ли Вы в приеме лекарственных препаратов, отпускаемых по рецепту.
Холестерин. Все о норме и патологии.
Холестерин — это жироподобное вещество, которое нам необходимо для:
Где берется холестерин?
Источниками холестерина являются частично продукты, которые мы потребляем (около 20% от всего количества холестерина в организме). Но основной процент вещества синтезируется в печени, которая ответственна за выработку 80% эндогенного холестерина. Другими участками синтеза, но в значительно меньшей степени являются кора надпочечников, яичек, яичников и кишечник.
Печень синтезирует холестерин для экспорта в другие клетки, и также способствует удалению избыточного холестерина из организма. Это достигается путем преобразования холестерина в соли желчи и переноса в желчь, из которой он в конечном итоге и выводится. Кроме того, печень синтезирует большинство необходимых липопротеинов, необходимых для транспортировки холестерина по всему организму. Так как холестерин переносится через кровь, но имея жироподобную структуру не растворяется в ней, а присоединяется к белкам, которые действуют как его носители. Комбинация белков и холестерина называется липопротеидами.
Липопротеиды высокой (ЛПВП) и низкой (ЛПНП) плотности или «плохой» и «хороший холестерин»
Существуют несколько важных типов липопротеидов, ответственных за перемещение холестерина. Основные это:
Часто, когда говорят о высоком уровне холестерина, имеют в виду повышенный уровень холестерина липопротеидов низкой и очень низкой плотности ЛПНП (ЛПНП-Х). Когда уровень ЛПНП увеличивается, повышается риск сердечно-сосудистых заболеваний.
Холестерин липропотеидов низкой плотности (ЛПНП) или «плохой холестерин»
Холестерин липопротеидов высокой плотности (ЛПВП) или хороший холестерин
Холестерин липопротеидов очень низкой плотности (пре-бета липротеиды), триглицериды
Контроль над уровнем “плохого” холестерина является важной частью снижения риска развития сердечных заболеваний, сердечного приступа или инсульта.
При повышении уровня холестерина могут развиваться жировые отложения в кровеносных сосудах. Со временем эти отложения растут, что затрудняет прохождение достаточного количества крови через артерии. Иногда эти отложения могут внезапно отделиться и образовывать сгусток, который вызывает сердечный приступ или инсульт перемещаясь с кровотоком к сердцу или мозгу.
Наследственность или высокий холестерин по наследству
Высокий уровень холестерина часто может передаваться по наследству и диагностироваться только при сдаче лабораторных анализов по причине возникновения сердечного приступа или инсульта. Немедленно сообщите своему врачу, если у кого-то из членов вашей семьи были такие заболевания особенно в молодом возрасте и подумайте о сдаче анализов.
Семейная гиперхолестеринемия является наследственным заболеванием, которое вызывает атипично высокие уровни холестерина липопротеинов низкой плотности (ЛПНП-Х). При этом заболевании печень не в состоянии утилизировать естественный запас холестерина, который постоянно вырабатывается. В результате холестерин становится опасно переизбыточным, что резко увеличивает риск отложений атеросклеротических бляшек и развития у человека ишемической болезни сердца (недостатка кислорода, поступающего к сердцу из-за сужения сосудов). Представьте себе неисправную утилизацию мусора через мусоропровод. Каждую ночь вам нужно выбросить новый мусор и испорченную пищу, но предыдущие отходы уже забили трубы. Как вы уже догадались, это скоро приведет к катастрофе. Если ваша печень не фильтрует и не перерабатывает холестерин ЛПНП должным образом, это мало чем отличается от неправильной утилизации мусора. Сосуды наиболее страдают из-за отложений бляшек холестерина они сужаются и имеют меньшую эластичность.
Симптомы высокого холестерина
Иногда холестерин откладывается и на поверхности кожных покров (в виде бляшек на коже лица, нижних веках, конечностях и туловище, но наиболее опасные отложения холестерина внутри нашего организма, которые не видны. Часто высокий уровень холестерина низкой плотности в организме не имеет симптомов. И в большинстве случаев заболевание остается вовремя не выявленным, что может привести к сердечному приступу, инфаркту миокарда, инсульту в раннем возрасте, а также проблемам с атеросклерозом.
Анализ крови на холестерин
Раннее выявление повышенного холестерина имеет решающее значение
Обычные тесты липидной панели могут также вовремя обнаружить повышенные уровни холестерина низкой плотности и высокого уровня триглицеридов. Тем самым предупредив риск сердечных и других заболеваний, так как своевременная диета, регулярные физические упражнения, а когда нужно и лекарства могут помочь вовремя снизить уровень холестерина.
Анализы на холестерин и липидный профиль
Вы можете сдать эти основные показатели в отдельности или заказать более обширный анализ липидного профиля по программе 112 липидный комплекс или 113 липидный комплекс расширенный которые включают дополнительно исследования
Норма холестерина в крови
Когда рекомендуют сдавать анализы на холестерин?
Молодые люди без факторов риска сердечно-сосудистых заболеваний обычно проходят тестирование один раз в возрасте от 17 до 19 лет. Повторное тестирование для взрослых без факторов риска для сердечных заболеваний обычно проводится каждые пять лет.
Американская кардиологическая ассоциация рекомендует проводить тестирование холестерина каждые 4 – 6 лет для людей в возрасте 20 лет и старше.
Пациенты принимающие лекарства при повышенном уровне холестерина, например статины, должны проверять уровень холестерина по рекомендации врача или через 4 – 12 недель после первой дозы, а затем каждые 3 –12 месяцев после этого.
Рекомендуется исследовать уровень холестерина не реже одного раза в пять лет, если у человека общий холестерин составляет 5,2 ммоль или есть предпосылки для развития сердечно-сосудистых заболеваний и инсульта. Дополнительные причины возможного развития сердечных заболеваний включают сахарный диабет, высокое кровяное давление или использование антигипертензивных препаратов), низкий уровень ЛПВП, семейный анамнез ишемической болезни сердца (ИБС) и гиперхолестеринемию, а также курение сигарет.
Факторы риска наличия повышенного холестерина включают в себя:
Осложнения высокого уровня холестерина
Профилактика
Чтобы помочь предотвратить высокий уровень холестерина, вы можете:
Пониженный уровень холестерина
Пониженный — это так же проблема. Так как холестерин является важным компонентом клеточных мембран, предшественником гормонов, желчных кислот и других компонентов, имеющих важное значение в живом организме, уменьшение его количества имеет негативные последствия
Внешние симптомы гипохолестеринемии могут проявляться по-разному у каждого человека, но лабораторная диагностика помогает узнать их причину