молекулярная вода что это
Какое строение имеет молекула воды
Вода является источником жизни для всех живых организмов.
Молекула воды имеет уникальное строение. В ней удивительным образом сочетаются прочность и устойчивость кристаллической структуры (льда), и подвижность жидкого вещества.
В статье мы подробно рассмотрим особенности строения молекулы воды в различных агрегатных состояниях: жидком, твердом, газообразном.
Какое строение имеет молекула воды
Долгое время химики считали воду простым соединением, не вступающим в сложные реакции.
Состав воды как сложного вещества был установлен Лавуазье в 1783 г.
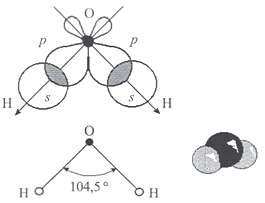
Одна молекула воды состоит из трех атомов: двух атомов водорода и одного атома кислорода, которые соединены между собой ковалентной связью. Химическая формула: H₂O
Характерные свойства ковалентной связи — направленность, насыщаемость, полярность, поляризуемость. Они определяют химические и физические свойства соединений.

По форме молекула воды напоминает равнобедренный треугольник, в основании которого находятся два атома водорода. Связь между атомом кислорода и атомами водорода полярная, т.к. кислород притягивает электроны сильнее, чем водород.
Межъядерные расстояния О—Н близки к 0,1 нм, расстояние между ядрами атомов водорода равно 0,15 нм, угол между связями Н—О—Н равен 104,5°.
Молекула воды имеет два положительных и два отрицательных полюса и поэтому в большинстве случаев ведёт себя как диполь (т.е. на одной стороне – положительный заряд, на другой – отрицательный)
Значения эффективных зарядов на атомах составляет ±0,17 от заряда электрона.
Водородная связь
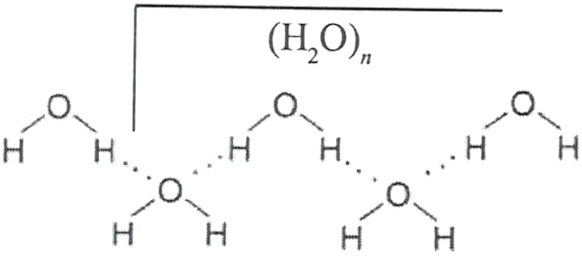
В жидкой воде происходит ассоциация молекул, т. е. соединение их в более сложные агрегаты за счёт особой химической связи, которая называется водородной.
Особенностями водородной связи, по которым её выделяют в отдельный вид, является её не очень высокая прочность.
Водородная связь также играет важную роль в процессах растворения, поскольку растворимость зависит и от способности соединения давать водородные связи с растворителем. В результате содержащие ОН-группы такие вещества, как сахар, глюкоза, спирты, карбоновые кислоты, как правило, хорошо растворимы в воде.

Димер — это две молекулы Н2О, соединенные водородной связью. Связь между молекулами воды водородная.
Каждая молекула способна образовать четыре водородные связи: две между неподеленными электронными парами её атома кислорода и атомами водорода соседних молекул и ещё две – между атомами водорода и атомами кислорода двух других молекул.
Энергия водородной связи может изменяться от 17 до 33 кДж/моль.
Строение молекулы в различных агрегатных состояниях
Вода может быть в нескольких состояниях:
Существуют также и переходные состояния жидкости, которые возникают при замерзании или испарении.
Примечательно, что различные формы воды могут одновременно находиться рядом и даже взаимодействовать, например реки с ледниками, айсберги с морской водой, облака на небе с водяным паром.
Строение молекулы воды, водородная связь способствует расположению молекул воды. Рассмотрим особенности каждого агрегатного состояния по отдельности.
Представляет собой твердое состояние воды.
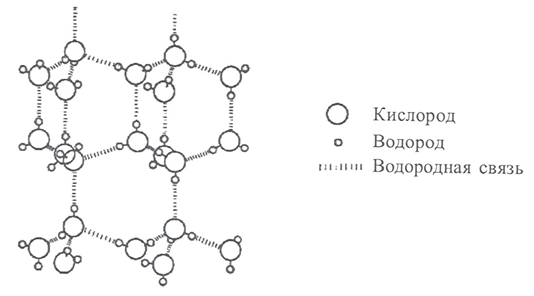
Молекулы воды образуют слои, причём каждая молекула связана с тремя молекулами в своём слое и с одной молекулой соседнего слоя. Расстояние между атомами кислорода ближайших молекул равно 0,276 нм.
Атом кислорода связан с четырьмя атомами водорода: с двумя, расположенными на расстоянии 0,096 — 0,102 нм посредством валентных связей, и с двумя другими, находящимися на расстоянии 0,174 — 0,180 нм посредством водородных связей.
Жидкая вода
В отличие от структуры льда структура жидкой воды исследована ещё недостаточно.
Предполагается, что жидкая вода по своему строению представляет нечто среднее между кристаллами льда и паром.
В результате изучения молекулы воды с помощью инфракрасных и рентгеновых лучей было видно, что при температуре близкой к точке замерзания, молекулы жидкой воды собираются в небольшие группы, практически так, как в кристаллах.
При температуре близкой к точке кипения они располагаются более свободно.
Водяной пар
Это газообразное агрегатное состояние воды.
При данном состоянии молекула воды не имеет структуры и состоит преимущественно из мономерных молекул воды, которые находятся на расстояние относительно друг друга.
Из чего состоит вода
При обычных условиях вода выглядит как прозрачная жидкость. У нее отсутствуют вкус и запах. При небольшой толщине слоя не наблюдается даже цвета.
Вода является отличным растворителем. В природе в ней постоянно находятся растворенные газы и соли. При соединении атомов кислорода с водородом получается молекула воды. Поскольку более сильными являются водородные соединения, то, когда происходит их разрыв, они прикрепляются к иным веществам, помогая тем растворяться.
Из-за своего малого размера каждую молекулу растворенного вещества окружают очень много молекул воды. Благодаря этому в ней присутствуют отрицательные и положительные ионы.
Чистая вода является еще и хорошим изолятором с концентрацией протонов и гидроксильных ионов в количестве 10-7 моль/л, это позволяет ей проводить электричество. Именно по ее электропроводности можно оценивать чистоту жидкости.
При взаимодействии с другими веществами состав воды не изменяется, что играет особую роль в жизни любого живого организма. Ведь очень важно, чтобы жидкостные растворы, через которые в организм поступают полезные вещества, не изменялись.
Кроме того, вода хорошо поглощает инфракрасное и микроволновое излучение, а также способна хранить в себе память о веществах, которые были в ней растворены.
Элементы
Проходя гидрологический цикл: испарение, конденсацию и выпадение в виде осадков вода может дополняться разными химическими элементами, которые можно разделить на 6 категорий. Рассмотрим информацию в таблице № 1.
Таблица № 1 «Элементы, которые могут входить в состав воды».
| Ионы | Na, K, Mg, Ca, анионы: Cl, HCO3 и SO4. Эти компоненты находятся в воде в наибольшем, по сравнению с другими, количестве. |
| Растворенные газы | Кислород, азот, сероводород, углекислый газ и прочие. Количество каждого газа в воде напрямую зависит от ее температуры. |
| Биогенные элементы | Главными из них являются фосфор и азот, которые поступают в жидкость из осадков |
| Микроэлементы | Их насчитывается около 30 видов: бром, селен, медь, цинк и т. д. Показатели их в составе воды очень малы и колеблются от 0,1 до микрограмма на 1 литр. |
| Органические вещества | Спирты, углеводы, альдегиды, фенолы, пептиды и прочее. |
| Токсины | Тяжелые металлы и продукты нефтепереработки. |
В настоящий момент доступны специальные методы очистки, которые эффективно борются с вредными химическими соединениями.
Вода также может содержать в себе магний и катионы кальция. В зависимости от этого ее подразделяют на мягкую и жесткую.
По изотопам водорода в молекуле воды можно говорить о легкой воде, тяжелой и сверхтяжелой воде.
Подводим итоги
Вода необходима для жизни всего живого на Земле. Она участвует в мировом круговороте воды в природе. Благодаря испарению с поверхности водоемов, почвы, растений образуются облака. Затем они выпадают в виде дождя, снега, града, питая собой подземные воды и родники. Родниковые воды по рекам попадает в море.
Таким образом, количество воды на Земле не изменяется, она только меняет свои формы — это и есть круговорот воды в природе.
Уникальное строение молекулы воды помогает ей трансформироваться в три агрегатных состояния.
При замерзании воды ее молекулы собираются в небольшие группы. При испарении находится на расстоянии относительно друг друга. Жидкая вода по своему строению представляет нечто среднее между кристаллами льда и паром.
Структурированная вода
Структурированная вода несет в себе биологическую активность за счёт особой молекулярной структуры. Чем стабильнее сформирована молекулярная структура, тем полезнее и эффективней будет её потребление.
Молекулы воды способны соединяться между собой благодаря положительно заряженным атомам водорода, которые притягиваются к отрицательно заряженному кислороду, такая молекулярная связь называется водородная.
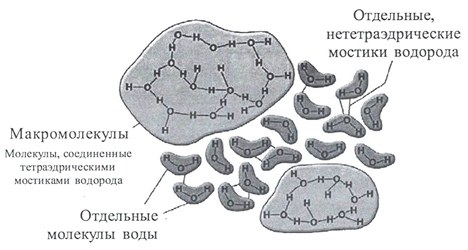
Водородная связь образует как случайные соединения(ассоциаты), не имеющие упорядоченной структуры, так и кластеры, в которых ассоциаты имеют определенную структуру. По прочности водородная связь примерно в 15 — 20 раз слабее ковалентной связи. Поэтому ассоциаты молекул воды не стабильны и коротко живущие, они постоянно разделяются и образуютновые соединения. Считается, что из-за таких свойств, вода является самым универсальным растворителем.
Интересным фактом является то, что отдельные молекулы воды, не связанные в ассоциаты, присутствуют в самой структуре воды лишь в виде 1%. В основном вода – это совокупность беспорядочных ассоциатов и кластеров «водяных кристаллов», где количество связанных молекул может достигать сотен и даже тысяч единиц.
Кластеры воды имеют стабильную структуру подобно клеточной воде
Под кластером обычно понимают группу атомов или молекул, объединенных физическим взаимодействием в единое целое, но сохраняющих внутри него индивидуальное поведение. Их жизнь быстротечна, и потому они с трудом поддаются изучению. Уникальность воды заключается в том, что она представляет собой сложную и динамически меняющуюся структуру кластеров и ассоциатов.
Кластеры – это группы молекул, объединенные водородными связями, которые имеют стабильную структуру. Группируясь, молекулы воды создают различные пространственные и плоскостные структуры. Базовой структурой кластера считается группа из шести молекул, объединенных в кольцо. Такой тип структуры имеют лёд, снег, талая вода, и клеточная вода всех живых тканей.
К примеру, в обычной воде кластеры состоят из макромолекулярных групп, образованных из 15-17 молекул и более сотен молекул. Такая вода менее подвижна, плохо растворяет химические вещества, плохо проникает через мембрану клеток, что ухудшает клеточный метаболизм (обмен веществ) и приводит к дополнительным энергозатратам, т.к. каждый организм структурирует воду под себя.
Изменения структуры воды в природе
Вода самое аномальное из всех известных в природе веществ. Её структура легко может изменяться под внешним воздействием: при помощи давления, температуры, магнитного поля, электрического поля и т. д.
При изменении температуры структура воды меняет свое состояние: Пар, жидкость, лед.
Объяснение такого изменения в том, что молекулы воды совершают колебания с определенной частотой. При нагреве воды до 100 градусов, амплитуда колебания молекул становится такой силы, что притяжение молекул воды друг к другу становится не в состоянии удерживать их вместе, в результате структура кластера распадается. При охлаждении амплитуда колебаний уменьшается, и структура становится более прочной.
Газообразное состояние. При температуре выше +100°С вода преобразуется в газообразное состояние. В газообразном состоянии водородная связь между молекулами воды почти полностью отсутствует. На этом примере мы можем увидеть, как легко разрываются водородные связи между молекулами превращаясь в пар.
Твердое состояние. При температуре ниже 0 вода переходит в твердое состояние «Лед». В твердом состоянии водородные связи молекул воды образуют крепкую, непрерывную кристаллическую сетку, в которой каждая молекула имеет четырёх ближайших соседей, которые соединены между собой прямыми одинаковыми водородными связями в сетчатый каркас с пустотами в нем. Это объясняет почему плотность льда меньше плотности воды.
Этим можно объяснить полезность воды из горных источников. Она зарождается у кромки таяния снега и льда, то имеет специфическую структуру, где связи между молекулами упорядочены, а молекулы объединены в кластеры.
Роль структурированной воды в организме человека
Человек состоит на большую часть из воды, поэтому вода является самым важным элементом в организме. Подробнее о клеточной воде и ее функциях.
Благодаря такой структуре, вода обладает хорошей проникающей способностью в клетки, быстро циркулирует и способствует нормальному протеканию всех биохимических реакций, что существенно повышает эффективность и синхронность работы всех систем организма.
При потреблении обычных водопроводных или газированных вод либо напитков, где структура воды всегда разрушена и состоит из макромолекулярных кластеров, организм структурирует воду по типу своей внутренней структуры, затрачивая при этом клеточную энергию. Именно затрата жизненной энергии на структурирование воды является главной причиной «синдрома хронической усталости». Поэтому потребление структурированной воды легко усваивается организмом и не требует энергетических затрат.
Чем полезна структурированная вода
Структурированная вода, имеющая структуру близкую к внутренней жидкости организма легко усваивается организмом, не тратиться дополнительная клеточная энергия на преобразование в низкомолекулярную. Биологическое действие на организм связано с тем, что каналы мембран клеток имеют регулярную структуру схожую со структурой преобразованной воды, в результате молекулы структурированной воды пропускаются с повышенной скоростью. Кстати, таким же эффектом объясняется польза от потребления различных фруктов и овощей в связи с тем, что, межклеточная жидкость растений, имеет аналогичную структуру.
Вывод: Клеточная вода любого живого организма имеет упорядоченную структуру (структурированная), а употребление структурированной воды не требует затрат дополнительной энергии на ее преобразование. Высвободившийся энергетический потенциал организм использует на собственное восстановление, тем самым укрепляется иммунитет, регенерация тканей. Существенно повышается порог интеллектуальных и стрессовых перегрузок.
Вода с «живой» структурой без труда проникает через мембраны клеток, где приносит каждой клетке витамины и питательные вещества, вымывает токсины и шлаки из организма, а также усиливает действие натуральных лекарственных препаратов.
Как обычно структурируют воду в домашних условиях
Вода структурируется, а точнее обретает особую регулярную структуру при воздействии некоторых факторов, от которых зависят способы ее приготовления и жизненный цикл регулярной структуры. Например,
Полученная структурированная вода становиться активной и несет полезные свойства для всего организма.
Молекулярная вода что это
Вода- удивительное вещество. Являясь окисью водорода, H2О также является сложным устойчивым вобычных условиях химическим соединением 11,19% водорода и88,81% кислорода.
«Воде была дана волшебная власть стать соком жизни наЗемле»,- cлова величайшего гения вистории человечества Леонардо ДаВинчи. Вполне допустимо, чтопроисхождение воды неразрывно связано смногочисленными теориями окосмическом происхождении Земли. Самое известное предположение: протоны, пришедшие вверхнюю атмосферу отСолнца, «захватывают» электроны, превращаются ватомы водорода, которые, всвою очередь соединяются сатомами кислорода иобразуют H2O.
При изучении молекулярного строения воды стало известно, чтокислород иводород имеют изотопы (разновидности атомов иядер одного химического элемента сразным количеством нейтронов). Зная обизотопах кислорода иводорода, можно составить несколько видов молекулы H2O сразличными относительными молекулярными массами. Кислород имеет шесть изотопов: 14 O, 15 O, 16 O, 17 O, 18 O, 19 O, изкоторых стабильны только три, аводород три: 1 H (протий), 2 H (дейтерий), 3H (тритий).
На сегодняшний день можно говорить о135 различных видах воды. Однако только девять изних являются устойчивыми исоотношение стабильных изотопов вних имеет вид: 1 H2 16 O
0,04 %. Другие изотопы присутствуют вничтожном количестве.
Проблема оценки структуры воды пока остается одной изсамых сложных, поэтому существует несколько гипотез оее структуре. Наиболее признанными являются только две: первая- основной строительной единицей воды является двойная молекула воды (H2O)2- дигидроль; вторая- лед, вода иводяной парсостоят измолекул H2O, объединенных вгруппы спомощью водородных связей, которые возникают врезультате взаимодействия атомов водорода одной молекулы сатомом кислорода соседней молекулы.
Следует отметить, чтопо сравнению сдругими трехатомными соединениями водорода, вода имеет аномально высокие температуры кипения изамерзания. Также онаспособна кполимеризации- соединению большого числа молекул воды вкластеры. Такая вода имеет рядсовершенно новых физических свойств, вчастности онакипит притемпературе в5-6 более высокой, чемобычная.
Между гранями элементов кластеров действуют дальние кулоновские силы притяжения, чтопозволяет рассматривать структурированное состояние воды ввиде особой информационной матрицы. Молекулы воды втаких образованиях могут взаимодействовать между собой попринципу зарядовой комплементарности, засчет которой осуществляется построение структурных элементов воды вячейки, называемые клатратами.
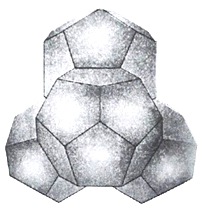
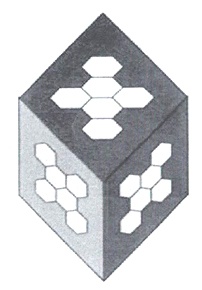
На молекулярном уровне вода представляет собой иерархию правильных объемных структур, воснове которых лежат кристаллоподобные образования, состоящие из57 молекул ивзаимодействующие друг сдругом засчет свободных водородных связей. Взаимодействие этих образований приводит кпоявлению структур второго порядка ввиде шестигранников, состоящих из912 молекул воды. Взависимости оттого, вкаком соотношении выступают наповерхность кислород иводород, зависят свойства кластеров. Конфигурация элементов воды реагирует налюбое внешнее воздействие ипримеси.
Многие верят, чтов ближайшем будущем освойствах иструктуре воды станет известно намного больше, ивлияние наних даже такого неоднозначного фактора, какинформация, будет иметь научное объяснение.
Вода | Строение молекулы и структура воды в жидком, твердом и газообразном виде.
Содержание:
1. Современные представления о составе и структуре воды. Строение молекулы воды. Легкая и тяжелая вода.
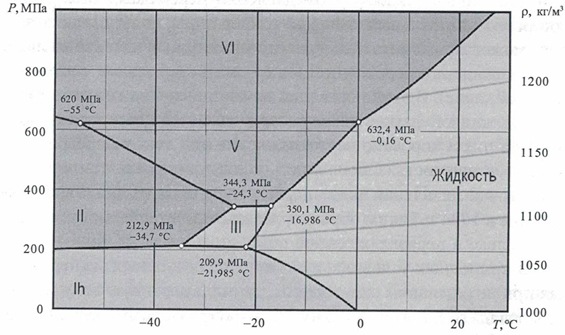
В «тройной» точке на диаграмме может одновременно существовать вода во всех трех агрегатных состояниях.
В «критической» точке все свойства жидкости и пара (энергия, плотность, структура, характер движения частиц и т.п.) становятся равны. При более высоком давлении и/или температуре агрегатное состояние воды называют «сверхкритическим».
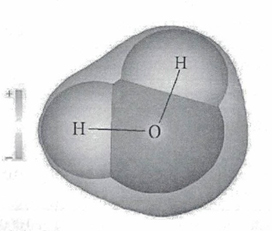
В стабильном энергетическом состоянии молекула воды имеет тетраэдрическую пространственную структуру. При изменении агрегатного состояния воды длина сторон и угол между ними меняются. Если бы мы увидели молекулу воды, то обнаружили, что она имеет сфероидальную форму с двумя выпуклостями (рисунок 3).
Наличие неподеленных пар электронов у кислорода и смещение обобществленных электронных пар обуславливает возникновение водородных связей, что способствует ассоциации молекул воды в группы.
Обладая значительным дипольным моментом, молекулы воды также сильно взаимодействуют с полярными молекулами других веществ.
Идеально чистую воду практически невозможно получить. По факту, мы всегда будем иметь дело хоть и с очень разбавленными, но растворами.
В природе на 1 000 000 молекул воды в среднем приходится:
— 997 284 молекул легкой воды 1 H2 16 O;
— 311 молекул 1 HD 16 O;
— 390 молекул 1 H2 17 O;
— 2005 молекул 1 H2 18 O.
Если из глубинной океанической воды, отвечающей стандарту SMOW (Standard Mean Ocean Water) удалить все тяжелые изотопы и заменить их на 1 H2 16 O, то масса 1 л такой воды станет меньше на 250 мг, т.е. на четверть.
2. Структура воды. Водородные связи.
В ходе современных физико-химических исследований были выявлены характерные структурные агрегаты воды, формирующиеся с помощью водородных связей.
Для формирования трехмерных структур необходимо, кроме способности молекул создавать водородные связи, выполнение еще двух условий. Этих связей должно быть не менее четырех на одну молекулу и геометрические размеры молекулы не должны противоречить оптимальным направлениям водородных связей. Вода удовлетворяет этим требованиям. Так, нагревая лед мы получаем смесь жидкой воды и кристаллов льда, температура которой останется неизменной до тех пор, пока все кристаллики не расплавятся. Это говорит о том, что подводимое нами тепло будет расходоваться в первую очередь на разрушение водородных связей льда.
3. Структура воды в жидком виде.
Жидкость, как известно, отличается от других агрегатных состояний вещества своей текучестью, т.е. способностью неограниченно менять форму под действием касательных механических напряжений, сохраняя при этом объем. Жидкость способна течь даже под свей неподвижной поверхностью. Молекулы жидкости не имеют своего строго определенного места, но, все же, им недоступна полная свобода перемещения, как в паре.
Структура жидкости есть статистическая закономерность межмолекулярных расстояний и ориентаций, характерных для плотно упакованных систем.
Согласно одной из первых моделей воды Бернала и Фаулера, основанной на рентгеноструктурном анализе, существует три формы расположения молекул в жидкой воде:
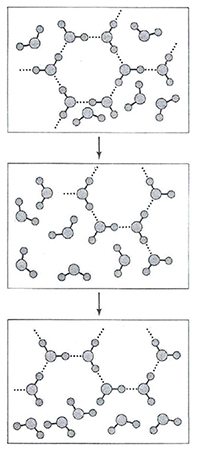
В 1951 г. Дж. Попл предложил модель воды в виде непрерывной сетки (рисунок 5), отличной от модели Бернала и Фаулера. Отличия заключались в том, что сетка была случайной, связи в ней искривлены и имеют различную длину.
Попл объяснял уплотнение воды при плавлении искривлением связей. Однако, данная модель не могла объяснить нелинейность зависимости свойств воды от температуры и давления.
Почти одновременно с идеей Попла возникли кластерные и клатратные модели, которые можно обозначить как «смешанные».
Кластерная модель представляла жидкую воду как кластеры из молекул, связанных водородными связями, плавающих в объеме свободных молекул. В группе кластерных моделей выделяется теория Г.Немети и Х.Шераги (рисунок 6). Отметим, что в данной модели разрушение одной водородной связи приводит к разрушению всего кластера. Разрушение и образование кластеров происходит постоянно.
Кластерная модель не говорит о расположении молекул в гроздьях, но авторы предполагают наличие отдельных «роев». При этом постулируется тот факт, что большинство молекул должно быть тетракоординировано. Состояние молекул будет определяться количеством водородных связей, которые она образует (0-5).
Удар по кластерной теории наносят исследования Г.Стэнли на основе теории перколяции (протекания). Г.Стэнли доказывает невозможность существования в воде изолированных кластеров.
Клатратная модель говорила о воде как о непрерывной сетке-каркасе связанных молекул, внутри которого содержались пустоты со свободными молекулами.
Первую модель клатратного типа предложил О.Я.Самойлов в 1946 году. В ее основе лежало представление о жидкой воде как о испорченной, размытой структуре льда Ih с частичным заполнением полостей мономерами. В процессе движения молекул решетка постоянно перестраивается. Настройкой свойств и концентраций микрофаз, а также параметрами пустот легко можно было объяснить все закономерности свойств воды.
Пустоты в воде по результатам моделирования имеют тенденцию объединяться друг с другом, образуя еще более крупные пустоты, как показано на рисунке 7.
Рассмотрим кластерную и клатратную модели строения жидкой воды подробнее.
3.1 Кластерная модель строения жидкой воды.
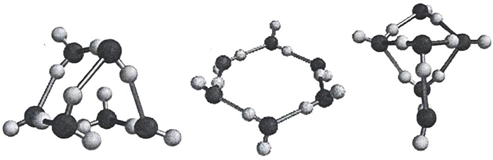
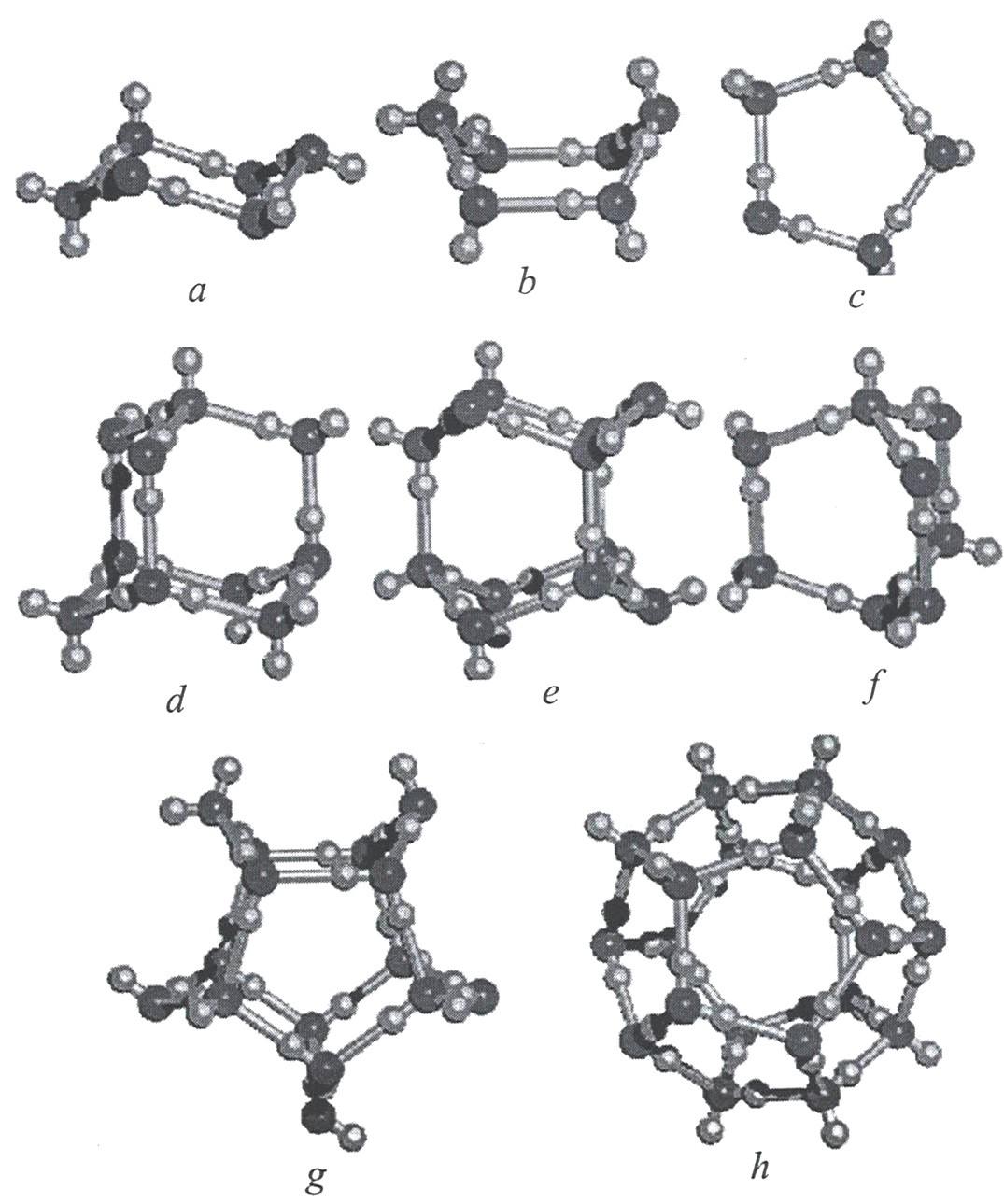
Согласно квантово-химическим расчетам большей устойчивостью обладают линейного «открытого» димера воды, по сравнению с циклическими формами. В случае цикла выгодными являются трех-четырех- и пятичленные образования, в которых водородные связи имеют одинаковое направление. Для шестичленного цикла выгодным становится структура типа «кресло».
Одно из первых изображений формирования циклических кластеров воды приведено на рисунке 9.
Большой вклад в возможность формирования и устойчивость кластеров воды во времени внесли работы Г.А.Домрачева и Д.А. Селивановского. Они доказывали существование механохимических реакций радикальной диссоциации воды. Доказательство основывалось на том, что вода, по их мнению, представляет собой динамически нестабильную полимероподобную систему и по аналогии с механохимическими реакциями в полимерах при механическом воздействии на воду поглощенная водой энергия используется для разрыва химических связей H-OH. Реакция разрыва связи может выглядеть так:
Рассчитав эффективность механодиссоциации воды, авторы пришли к выводу, что кислород на Земле появился при диссоциации воды.
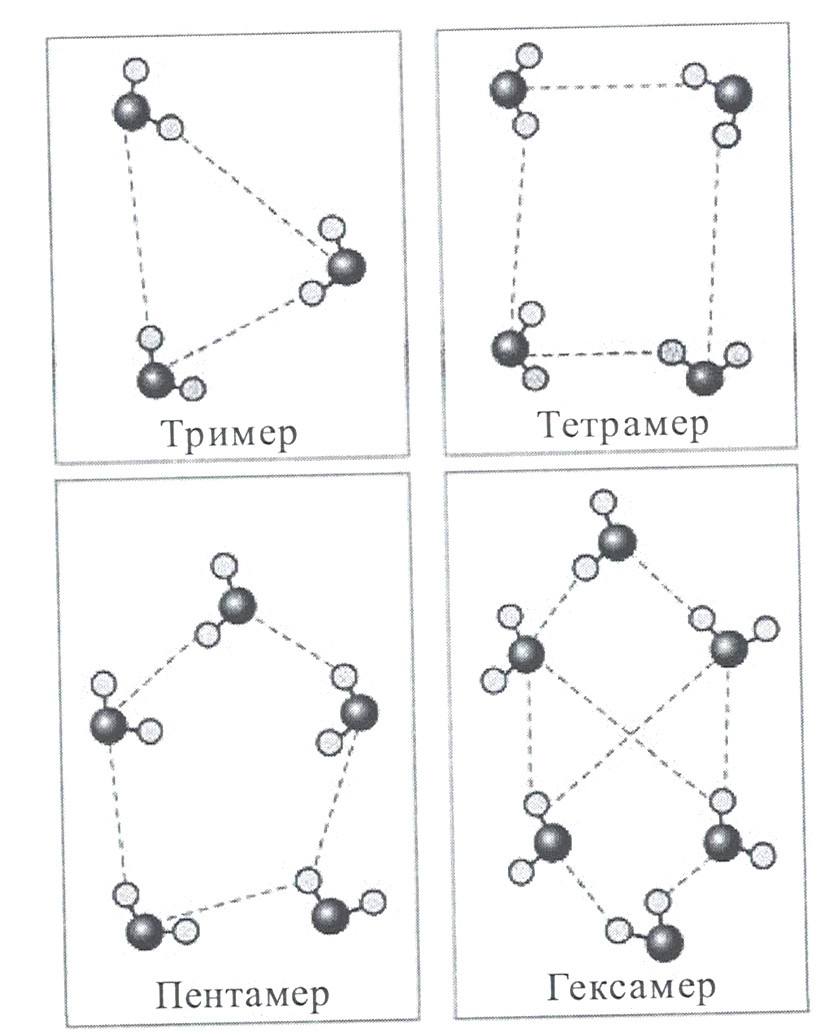
В 1993 г. К.Джордан предложил свои варианты устойчивых «ассоциатов воды», которые состоят из 6 молекул (рисунок 10).
По Джордану кластеры могут объединяться и друг с другом, и со свободными молекулами воды за счет водородных связей, формируя более крупные ассоциаты. Такие кластеры могут объединяться как друг с другом, так и со свободными молекулами воды.
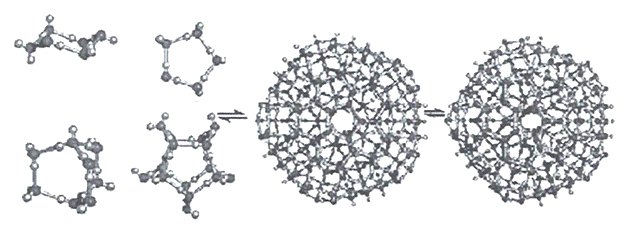
Квантово-химические расчеты нанокластеров с общей формулой (H2O)n с n=6-20 показали, что самые устойчивые структуры образуются посредством взаимодействия тетрамерных и пентамерных кольцевых структур (рисунок 11). На рисунке ниже показаны возможные структуры конформации кластеров воды.
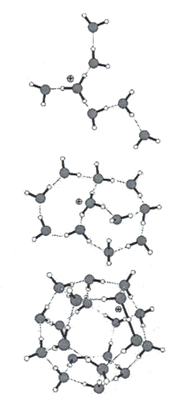
Оригинальной кластерной моделью является теория С.В.Зенина. Согласно модели С.В.Зенина вода представляет собой иерархию геометрически правильных объемных структур «ассоциато». Согласно его теории элементарной структурной ячейкой воды являются тетраэдры, в которых может содержаться 4 (простой тетраэдр) или 5 (объемно-центрированный тетраэдр) молекул воды. При этом у каждой молекулы воды в простых тетраэдрах сохраняется способность образовывать водородные связи, благодаря чему создаются более сложные структуры, как показано на рисунке 13.
Кластеры, содержащие 20 молекул воды (додэкаэдры) более стабильны. Схема их образования показана на рисунке 14.
Из 57 молекул такого образования 17 составляют гидрофобный каркас с полностью насыщенными связями, а по 10 молекул на поверхности каждого додекаэдра формируют центры образования водородных связей.
Методами жидкостной хроматографии было подтверждено существование пяти- и шестиквантовых структур типа «четырехконечной звезды» и «шестилучевой снежинки».
На уровне 24 центров связывание по водородным связям практически прекращается ввиду того, что поверхность образований становится насыщенной (нейтральной).
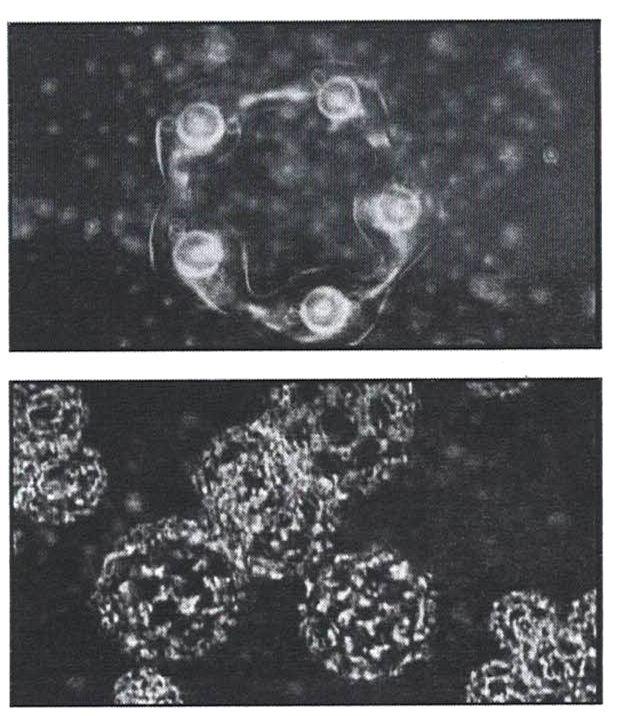
Кластеры почти не взаимодействуют между собой, а скользят друг по другу, поэтому вода не отличается высокой вязкостью. В таком «режиме» из кластеров формируются метастабильные структуры, пример которых показан на рисунке 17 (микроизображение в режиме фазового контраста).
Теория Зенина хорошо объясняет электропроводные свойства воды, уменьшение плотности при плавлении, но плохо согласуется с большими значениями коэффициента самодиффузии и малым временем диэлектрической релаксации.
Однако практически существование регулярных матриц в воде маловероятно. Кластеры из 280 молекул также могут формировать цепочки, но с более напряженными водородными связями.
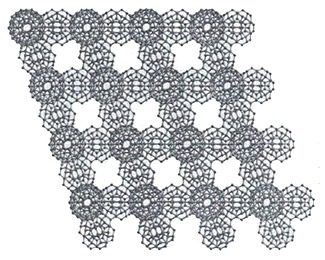
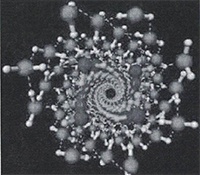
Кластеры могут разрастаться в суперкластеры (гигантские икосаэдры), примеры которых приведены на рисунке 19.
В 2002 Беркли методом рентгеноструктурного анализа показала, что молекулы воды действительно способны образовывать структуры, представляющие собой топологические цепочки и кольца из множества молекул.
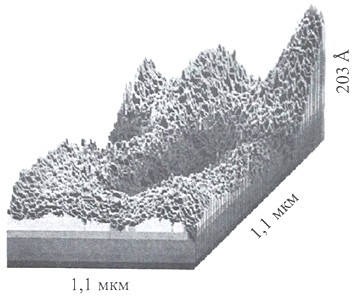
А.Н.Смирновым в бидистиллированной воде и некоторых растворах методами акустической эмиссии, лазерной интерферометрии и термического анализа удалось визуализировать надмолекулярные образования с размерами частиц от 1 до 100 мкм, распределенных в водной среде (рисунок 20). Свойства таких частиц были сходны со свойствами частиц, образующих эмульсию, поэтому они были названы «эмулонами».
Размеры и пространственная организация эмулонов зависят от состава водного раствора, температуры и предыстории раствора. Наибольшее число фракций имеют размеры 30, 70 и 100 мкм.
Температурная динамика структуры эмулонов имеет следующие отсечки:
3.2 Клатратная модель строения жидкой воды.
Клатраты в целом (не только вода) делятся на два класса, зависящие от соединения-хозяина. Молекулярные клатраты образуются «хозяевами», имеющими внутримолекуярные полости. Такие клатраты могут существовать как в растворе, так и в кристаллическом состоянии. Если «хозяин» способен образовывать только межмолекулярные или кристаллические полости, то из него получаются решетчатые клатраты (рисунок 21), устойчивые лишь в твердом состоянии.
В поздних модификациях клатратной модели воды допускается образование водородных связей между молекулами в каркасе и молекулами в пустотах. При этом сами молекулы в обеих микрофазах соединены водородными связями.
В заключение отметим, что существует целый ряд воздействий, которые могут приводить к определенному структурированию воды:
Более подробно структурирование воды под воздействием внешних сил будет рассмотрено в отдельной статье.
4. Особенности строения воды в твердом виде. Лед.
• Всего насчитывается около 15 структурных модификаций льда (рисунок 22).
1922 г. У.Г.Брэгг в статье «Кристаллическая структура льда» пытается выяснить причины возможных ошибок при расшифровке положений ядер кислорода. Он убежден, что ни Джон, ни Деннисон не смогли найти истинного расположения ядер кислорода в структуре льда. Брэгг сделал важное замечание: каждый атом кислорода в структуре льда должен быть окружен четырьмя другими. Атом же водорода располагается между двумя кислородами как бусинки на нитке. При этом, что важно, бусинки сдвинуты, смещены, относительно центра льда. Т.е. ядра водорода расположены асимметрично.
Кристаллическая решетка льда называется ажурной (рисунок 23). Паутина связей между молекулами воды во льду содержит много крупных пустот, больших по размеру, чем сами молекулы. Именно поэтому лед более легкий, чем жидкая вода. При плавлении льда водородные связи начинают разрушаться и в пустотах оставшихся ассоциатов поместиться освободившиеся молекулы воды.
• При давлении в 2 ГПа можно получить лед со структурой VI (горячий лед), который не будет плавиться даже при 80 о С.
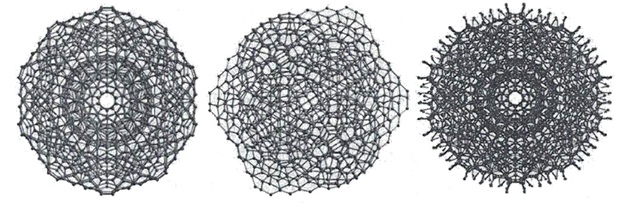
• При очень высоких давлениях внутри нанотрубок с диаметром от 1,35 до 1,90 нм вода может кристаллизоваться в форме двойных спиралей (рисунок 24).
• Современные представления о структуре льда говорят о наличии кластерного строения. Чем ниже температура, тем крупнее кластеры. Наиболее устойчивы кластеры из 8, 12, 24, 36 молекул.
5. Особенности строения воды в газообразном виде. Пар.
В паре водородные связи на 99% разорваны. При этом в нем сохраняется до 1% димеров. Полностью разорвать все связи в паре можно лишь при температура 600 о С.
Расстояние между молекулами во много раз больше самих молекул. При этом сами молекулы хаотично двигаются, сталкиваются со стенками сосуда, в котором заключены, и между собой. Скорость их тем выше, чем выше температура системы.
Вода может длительное время находиться и в перегретом состоянии до 200 о С. При введении пузырька воздуха в такую перегретую воду она мгновенно вскипает и ее температура падает до 100 о С.