vbinder что это вирус
Что такое Win32: Binder-DL?
Win32: Связующее-DL это тип вредоносного ПО, позволяющего хакеру получить контроль над зараженным компьютером. После того, как Win32: Binder-DL берет под свой контроль вашу систему, он может выполнять множество автоматических задач, которые могут отображать странные сообщения, замедлять работу вашей системы или даже приводить к сбою. С помощью Win32: Binder-DL хакер может украсть вашу конфиденциальную информацию, рассылая спам, отказываясь от определенных услуг в Интернете и даже совершая «мошенничество с кликами».
Win32: Binder-DL обычно создается не для того, чтобы взломать один компьютер, а для заражения миллионов устройств. Бот-пастухи часто используют Win32: Binder-DL на компьютерах через вирус-троян. Стратегия обычно требует, чтобы пользователи заражали свои собственные системы, открывая вложения электронной почты, нажимая на вредоносные всплывающие окна или загружая опасное программное обеспечение с веб-сайта. После того, как устройства заражены, Win32: Binder-DL может свободно получать доступ и изменять личную информацию, атаковать другие компьютеры и совершать другие преступления.
Более сложный Win32: Binder-DL может даже распространять, находить и автоматически заражать устройства. Эти автономные роботы выполняют задачи поиска и заражения и постоянно ищут в Интернете уязвимые устройства, подключенные к Интернету, без обновления операционной системы или антивирусного программного обеспечения.
Win32: Binder-DL трудно обнаружить. Он потребляет мало вычислительной мощности, чтобы не мешать нормальным функциям устройства и предупреждать пользователя. Более продвинутый Win32: Binder-DL даже предназначен для обновления их поведения, чтобы предотвратить их обнаружение программным обеспечением для кибербезопасности. Пользователи не знают, что подключенное устройство контролируется злоумышленниками. Что еще хуже, дизайн Win32: Binder-DL постоянно развивается, что затрудняет поиск новых версий.
Win32: Binder-DL требует времени для роста. Многие из них будут спать на устройствах, ожидая, когда бот-мастер попросит их принять меры в случае атаки DDoS или распространения спама.
Win32: Binder-DL Подробности
Что такое боты?
Боты (сокращение от роботов) также известны как пауки, сканеры и веб-роботы. Хотя они могут использоваться для повторяющихся задач, таких как индексация поисковой системы, они часто представляют собой вредоносные программы. Вредоносное ПО используется для получения полного контроля над компьютером.
Вредоносные роботы определяются как вредоносные программы собственного производства, которые заражают свой хост и повторно подключаются к одному или нескольким центральным серверам. Сервер служит «центром управления» для ботнета или сети уязвимых компьютеров и подобных устройств. Вредоносные роботы обладают «способностью распространяться как черви», а также могут:
Боты обычно используются для заражения большого количества компьютеров. Эти компьютеры образуют «ботнет» или сеть ботов.
Как Win32: Binder-DL попал на мой компьютер?
Как и другие вредоносные программы, боты часто случайно загружаются на компьютер по электронной почте, фишинговые сообщения, в которых просят получателя нажать на ссылку, или сообщения в социальных сетях, которые пытаются заставить вас загрузить изображение или перейти по ссылке.
Передовые вредоносные программы обычно достигают компьютера или сети через следующие каналы распространения:
Симптомы Win32: Binder-DL?
Основными симптомами заражения Win32: Binder-DL являются:
Как удалить Win32: Binder-DL с вашего компьютера?
Если вы подозреваете инфекцию, предпримите следующие шаги, чтобы выяснить, что происходит:
Используйте диспетчер задач Windows или, вернее, Sysinternal Process Explorer, чтобы искать приложения, которые, кажется, не принадлежат или, кажется, потребляют большое количество системных ресурсов. Скорее всего, вы не найдете бота напрямую таким образом, но информация, которую ваша система предоставляет вам, может помочь вам двигаться в правильном направлении.
Как исправить и удалить Win32: Binder-DL
Вы можете скачать этот инструмент с официальной страницы загрузки. Установка довольно обычная и простая. После установки вам нужно будет запустить его. Инструмент автоматически анализирует ваш компьютер и отображает ошибки, вирусы, вредоносное ПО и соответствующие проблемы, которые необходимо исправить. Полный анализ занимает немного больше времени, но обеспечивает полный охват и безопасность. Результаты анализа очень подробны, и вы можете определить, какая часть вашего компьютера замедляется.
Вот области или вещи, которые диагностируются во время процесса:
После просмотра результатов анализа настало время приступить к устранению неполадок. Все, что вам нужно сделать, это нажать на кнопку «Начать восстановление», и ваша работа завершена. Reimage исправляет проблемы, возникающие с назначающими врачами, а также выполняет еще один углубленный анализ для решения других проблем.
Заключение
Убедитесь, что ваша система всегда обновлена и что ваша антивирусная программа работает, чтобы предоставить вам, вашей семье и друзьям дополнительную защиту.
Неприятно познакомиться: как появились вирусы и почему в России их меньше, чем в Китае
В любой энциклопедии написано: «вирус» в переводе с латинского языка означает « яд». С тех пор как в XIX веке исследователи впервые столкнулись с заражением одного организма другим, знания о вирусах множились. К настоящему времени ученые изучили порядка пяти тысяч видов вирусов, но сказать, что науке доподлинно известно и с чем она имеет дело, нельзя. В двадцать первом веке все еще остаются вопросы, на которые у ученых-вирусологов нет ответов. Ведь количество неизученных вирусов, которые «свободно парят» вокруг нас, находятся в воде, земле, в организмах животных, в стеблях растений, исчисляется миллионами!
— За всю историю исследований в основном изучались вирусы человека и сельскохозяйственных животных, — поясняет «Вечерке» вирусолог, директор Института медицинской паразитологии, тропических и трансмиссивных заболеваний им. Е. И. Марциновского Сеченовского университета Александр Лукашев. — А вирусы есть у каждого вида живых существ на Земле, в том числе у грибов, мхов, бактерий, простейших. И многие могут перейти к человеку.
Когда и при каких условиях тому или иному вирусу приспичит активизироваться — вопрос, не поддающийся прогнозам. Точнее, «паразиты» бомбардируют все живое постоянно. Вирусная атака — это процесс в природе непрекращающийся. Ведь вирус не бактерия и не микроорганизм. Это фрагмент генетической информации, упакованный в белковую оболочку. У него нет клетки, а значит, вне живого организма он как бы не живет, а находится в замершем состоянии. Поэтому если вы спросите у специалиста, живые вирусы или нет, он ответит уклончиво: как бы нет, но в общем-то да. Делиться самостоятельно вирус не может, и чужая клетка нужна ему, чтобы жить.
— Любая живая информация старается выжить в биосфере, — говорит вирусолог Александр Лукашев. — Главная эволюционная задача вируса — не уничтожить живую клетку, а, используя ее ресурсы, размножиться как можно в большем количестве своих копий. У вируса нет задачи быть «плохим». Наоборот, «хороший» вирус имеет преимущества. Например, вирус герпеса большинству людей практически не наносит вреда. Им заражены все, он распространен повсеместно, и свою функцию — максимально размножиться — он выполняет. А, скажем, вирус Эболы убивает примерно половину своих жертв, и в том числе и поэтому он не может размножиться в популяции человека. С точки зрения эволюции убивать своего носителя вирусу невыгодно. Клеткам живых организмов приходится держать глухую оборону практически постоянно. Но человек и не знает, что находится под обстрелом фрагментов генетической информации, потому что в подавляющем большинстве случаев клетки самостоятельно разбираются с захватчиком, не допуская заражения. Только с воздухом мы вдыхаем едва ли не ежесекундно десятки вирусов, и ничего.
— Вирусы редко переходят между видами нечасто, — говорит вирусолог Александр Лукашев. — Скажем, вирусы от растений к животным переходят, наверное, раз в один миллион лет. Бомбардировка новых видов происходит постоянно, но чаще всего безуспешно. Легче перейти к близкому виду. Например, от приматов к человеку вирусы переходят много раз в год. От млекопитающих — примерно раз в 10 лет. Ту же Эболу человек подхватывает от летучих лисиц. И вспомним свиной грипп и другие «болячки», перешедшие от животных. Случаи могут регистрироваться, например, и два года подряд, а потом 20 лет будет затишье, но я говорю о средней периодичности. Но на каждый успешный переход приходится, условно, миллион безуспешных.
— Скученность населения и, скажем так, очень близкий контакт между людьми и животными — в Китае совпали все условия. Из-за особенностей пищевых рынков и, возможно, более высокой восприимчивости населения «чужой» вирус «зацепился», а дальше из-за высокой плотности китайского населения смог распространиться, — рассуждает вирусолог Александр Лукашев. — У нас в стране совсем другие условия, хотя известно, что зараженные примерно такими же опасными вирусами летучие мыши обитают на юге России. Кроме того, мы летучих мышей и панголинов не едим, не разделываем и на рынках не продаем, а значит, и попыток перейти от животного к человеку их вирус может предпринимать значительно меньше. Гипотетически же к человеку может перейти огромное число вирусов — умножьте число всех видов млекопитающих на 1000 и примерно узнаете, сколько. Но если нет условий, выгодных для распространения заразы, бояться нечего.
Вместе с тем наука признала, что вирусы — это наследие древнего мира, существовавшего до появления первой живой клетки, четыре миллиарда лет назад. Более того, из вирусов или их остатков по большей части состоит геном человека. Это значит, что они были основой развития жизни на Земле. Доказано, что человек, как млекопитающее, обязан существованием именно им, поскольку благодаря вирусам у наших предков начала формироваться плацента. Как? Они привнесли в человеческий геном белок, отвечающий за ее функцию. Кроме того, вирусы сильно повысили эффективность эволюции. Они переносили генетическую информацию намного эффективнее, чем это делалось только в ходе естественного размножения. То есть удачные гены они передавали не потомству вида, а сразу в новый организм.
Вирусы мутируют. Ученые говорят, что у многих из них каждый новый геном имеет дополнительную мутацию. Изменяется вирус иногда в течение нескольких часов. Внутри одной клетки, внутри одного цикла размножения одинаковых вирусов нет! Чтобы иметь возможность приспособиться к новым условиям, вирус меняется, производя в популяции самые разные варианты. Мутация для вирусов — обязательная часть их жизненного цикла. Собственный геном вирусов в миллион раз меньше человеческого, и чтобы с нами конкурировать, они мутируют, создавая множество вариантов, которые могут «пригодиться» в разных условиях.
Паниковать не стоит, но лечиться надо. Что мы знаем о вирусе Эпштейна-Барр?
От него не скроешься. Рано или поздно с ним встречается каждый человек. Надо ли его бояться? А может, инфекция совсем безобидна? Паниковать не стоит, но и легкомысленное отношение – ошибка.
О вирусе Эпштейна-Барр рассказала врач-инфекционист «Клиники Эксперт» Тула Елена Геннадьевна Королёва.
— Елена Геннадьевна, что такое вирус Эпштейна-Барр?
— Среди герпес-вирусов насчитывают 8 типов, вызывающих патологии у вида Homo sapiens, то есть у людей. Вирус Эпштейна-Барр – герпес-вирус IV типа. После заражения вирусом Эпштейна-Барр инфекция остаётся в организме навсегда и никогда его не покидает.
Вирус Эпштейна-Барр – один из самых распространённых герпес-вирусов у людей. Восприимчивость к нему человека высока. Многие дети инфицируются до достижения годовалого возраста, а к 40-50 годам инфекция есть в организме практически у каждого.
— Как происходит заражение вирусом Эпштейна-Барр?
— Источник инфекции – вирусоносители, а также больные с типичными (манифестными) и стёртыми формами заболевания. Наиболее распространённый путь передачи – воздушно-капельный: с частицами слюны при разговоре, чихании, кашле. Возможна передача вируса при поцелуе (именно поэтому в некоторых источниках вызванный им инфекционный мононуклеоз называют «болезнью поцелуев»). Возможен и контактный путь заражения (например, через предметы домашнего обихода).
Вирус Эпштейна-Барр проникает в организм через верхние дыхательные пути, и уже оттуда распространяется в лимфоидную ткань, вызывая поражения лимфоузлов, миндалин, селезёнки и печени.
При размножении в организме вирус Эпштейна-Барр воздействует на иммунную систему. Механизм воздействия сложен, но в конечном результате за счёт поражения В-лимфоцитов и угнетения Т-клеточного иммунитета происходит подавление выработки интерферона – белка, отвечающего за противовирусную защиту организма.
В современном мире у детей отмечается всплеск заболеваемости, особенно в городах. Наиболее высока вероятность заразиться в местах скопления людей.
— А бессимптомный носитель может быть опасен?
— Чаще всего источником инфекции становится человек в острой стадии болезни. Но передача от бессимптомного носителя не исключена.
— Какую болезнь вызывает вирус Эпштейна-Барр?
— Классическое проявление – инфекционный мононуклеоз. Для него характерны общие интоксикационные симптомы: высокая температура тела, сонливость, вялость, головные боли, боль в горле, увеличение лимфоузлов (или лимфопролиферативный синдром).
Лимфопролиферативный синдром сочетает:
В общем анализе крови определяется наличие атипичных мононуклеаров. Что это такое? Атипичные мононуклеары (другое их название – «вироциты») – это изменённые одноядерные клетки крови. При течении инфекционного мононуклеоза количество атипичных мононуклеаров в крови повышается значительно (больше 10 %). Может снижаться общее количество тромбоцитов и лейкоцитов, что говорит о тяжести переносимой инфекции.
Есть особенности проявления вируса Эпштейна-Барр у детей. Инфицированные попадают в такую категорию, как «часто болеющие дети». Из-за ослабления иммунитета регулярно возникают заболевания ЛОР-органов, трудности при выздоровлении (подкашливание, постоянно красное горло), бывает храп (из-за разрастания миндалин). При таком течении к взрослому возрасту иммунитет учится противостоять инфекции, взрослые болеют уже не так часто. Показания к оперативному удалению аденоидов у детей практически всегда связаны с непролеченным вирусом Эпштейна-Барр. И это очень печально: ничего лишнего в организме нет, а при своевременном лечении удаления можно было бы избежать.
Читайте материалы по теме:
Знать, что ребёнок инфицирован, важно и по другой причине. Вирус Эпштейна-Барр может изменить реакцию на некоторые антибиотики, спровоцировать токсикоаллергическую реакцию. Поэтому следует обязательно своевременно выявлять вирус и сообщать о нём лечащим врачам, они будут подбирать антибиотики с учётом этого факта.
Тяжёлые последствия возникают, если первичное заражение происходит у женщины в период беременности. Вирус Эпштейна-Барр преодолевает плацентарный барьер, это грозит гибелью плода или значительными дефектами развития.
«После первичного инфицирования некоторые из этих инфекций организм не покидают. Они «спят» в определенных клетках, если с иммунной системой все в порядке и она хорошо контролирует их «сон». Цитата из материала «Чем опасны ТОРЧ-инфекции»
— Есть мнение, что вирус Эпштейна-Барр вызывает гепатит и даже лимфому. Это правда?
— Герпетические вирусы кровотоком разносятся по всему организму, поражают все группы лимфатических узлов. И печень, и селезёнка при остром течении мононуклеоза увеличены. При этом течение болезни обычно благоприятное, здоровье печени полностью восстанавливается.
Утверждать, что вирус Эпштейна-Барр непременно приводит к лимфоме, нельзя. Обнаружить вирус недостаточно: если инфицировано практически всё население планеты, естественно, анализы обнаружат наличие вируса в организме, но ведь лимфомой заболевает далеко не каждый. Конечно, хроническое подавление иммунной системы может приводить к разным нарушениям, в том числе к онкологическим заболеваниям. Но достоверной связи нет. А скомпенсировать иммунные нарушения современная медицина в силах.
Паниковать точно не стоит. Но и надеяться на самостоятельное излечение не надо. Когда ребёнок постоянно болеет, родители зачастую впадают в отчаяние. И хотя избавиться от герпес-вирусов навсегда невозможно, вполне можно облегчить состояние и в разы уменьшить частоту заболеваний. Лечиться можно и нужно.
Подробнее о гепатитах читайте в наших статьях:
— Какими методами можно проверить, присутствует ли в организме вирус Эпштейна-Барр? Какие анализы его выявляют?
— В нашем арсенале два метода: иммуноферментный анализ (ИФА) и полимеразная цепная реакция (ПЦР). Преимущество метода ПЦР – возможность определить ДНК вируса в слюне, соскобе из носоглотки. Благодаря этому можно не брать кровь и не нервировать ребёнка. Но если нет обострения, такой анализ может дать ложноотрицательный результат. Это значит, что вирус в организме есть, но он «спит», и, соответственно, в мазке из носоглотки может отсутствовать. А поскольку с помощью ПЦР ищут сам вирус, точнее, его нуклеиновые кислоты (ДНК), то и анализ будет отрицательным. Нередки также искажения из-за того, что мазок взят неправильно.
Метод ИФА точнее, он в любом случае покажет и наличие инфекции, и выраженность инфекционного процесса. Выводы в данном случае делают по присутствию в крови специфических иммуноглобулинов (антител) к вирусу. Например, если обнаружены иммуноглобулины класса М (IgM), можно говорить об острой фазе инфекции (первичном заражении либо реактивации вируса, когда-то попавшего в организм). Если найдена определённая фракция иммуноглобулина класса G (IgG), это свидетельствует, что организм в прошлом уже сталкивался с инфекцией. Поэтому для определения диагностического метода нужна консультация врача.
— Какими методами лечения вируса Эпштейна-Барр располагает современная медицина?
— Это сложная задача. Если для герпес-вирусов I и II типа (вирусов простого герпеса) есть специфические противовирусные средства, то для вируса Эпштейна-Барр и цитомегаловируса специфической терапии пока не разработали. При лёгком течении болезнь может пройти сама, но при тяжёлом течении с поражением костного мозга медицинская помощь необходима. Лечение направлено на стимуляцию иммунитета, применяются интерфероны. Схему лечения выбирают, исходя из множества факторов, определять её должен только врач.
После излечения вирус продолжает жить в организме. Периодически могут возникать обострения: из-за переохлаждения, длительного пребывания под солнцем, стресса и т. д. Проявления инфекции – всегда повод идти к врачу.
Беседовала Дарья Ушкова
Редакция рекомендует:
Для справки:
Королёва Елена Геннадьевна
VirTool:Win32/Vbinder
What is VirTool:Win32/Vbinder infection?
In this article you will locate concerning the interpretation of VirTool:Win32/Vbinder and also its adverse impact on your computer. Such ransomware are a kind of malware that is specified by on the internet frauds to demand paying the ransom by a victim.
It is better to prevent, than repair and repent!
Most of the instances, VirTool:Win32/Vbinder virus will certainly advise its targets to initiate funds transfer for the objective of neutralizing the amendments that the Trojan infection has actually introduced to the target’s tool.
VirTool:Win32/Vbinder Summary
These alterations can be as adheres to:
VirTool:Win32/Vbinder
The most normal networks through which VirTool:Win32/Vbinder Trojans are injected are:
As quickly as the Trojan is efficiently injected, it will either cipher the information on the sufferer’s PC or avoid the device from functioning in an appropriate manner – while additionally putting a ransom money note that mentions the need for the sufferers to effect the repayment for the purpose of decrypting the papers or restoring the documents system back to the preliminary condition. In the majority of instances, the ransom note will come up when the client restarts the COMPUTER after the system has currently been damaged.
VirTool:Win32/Vbinder circulation networks.
In different corners of the world, VirTool:Win32/Vbinder expands by leaps as well as bounds. Nevertheless, the ransom money notes as well as tricks of obtaining the ransom amount may differ depending upon certain neighborhood (local) setups. The ransom notes as well as methods of extorting the ransom money quantity might vary depending on certain local (regional) settings.
Faulty alerts concerning unlicensed software program.
In certain areas, the Trojans commonly wrongfully report having actually found some unlicensed applications enabled on the victim’s gadget. The sharp then demands the user to pay the ransom.
Faulty statements about unlawful material.
VirTool:Win32/Vbinder popup alert may incorrectly claim to be obtaining from a legislation enforcement organization and also will report having located kid pornography or other prohibited information on the tool. The alert will similarly include a requirement for the individual to pay the ransom.
Как вирусы обманывают человека?
Метафорическая зарисовка. Представители различных генетических вариантов SARS-CoV-2 собрались за круглым столом и обсуждают план захвата мира. Рисунок в полном размере.
Автор
Редакторы
Статья на конкурс «Био/Мол/Текст»: Вирусы умеют не только размножаться внутри клеток хозяина, но и прятаться от его иммунитета. Способов избежать фатальных встреч с оборонными силами организма существует множество, но один из самых хитрых (и потому особенно интересных) механизмов демонстрируют вирусы с измененными генетическими последовательностями. Эта статья расскажет, что такое генотипы и генетические варианты вирусов и почему так важно о них знать.
Конкурс «Био/Мол/Текст»-2020/2021
Эта работа опубликована в номинации «Вирусы и микроорганизмы» конкурса «Био/Мол/Текст»-2020/2021.
Генеральный партнер конкурса — ежегодная биотехнологическая конференция BiotechClub, организованная международной инновационной биотехнологической компанией BIOCAD.
Спонсор конкурса — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.
Спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.
Зачем нам знать о генетических вариантах вирусов?
Новости о коронавирусе на протяжении всего 2020 года оставались самыми читаемыми, а количество научных публикаций о SARS-CoV-2 почти в пять раз превысило число статей по другой «громкой» теме — системам CRISPR/Cas: по данным PubMed их уже больше 60 тысяч! И здесь важнее следить не столько за драматической статистикой заражений и исходов, сколько за потенциалом и способностями возбудителя. Ведь вирусы умеют мутировать и порождать таким образом новые генетические варианты [1].
Генетические варианты вируса — это геномы какого-то вида (или штамма) вируса, отличающиеся друг от друга по последовательности нуклеотидов, и эти отличия могут обусловливать появление новых штаммов. «Генотип», «субтип», «генетический вариант» — термины, отражающие степень геномных различий (в порядке убывания).
По мере накопления знаний по этой теме опасения ученых лишь крепли: мутации могут влиять как на вирулентность, так и на тяжесть протекания заболевания, развитие лекарственной устойчивости и вероятность повторного заражения [2].
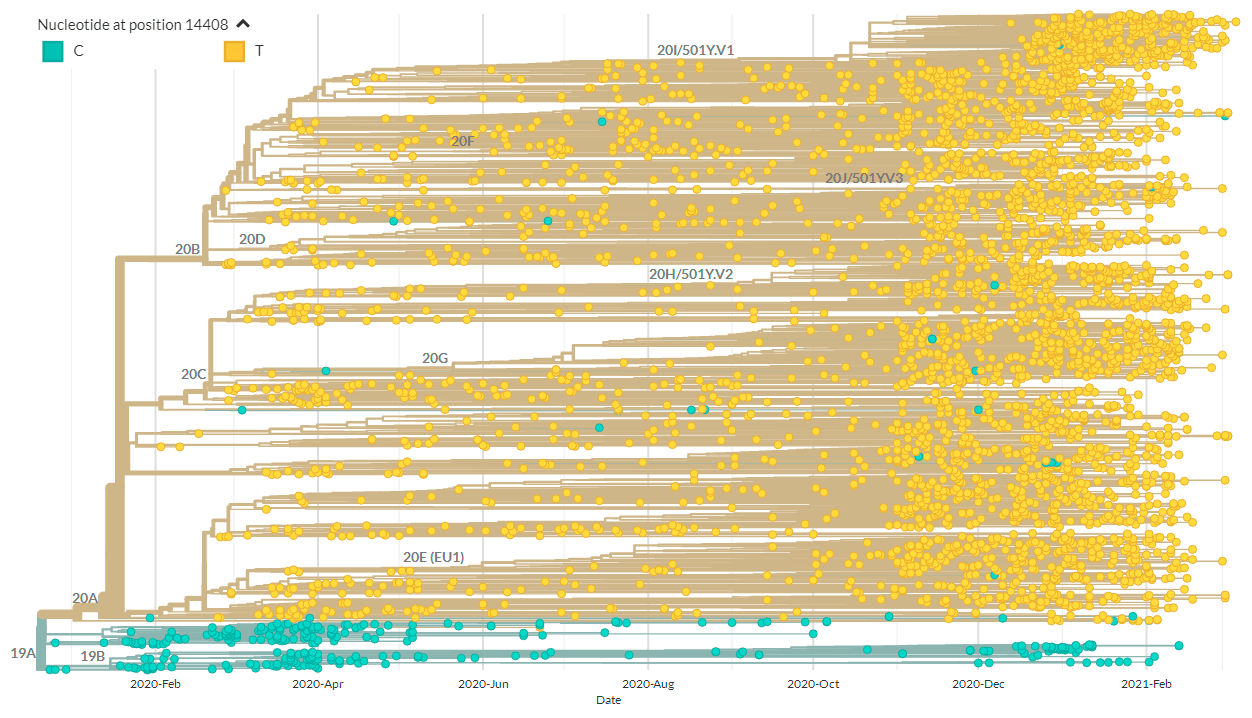
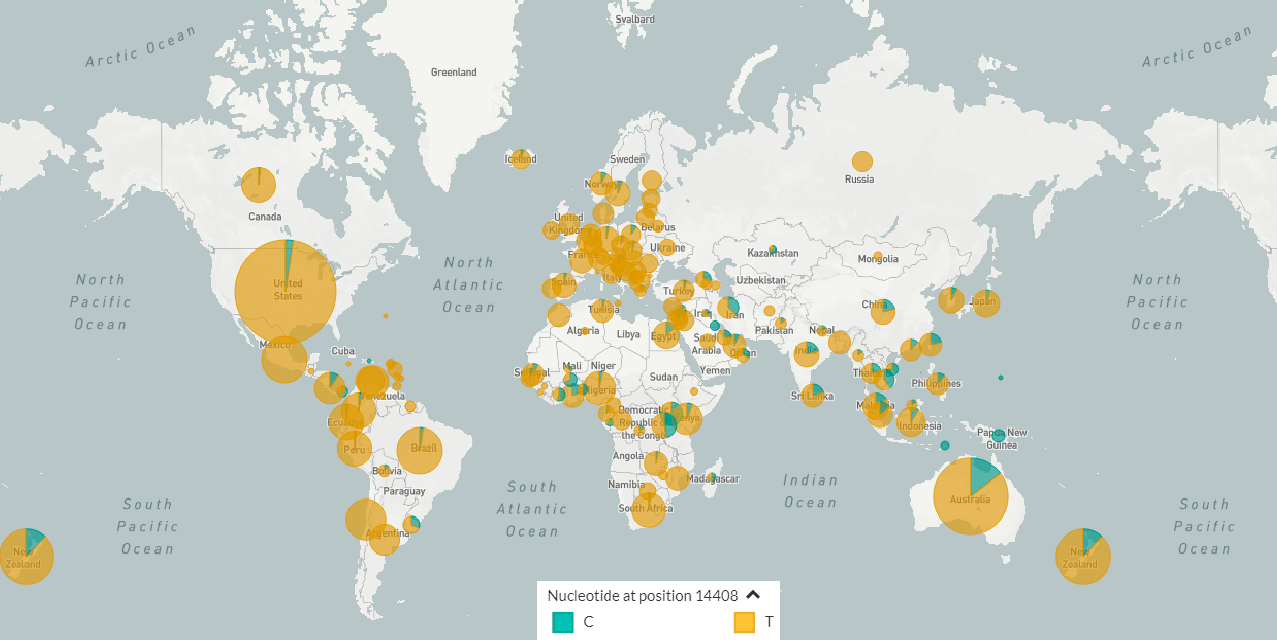
У SARS-CoV-2 весной 2020 года выделяли 3 генотипа: A, B и C [1]. Но сейчас особое внимание обращают на некоторые генетические варианты этого вируса и их географическое распределение (рис. 1) [3]. Известно, что даже самое маленькое изменение в генетическом материале возбудителя способно сильно сказаться на протекании либо распространении заболевания. На что же могли повлиять мутации в геноме SARS-CoV-2?
Рисунок 1а. Схематическое изображение эволюции SARS-CoV-2
Рисунок 1б. Карта распространения генетических вариантов SARS-CoV-2
Например, единственная мутация в гене поверхностного белка (spike-белка), вызвавшая замену его 614-й аминокислоты — D614G, — способствовала распространению SARS-CoV-2 по миру [4], [5].
Другая мутация, C14408T, в последовательности, кодирующей вирусную РНК-зависимую РНК-полимеразу (RdRp), потенциально способна влиять на развитие лекарственной устойчивости [6], [7]. Но самым поразительным можно считать случай, когда у пациента один генетический вариант SARS-CoV-2 заместился другим [8]. Дело в том, что наша иммунная система выстраивает защиту, по сути, от определенного вирусного генотипа. Если же вирус меняется, организм, встречавшийся с его предшествующим вариантом, новый может и не узнать.
Однако можно чуть-чуть успокоиться: мутации SARS-CoV-2 хоть и устроили хорошую суматоху, но так и не показали пока явной клинической значимости — в отличие от изменений ряда других вирусов. О них и пойдет речь дальше.
Вирусы гепатитов и компания
Гепатиты
В 2020 году Нобелевскую премию по физиологии или медицине вручили за открытие возбудителя одного из гепатитов — вируса гепатита С (ВГС, HCV) [9]. Болезнь может протекать без видимых симптомов, но при этом вирус сильно поражает печень. В крайних случаях развивается цирроз или даже рак печени [10]. К счастью, уже есть эффективные средства от гепатита С: по словам нобелевского лауреата Харви Олтера, противовирусные препараты прямого действия позволяют излечивать 95–98% пациентов [9]. Так в чем же подвох?
Интересно, что ВГС генотипов 1 и 4 обычно хуже поддаются терапии и требуют более продолжительного лечения, чем 2 и 3 [12].
| Генотипы ВГС | Субтипы |
|---|---|
| Генотип 1 | 1a, 1b |
| Генотип 2 | 2a, 2b, 2c, 2d |
| Генотип 3 | 3a, 3b, 3c, 3d, 3e, 3f |
| Генотип 4 | 4a, 4b, 4c, 4d, 4e, 4f, 4g, 4h, 4i, 4j |
| Генотип 5 | 5a |
| Генотип 6 | 6a |
| Генотип 7 |
При этом из-за высокой генетической вариативности, то есть больших различий между вирусными генотипами (до 30–35%), против ВГС не получается создать эффективную вакцину. Проблема усугубляется тем, что для тестирования прототипов вакцин нужны небольшие модельные животные, а получить мышей, способных одновременно болеть гепатитом С и имитировать человеческий иммунный ответ на инфекцию, очень трудно. И наконец, для изучения вируса in vitro нужно нарабатывать заразные частицы ВГС, а способные на это клеточные культуры появились лишь недавно [14].
Секвенирование вирусного генома показало, что в России циркулирует рекомбинантный вариант ВГС (RF2k/1b), генетически сходный с генотипами 1 и 2 одновременно. Из-за такой маскировки детекция этого генотипа затруднительна, а значит, и лечение бывает менее эффективным [15].
Итак, чтобы эффективно справиться с гепатитом С, нужно определить генотип его возбудителя. Не менее важно знать и генотип вируса, вызывающего другой гепатит — гепатит B. Да, от ВГВ (HBV) существует прививка [16]. Но! Есть основания считать, что генотипы ВГВ, несмотря на относительно небольшую вариативность (около 8% генома), по-разному влияют на тяжесть заболевания [17], [18].
Стоит, однако, учитывать, что результаты исследований связи вирусных генотипов с особенностями течения болезни весьма противоречивы. Чаще всего это связано с недостаточным размером изученных выборок, что, в свою очередь, обусловлено сложностями массового генотипирования. Из-за этого, например, на Тайване развитие гепатоцеллюлярной карциномы связывают с ВГВ генотипа В, а в Японии и КНР — с ВГВ генотипа С [19]. Тем не менее некоторые авторы приходят к выводу, что генотип ВГВ вообще не имеет большого клинического значения [20].
Хоть пока и нет общих рекомендаций проводить генотипирование ВГВ, ряд ученых призывает сделать его обязательным, поскольку пангенотипной терапии в случае гепатита В не разработано, а эффективность лекарств порой разнится в зависимости от генотипа.
Детекция генотипа вируса может стать хорошим подспорьем для врачей как минимум в двух направлениях: в определении вероятности развития той или иной формы болезни у конкретного пациента и в персонализации лечения. Однако подобных исследований крайне мало, можно даже сказать, что это поле еще совсем не пахано.
Денге
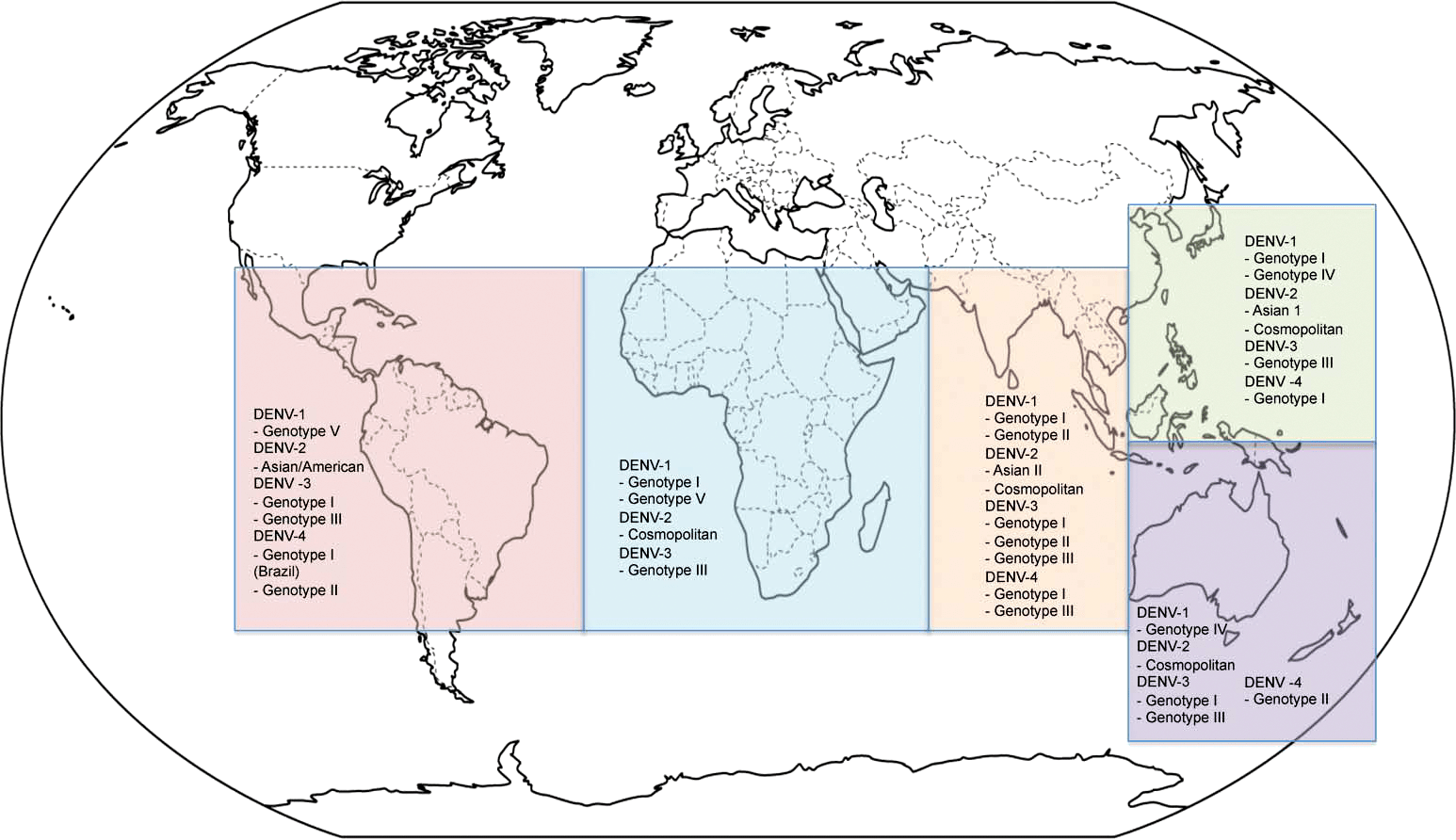
Мы уже заметили, что при разработке вакцин необходимо знать и учитывать разнообразие генотипов вируса. В этом отношении яркими примерами могут служить подходы к производству вакцин от гриппа и менее распространенной болезни — лихорадки денге, о возбудителе которой мы сейчас и расскажем [21].
Рисунок 2. Географическое распределение эндемичных по вирусу денге районов в 2011 году
У вируса денге выделяют четыре серотипа, то есть четыре группы вирусов с общей антигенной структурой. Генотипов у этого возбудителя больше, соответственно, и отслеживать их сложнее. Увы, но знания серотипа порой недостаточно для качественной вакцинации. Например, низкую эффективность одной из проходивших клинические исследования вакцин против серотипа 2 можно объяснить большой вариативностью составляющих его генотипов [22].
Существует мнение, что если эффективность вакцин против денге в новых клинических исследованиях останется низкой, при создании вакцинных препаратов необходимо будет отталкиваться именно от результатов генотипирования [21]. Это нужно и для исключения возможного антителозависимого усиления инфекции в случае, если вакцина будет защищать не от всех серотипов/генотипов, с которыми может встретиться отдельный организм.
Примечание
Антителозависимое усиление инфекции (ADE, antibody-dependent enhancement) — феномен, при котором связывание вируса с cубоптимальными нейтрализующими или не нейтрализующими антителами способствует его проникновению в иммунные клетки с последующей репликацией в них. Из-за ADE непроверенные вакцины могут быть очень опасными: при встрече с инфекцией вместо обеспечения защиты некоторые из них способны утяжелять течение заболевания [23].
Подводя итог, можно сказать, что знание генотипов вирусов необходимо для отслеживания распространения заболеваний по миру, для их лечения, а также для получения эффективных вакцин. К сожалению, пока генотип-специфичная борьба с инфекциями сильно ограничивается в том числе и недостатком информации о вирусных штаммах.
Но как вообще появляется это штаммовое разнообразие?
Вирусная хитрость: механизмы изменения геномов
Вирусы способны изменять свои свойства внутри клеток хозяев и в результате становиться заразнее и опаснее. Впрочем, не стоит пугаться. Обычно вирусная эволюция протекает в сторону снижения летальности, поскольку вирусу, который не убивает своего носителя и почти не вызывает симптомов, намного проще распространиться в популяции. Хоть геномы вирусов и изменяются с довольно высокой частотой, на деле мутации чаще оказываются нейтральными, не влекущими заметных последствий для вируса и его хозяина. Очень немногие из них действительно вносят вклад в дальнейшую эволюцию [24].
В основе способности вирусов к изменениям лежат мутации и/или обмен генетическим материалом между разными вирусами, результаты которых закрепляются или не закрепляются давлением естественного отбора.
Мутация — это изменение последовательности нуклеотидов в определенном участке генома, нередко приводящее к изменениям структуры и/или функций организма или вируса. Мутации могут возникать из-за ошибок работы ферментов, создающих копии геномов, или под действием среды.
Когда одну и ту же клетку заражает два родственных вируса, могут образовываться гибридные вирусы, содержащие измененный по сравнению с родительскими формами генетический материал. Этот процесс называют рекомбинацией или реассортацией, если у вирусов сегментированный геном (в частицу он упаковывается отдельными сегментами типа мини-хромосом) [25].
Для справки
До введения термина «реассортация» в научный обиход рекомбинацией называли любой обмен генами, включая и те процессы, которые сейчас со знанием дела именуют реассортацией [25].
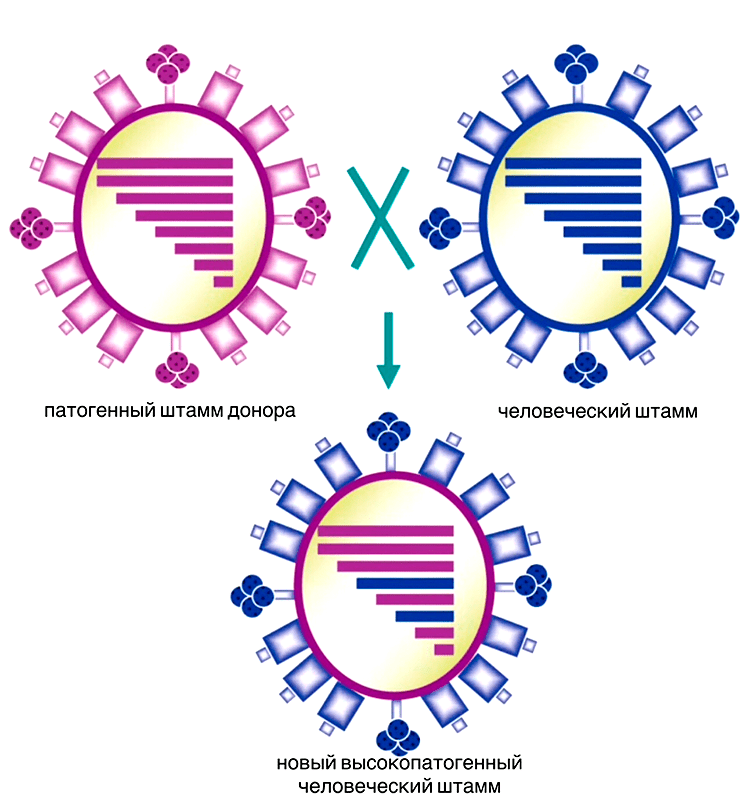
Реассортация очень напоминает появление детей у родителей: когда два разных вириона попадают в одну клетку и приступают к размножению, они могут обменяться частями геномов (рис. 3). В результате получится новая вариация (штамм) вируса, которая может значительно отличаться от своих предков [25]. Такие вирусы порой становятся неузнаваемыми для иммунной системы и распространяются, вызывая эпидемии и пандемии. Этот сценарий характерен, например, для вирусов гриппа. Некоторые исследователи винят в пандемии той же «испанки» именно вирусную реассортацию [26].
Рисунок 3. Реассортация вирусов, которая приводит к появлению штамма с измененным генетическим материалом
Благодаря мутациям и обмену генетическим материалом вирус может даже менять своего хозяина. Так SARS-CoV-1 от летучих мышей перешел в семейство виверровых (к мусангам и циветам), а затем и к людям. В начале 2000-х этот вирус вызвал эпидемию, охватившую 29 стран [28].
Новые генотипы могут возникать и в ходе лабораторных пассажей, когда вирусом последовательно заражают нескольких животных, выделяя из них новую чистую культуру возбудителя [29]. Такая процедура нужна, в частности, для тестирования противовирусных лекарств и вакцин.
Свойства вируса во время пассажей меняются ступенчато. В первых пассажах в основном обнаруживают вирионы, изменившие какой-то один генетический признак. Но с увеличением числа пассажей у подавляющего большинства вирусных частиц наблюдают изменение многих генетических признаков.
Кроме рекомбинации и мутаций, изменчивость вируса может быть обусловлена влиянием хозяина (host-controlled variation). Такие модификации не затрагивают генетический материал вируса и встречаются, например, у ДНК-содержащих бактериофагов, вирусов гриппа и Сендай. Клетка может влиять на характер синтезируемых в ней вирусных компонентов. Или в вирусную частицу могут попадать хозяйские белки и липиды. Поэтому при смене клетки-хозяина в структуре оболочки вириона меняются и антигены, с помощью которых организм узнает вирус.
Итак, образование новых вирусных генотипов — совершенно обычное явление, основанное на стандартных эволюционных процессах. Однако как нам эти генотипы детектировать?
Как выявляют генотипы вирусов?
Теперь, когда мы знаем, как возникают вирусные генотипы и как от генетического варианта возбудителя могут зависеть течение, распространение и лечение заболевания, перейдем к обсуждению лабораторных методов. Они позволяют нам определять, вирус какого генотипа вызвал болезнь у конкретного пациента. Рассмотрим методы детекции генотипов на примере вируса ВГС. В настоящее время лабораторные анализы, используемые в схемах диагностики и лечения гепатита C, представлены серологическими тестами для обнаружения антител к ВГС, молекулярными тестами для выявления и количественной оценки РНК ВГС, а также методами генотипирования возбудителя [30].
При первоначальной диагностике гепатита C учитывают симптоматику и уровни ферментов печени (особенно аланинаминотрансферазы, АЛТ) в крови. У пациентов с подозрением на гепатит C иммуноферментным анализом (EIA) [31] или хемилюминесцентным иммуноанализом (CIA) выявляют антитела к ВГС. В популяциях с низким риском инфицирования этим вирусом отрицательного результата EIA или CIA достаточно, чтобы исключить заражение гепатитом C. Но важно помнить, что у пациентов с ВИЧ или последней стадией почечной недостаточности серологические тесты на антитела к ВГС могут давать ложноотрицательные результаты. Если тест выявил антитела или допускается возможность ложноотрицательного результата, в организме пациента должны искать РНК самогό вируса.
Определение статуса инфекции ВГС, решение о лечении и мониторинг ответа на него зависят от трех важных факторов: обнаружения РНК вируса гепатита С, ее количества и вирусного генотипа. Для оценки всех этих параметров есть несколько коммерческих тест-систем. Они различаются по диапазону обнаружения, чувствительности, специфичности, стоимости и сложности использования.
Выявление РНК вируса гепатита С основано на принципе амплификации нуклеиновых кислот [32], причем применяют здесь комбинацию разновидностей полимеразной цепной реакции (ПЦР): качественную ПЦР, опосредованную транскрипцией амплификацию (ТМА) и количественную ПЦР в реальном времени.
Генотипирование ВГС необходимо для назначения оптимальной схемы лечения. Генотип этого вируса можно определить несколькими методами, нацеленными на гены вирусных белков (E1, NS4 и NS5) и на 5′-нетранслируемую область (5′-UTR) генома ВГС. Они включают простую ПЦР, гибридизацию с генотип-специфичными зондами и ПЦР в реальном времени. Однако для более точного определения вирусного генотипа следует прибегать к методам секвенирования нового поколения (NGS) [33].
Наш проект HaploSense
Как мы уже поняли, определять генотипы сложно, поскольку практически нет быстрых и доступных тестов. Наша команда студентов и аспирантов под названием Moscow 2020 решила изменить эту ситуацию.
На международном конкурсе iGEM в этом году мы представили проект детектора генотипов вируса гепатита С. В основе детекции лежит система CRISPR-Cas, с которой многие читатели уже знакомы [34], [35], а принцип работы напоминает популярные методы детекции SHERLOCK (Specific High sensitivity Enzymatic Reporter unLOCKing) и DETECTR (DNA Endonuclease Targeted CRISPR Trans Reporter) [35]. Но есть и важные отличия, о которых сейчас расскажем.
В своей тест-системе мы использовали самый маленький из открытых к этому моменту Cas-белков — CasX (или Cas12e) из Deltaproteobacteria: он состоит из 980 аминокислотных остатков по сравнению с 1300 у Cas9 [36]. Как и Cas13a с Cas12a, маленький CasX обладает коллатеральной нуклеазной активностью (может неспецифически резать нуклеотидные последовательности, с которыми встретится после связывания с мишенью): она позволяет разрезать олигонуклеотиды с флуоресцентными метками после прикрепления белка к геному вируса. Но ВГС — РНК-содержащий вирус, поэтому для связывания с ним CasX нужно провести дополнительную реакцию: с помощью обратной транскрипции получить комплементарную последовательность ДНК.
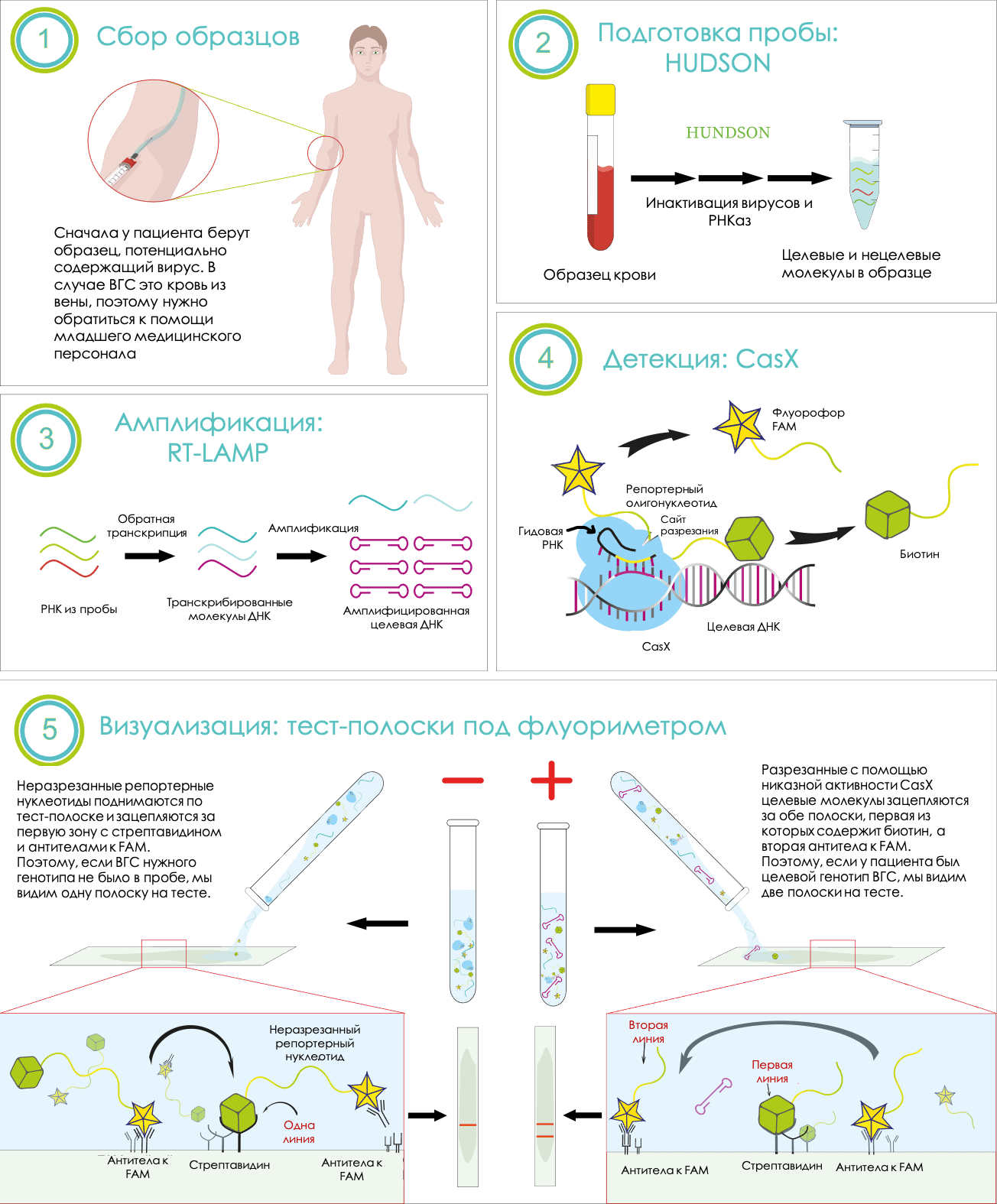
Итак, в нашей системе четыре основные стадии (рис. 4):
Пока наша тест-система предполагает определение только одного генетического варианта ВГС — рекомбинантного RF2k/1b, распространенного в России. В 2020 году доступ в лабораторию для нас был закрыт, поэтому систему предстоит еще собрать и протестировать. Если все лабораторные испытания пройдут успешно, мы планируем расширить специфичность системы на все генотипы вируса, не умножая при этом количество приборов.
Рисунок 4. Схема детекции генотипов ВГС с помощью HaploSense
Такая на первый взгляд сложная система позволит определять генотип возбудителя гепатита С быстрее, вне специально оборудованной лаборатории и с не меньшей точностью, чем ПЦР. Мы надеемся, что когда-нибудь такой подход поможет сделать тестирование массовым и доступным.
Подробнее о iGEM
В 2020 году команда студентов с биологического факультета МГУ представила свою разработку на самом престижном международном конкурсе по синтетической биологии — The International Genetically Engineered Machines competition (iGEM). С английского название переводится как «Международное соревнование генно-инженерных машин». Это соревнование учредили в 2003 году в Массачусетском технологическом институте (Бостон, США). Школьники, студенты и аспиранты со всего мира и с разным академическим бэкграундом, начиная от журналистов и экономистов и заканчивая айтишниками и биологами, собираются в команды, в течение года работают над актуальной задачей и представляют свои проекты на осенней, финальной конференции Giant Jamboree. Конкурс iGEM уникален тем, что формирует открытое сообщество людей, которые обмениваются друг с другом и миром своими наработками. Выгодно отличают конкурс также комплексность и разноплановость проектов: упор делается на применение инженерных принципов и подходов, использование методов моделирования, обсуждение и проработку проекта с потенциальными пользователями и экспертами из разных областей (науки, бизнеса, права, государственного управления и т.д.). Образовательная деятельность, популяризация наук, налаживание между учеными и обществом мостов с целью обсуждения актуальных проблем — все это тоже входит в задачи команды. В этом году из-за пандемии конкурс проходил онлайн. Ядро нашей команды составляли студенты биологического факультета МГУ, которые получили бесценный опыт и выиграли золотую медаль. Однако подробнее об iGEM мы поговорим с вами в следующий раз [39].
Работа в команде
В конце марта 2020 года команда Moscow 2019 собрала новый состав для участия в конкурсе iGEM (рис. 5). Тогда впервые встретились незнакомые друг другу люди с общим желанием — создать проект в области синтетической биологии, который мог бы что-то изменить в мире.
Идея нашего проекта появилась только спустя полтора месяца, в начале мая. iGEM предлагает полную тематическую свободу: можно делать хлеб из дрожжей на Марсе, очищать воду бактериями, синтезировать натуральную краску для волос или разрабатывать системы мониторинга заболеваний. На выбор темы для нашего проекта сильно повлиял руководитель команды, Алексей Константинович Шайтан. Его лаборатория использует в работе системы CRISPR-Cas, а на их основе можно создавать детекторы заболеваний. Пандемия COVID-19 только начиналась, но уже было ясно, что SARS-CoV-2 необходимо выявлять быстро, массово и с высокой точностью. Так мы и создали наш проект — с целью детектировать генотипы коронавируса.
Очень важное требование конкурса — актуальность разработки. Другими словами, важно было понять, что наш проект нужен людям и его будут использовать. Этим проекты iGEM сильно отличаются от рутинной работы научных лабораторий. Именно поэтому мы встречались с экспертами, писали письма главному эпидемиологу Министерства здравоохранения, Николаю Ивановичу Брико, размещали посты в социальных сетях. Обратная связь полностью изменила наш проект: HaploSense переориентировался на детекцию генотипов вируса гепатита С.
С другой стороны, важен был сам детектор — как он будет работать, выглядеть, сможем ли мы его вообще собрать. Здесь нам на помощь пришел спонсор, компания BIOCAD. Эксперты компании консультировали нас относительно идеи проекта и ее реализуемости в столь короткие сроки. Они рассказали нам, как готовить патенты и выводить продукт на рынок. А это далеко не простые процессы.
В результате мы проанализировали гору тематической литературы, смогли придумать целостную систему на основе технологий CRISPR-Cas, провели ее моделирование и биоинформатический анализ.
Надо сказать, что организаторы iGEM помогают командам на протяжении всего пути: устраивают семинары, знакомят со специалистами, создают удобные платформы. А особенно поддерживают взаимодействие между командами. Все полгода мы общались и встречались с мотивированными ребятами из Америки, Эстонии, Индии, Франции, Германии и России (в этом году в конкурсе участвовали две команды из нашей страны). После таких встреч мы понимали, что можем сделать хороший, качественный проект, даже будучи студентами.
Рисунок 5. Команда iGEM Moscow 2020
Пандемия, конечно, сыграла свою роль в работе нашей команды: мы работали дистанционно и встречались друг с другом офлайн всего четыре раза. По-настоящему сплоченными мы стали, когда приблизились конкурсные дедлайны. Мы уложились в срок благодаря слаженной работе команды. Одному человеку было бы невозможно справиться: кроме разработки идеи проекта, моделирования и проведения экспериментов нам предстояло сделать сайт с описанием проекта, два видео о команде и работе, заполнить форму безопасности, написать обзор по теме, да и это еще не все. Именно поэтому проект iGEM — прежде всего командная работа.
Итоги конкурса подводятся осенью, в начале ноября, на Giant Jamboree — огромной конференции, где команды, профессора, лекторы и судьи собираются, чтобы обсудить проекты, подметить их сильные и слабые стороны, сформировать новые коллаборации и просто хорошо провести время. Это финал iGEM: проекты уже подготовлены, критерии конкурса соблюдены. Казалось бы, можно выдохнуть… Но здесь же команды встречаются с судьями — исследователями, которые будут оценивать проекты и детально их рецензировать. Мы, конечно, тоже общались с судьями (в этом году онлайн): в воскресенье, в 17:00, нас спрашивали, почему мы использовали LAMP, сколько тест-полосок будем применять, ну и много чего другого. А после нашу команду ждала неделя, полная лекций по синтетической биологии и общения с коллегами со всего мира, а также викторины по синтетической биологии и церемония награждения. В итоге мы выиграли золотую медаль и создали хороший проект, который продолжим развивать и, надеемся, доведем до состояния полноценной тест-системы, подходящей для обычных поликлиник.
Мы советуем всем молодым исследователям принимать участие в iGEM. Этот конкурс стал для нас лучшим событием 2020 года. Создать проект с нуля возможно, нужно только желание!