болезнь кавана что такое
Новости
Болезнь Канавана – грозный враг детей
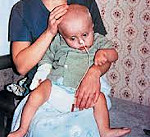
Рождение ребенка – большая радость для отца и матери. Но иной раз, к сожалению, это событие оборачивается горем, когда становится ясно, что малыш поражен тяжелым и неизлечимым заболеванием. Одно из таких заболеваний – болезнь Канавана (или, точнее, «болезнь Канавана – ван Богерта»). Этот грозный недуг представляет собой наследственно-дегенеративное поражение нервной системы, приводящее к дистрофии белого вещества головного мозга. Как следствие – резкое ухудшение общего состояния и развития ребенка, нарушение моторики, трудности при глотании пищи, мышечная дистрофия. По мере прогрессирования болезни, возникают судороги, эпилептические припадки, ухудшается зрение (вплоть до слепоты). Заболевание довольно быстро приводит к смерти, способов излечения пока не найдено.
Вряд ли нужно объяснять, какая это беда не только для ребенка, но и для его родителей. Поэтому очень важно знать, из-за чего возникает такое заболевание, можно ли его предотвратить и что следует делать, если оно, к несчастью, диагностировано.
В чем причина возникновения болезни Канавана и как она диагностируется
Все вышеуказанные расстройства происходят вследствие генетической мутации, возникающей в 17-й хромосоме человека. Эта мутация приводит к хроническому недостатку в организме ребенка фермента аспартоацилазы, «отвечающей» за расщепление N-ацетил-аспарагиновой кислоты. Указанная кислота возникает естественным путем в процессе жизнедеятельности клеток центральной нервной системы. До тех пор, пока ее концентрация не превышает предельно допустимых величин, она не опасна, но патологически высокий уровень ее содержания в организме приводит к нарушению метаболизма липидов. А это, в свою очередь, вызывает разрушение оболочки нервных клеток (в значительной степени, состоящей из липидов). Нейроны, лишенные оболочки, теряют способность к нормальному функционированию и быстро погибают, со всеми вытекающими последствиями для организма.
Диагноз «болезнь Канавана» ставится ребенку неврологом по результатам анализа мочи на концентрацию N-ацетил-аспарагиновой кислоты. У больного наблюдается неестественно высокое содержание этого вещества (нередко до 20-кратного превышения нормы!) Анализ мочи проводится в большинстве случаев хроматографическим или масс-спектрометрическим методом.
Другие методы исследования, вплоть до МРТ и электроэнцефалографии, затруднительно производить, и к тому же они не дают должной эффективности ввиду малого возраста пациента.
Общие сведения об этом заболевании
Начиная с 19-го века, многие медики фиксировали факт неестественно высокого процента психических расстройств и младенческой смертности среди евреев ашкенази. Изучение этого факта по мере развития науки вообще и медицины в частности позволило Миртелю Канавану в 1931 году описать основные симптомы этого заболевания, получившего его имя. Разумеется, тогда еще не было известно о генетической мутации в 17-й хромосоме, поскольку генетика только начала развиваться и до открытия знаменитой «двойной спирали» было далеко.
А в 1987 году врач Рубен Маталон добился от семьи своих пациентов (где были две девочки с болезнью Канавана) согласия на предоставление их биологических материалов для исследований. Получив образцы тканей девочек, Маталон начал эксперименты с целью обнаружения гена, «ответственного» за развитие болезни, и через несколько лет его усилия увенчались блестящим успехом. (В источниках встречаются упоминания различных дат: 1991 или 1993 год). Впоследствии Маталон разработал тест, позволяющий определить риск развития болезни Канавана у плода во время беременности, что привело к конфликту с Фондом Канавана, который сам, в свою очередь, разработал аналогичный тест и бесплатно распространял его среди беременных. Споры и судебные тяжбы завершились подписанием компромиссного мирового соглашения.
Возникнуть это заболевание может у ребенка любой национальности, но до сих пор в особой «группе риска» находятся евреи ашкенази, поскольку среди них наибольшее число носителей больного гена: порядка одного человека из сорока (т.е. около 2,5%).
Болезнь Канавана (спонгиозная младенческая дегенерация) — генетическое нейродегенеративное заболевание, в основе которого лежит недостаток фермента аспартоацилазы, приводящий к демиелинизации нервных волокон головного мозга. Болезнь Канавана проявляется в раннем детском возрасте нарушениями моторики и развития ребенка, затруднениями при приеме пищи, мышечной гипотонией, макроцефалией, эпилептическими припадками, слепотой. Диагностируется болезнь Канавана по анализу мочи на N-ацетил-аспарагиновую кислоту. Эффективная терапия заболевания пока не найдена. Производятся попытки лечить болезнь Канавана при помощи метаболической терапии и путем применения генных технологий, способных заменить патологическую аберрацию на здоровый ген.
МКБ-10
Общие сведения
Болезнь Канавана была описана Миртелем Канаваном в 1931 году. А в 1991 году Рубеном Маталоном был выделен ген, отвечающий за это заболевание. Спустя несколько лет стал применяться тест, позволяющий диагностировать болезнь Канавана еще в период ведения беременности. Болезнь Канавана встречается у людей любой национальности. Однако чаще всего ею болеют евреи ашкенази. Среди них носителем генной аберрации, кодирующей болезнь Канавана, является 1 из 40 человек.
Современная неврология относит болезнь Канавана к так называемым лейкодистрофиям — генетически обусловленным дегенеративным заболеваниям нервной системы, в основе которых лежит нарушение метаболизма липидов. Чаще всего нарушения касаются миелина, который на 70-75% состоит из липидов. Распад миелина приводит к разрушению миелиновой оболочки нервных стволов и вторичной гибели нейронов. Лежащая в основе заболевания прогрессирующая демиелинизация делает болезнь Канавана и другие лейкодистрофии схожими с демиелинизирующими заболеваниями головного мозга, которые имеют приобретенный характер (рассеянным склерозом, рассеянным энцефаломиелитом, полирадикулоневропатией Гийена-Барре, болезнью Девика).
Причины возникновения болезни Канавана
Болезнь Канавана связана с генетическим нарушением в геноме ASРА, расположенном в 17-й хромосоме. Вследствие этой генетической аберрации снижен синтез фермента аспартоацилазы, расщепляющего N-ацетил-аспарагиновую кислоту, образующуюся в процессе жизнедеятельности клеток центральной нервной системы. Патологически высокий уровень этой кислоты приводит к повреждению миелиновой оболочки нервных волокон головного мозга. Миелиновая оболочка выполняет роль своеобразного изолятора, не позволяющего нервному импульсу переходить с одного нервного волокна на другое. Таким образом, миелиновая оболочка способствует точному и быстрому проведению нервных импульсов. При ее разрушении этот процесс нарушается, что и является непосредственной причиной клинических проявлений болезни Канавана.
Болезнь Канавана передается по аутосомно-рецессивному типу наследования. Это означает, что в ситуации, когда оба родителя являются носителями патологического гена, вероятность рождения у них ребенка, имеющего болезнь Канавана, равна 25%.
Симптомы болезни Канавана
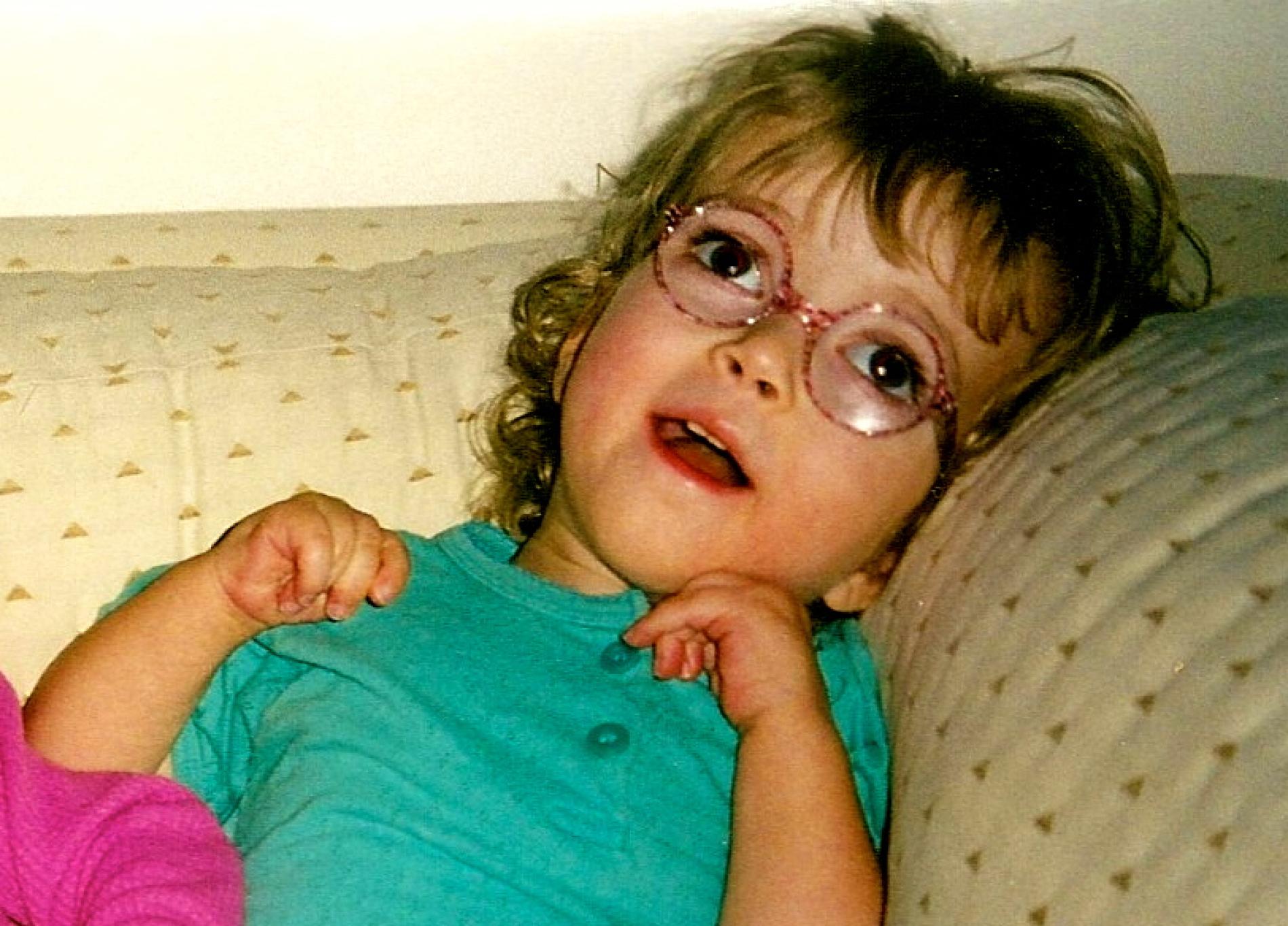
При рождении ребенок, имеющий болезнь Канавана, ничем не отличается от здоровых новорожденных. Симптомы заболевания начинают проявляться спустя месяц, а чаще в период от 3 месяцев до полугода. Отмечается задержка в развитии, замедленность движений, потеря уже приобретенных двигательных навыков, снижение мышечного тонуса. Возникающие затруднения при глотании обуславливают существенные трудности при кормлении ребенка. Примерно к 4-ому месяцу жизни становиться заметно увеличение головы (макроцефалия). Прогрессирование болезни Канавана сопровождается возникновением эпилептических припадков. Демиелинизация и атрофия зрительного нерва приводит к развитию слепоты.
Диагностика болезни Канавана
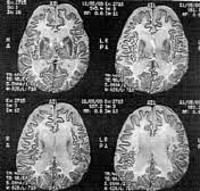
Болезнь Канавана представляет для невролога определенные сложности в диагностике, поскольку демиелинизирующий процесс наблюдается при целом ряде как врожденных, так и приобретенных заболеваний. Стандартные методы первичного неврологического обследования, такие как электроэнцефалография и ультрасонография не выявляют специфических изменений. Проведение МРТ головного мозга затруднено из-за слишком раннего возраста пациентов. Наиболее достоверным методом, позволяющим диагностировать болезнь Канавана, является анализ мочи на N-ацетил-аспарагиновую кислоту.
Генетики рекомендуют всем лицам еврейской национальности при планировании беременности проходить скрининг на наличие генной мутации, определяющей болезнь Канавана. Скрининг следует проходить также тем людям, в семье которых наблюдался случай этого заболевания. Разработаны методы пренатальной диагностики, позволяющие установить болезнь Канавана еще до рождения ребенка. Показанием к проведению подобного исследования является установленное носительство патологического гена у обоих родителей. Материалом для исследования на болезнь Канавана служат амниотическая жидкость, полученная в результате амниоцентеза, или ворсины хориона, взятые в ходе трансабдоминальной или трансцервикальной биопсии хориона.
Лечение болезни Канавана
В настоящее время не существует методики, при помощи которой можно было бы эффективно лечить болезнь Канавана. Замедлить развитие заболевания можно при применении метаболической терапии. Она заключается в приеме внутрь целого комплекса лекарственных препаратов: цитрата лития, ацетата кальция, сукцината натрия.
Наиболее оптимистичными среди современных экспериментальных разработок в области лечения болезни Канавана является генная терапия. Разработка метода генной терапии, способного значительно продлить жизнь имеющим болезнь Канавана пациентам, проводится в Нью Джерси (США). Ее идея заключается в клонировании и внедрении в организм здорового гена, способного заменить патологический ген. Носителями нового искусственно синтезированного гена являются непатогенные аденоассоциированные вирусы, которые в растворе водятся в головной мозг через 6 катетеров, установленных в различных его областях. Экспериментальное лечение прошли 13 детей. Их последующее обследование показало, что в результате генной терапии болезнь Канавана замедлила свое прогрессирование, произошло снижение токсичной N-ацетил-аспарагиновой кислоты и увеличение содержание миелина.
Прогноз болезни Канавана
К сожалению, болезнь Канавана приводит к летальному исходу еще в младенческом возрасте. В редких случаях больные доживают до возраста 10 лет.
Болезнь кавана что такое
а) Терминология:
1. Сокращения:
• Болезнь Канавана (БК)
2. Синонимы:
• Спонгиоформная лейкодистрофия, спонгиозная дегенерация ЦНС, болезнь Канавана-ван-Богарта-Бертрана, недостаточность аспартазилазы, недостаточность ASPA, недостаточность ASP, недостаточность аминоацилазаы 2, недостаточность ACY2
3. Определение:
• Прогрессирующая аутосомно-рецессивная спонгиоформная лейкодистрофия
1. Общие характеристики болезни Канавана:
• Лучший диагностический критерий
о Мегалэнцефалия с диффузным ↑ сигнала от белого вещества на Т2-ВИ и ДВИ, а также ↑ пика NAA
• Локализация:
о Белое вещество (БВ): вовлечение в процесс субкортикальных U-волокон, сохранность внутренних капсул и мозолистого тела
о Таламусы, бледные шары (БШ), ± зубчатые ядра, сохранность хвостатых ядер и скорлупы
2. КТ признаки болезни Канавана:
• Бесконтрастная КТ:
о Диффузное ↓ плотности пораженных зон
3. МРТ признаки болезни Канавана:
• Т1-ВИ:
о Гипоинтенсивный сигнал от пораженных зон
• Т2-ВИ:
о Гиперинтенсивный сигнал от пораженных зон
• ДВИ:
о Гиперинтенсивный сигнал, ИКД от нормального до ↓ в пораженных зонах
• Постконтрастные Т1-ВИ:
о Контрастное усиление отсутствует
• МР-спектроскопия:
о ↑ NAA/Cr, ↓ Cho/Cr
4. Рекомендации по визуализации:
• Лучший инструмент визуализации:
о МРТ
• Совет по протоколу исследования:
о Т2-ВИ, ДВИ и МР-спектроскопия
в) Дифференциальная диагностика болезни Канавана:
1. Болезнь «кленового сиропа»:
• ↑ аминокислот с разветвленной цепью + кетокислот
2. Болезнь Пелицеуса-Мерцбахера:
• ↑ ИКД, сохранность БШ и таламусов
3. Мерозиндефицитная врожденная мышечная дистрофия:
• ↑ ИКД, сохранность БШ и таламусов
4. Болезнь Александера:
• Характерно вовлечение БВ лобных долей, накопление контраста
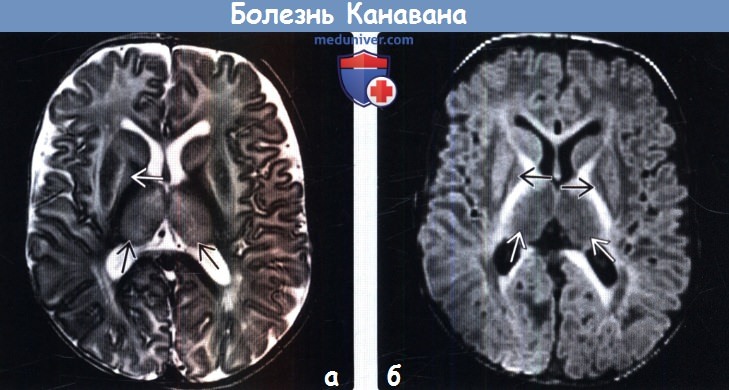
(б) МРТ, Т1-ВИ, аксиальный срез: у этого же шестимесячного ребенка отмечается диффузное снижение интенсивности сигнала от белого вещества, таламусов и бледных шаров. Внутренние капсулы, мозолистое тело, хвостатые ядра, а также скорлупа имеют нормальную интенсивность сигнала.
1. Общие характеристики болезни Канавана:
• Этиология:
о Недостаточность аспартоацилазы (которая метаболизирует N-a-цетиласпартат [NAA]) → ↑ ↑ NAA в головном мозге и моче
• Генетика:
о Аутосомно-рецессивный тип наследования → ген ASPA = длинное плечо 17-й хромосомы
2. Стадирование и классификация:
• Раннее начало → более быстрое прогрессирование
3. Макроскопические и хирургические особенности:
• Отек-набухание головного мозга
4. Микроскопия:
• Спонгиоформная дегенерация белого вещества; набухание астроцитов в БШ и таламусах
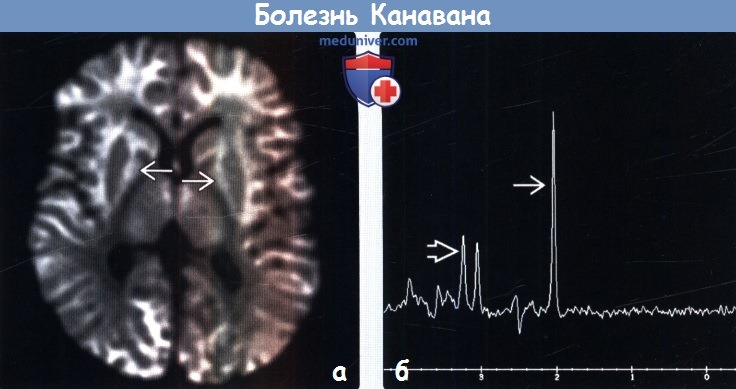
(б) Протонная МР-спектроскопия на томографе 1,5Т в аксиальной плоскости, длинное время эхо (ТЕ = 144 мс), область интереса в полуовальном центре: определяется выраженное относительное увеличение пика NAA и снижение пика холина по отношению к Cr для этого возраста.
г) Клиническая картина:
1. Проявления болезни Канавана:
• Наиболее частые признаки/симптомы:
о Три варианта клинического течения (в зависимости от возраста при постановке диагноза):
— Врожденный (первые несколько дней жизни):
Гипотония, быстрое наступление летального исхода
— Инфантильный (3-6 месяцев)
Наиболее частый вариант
Гипотония, запрокидывание головы, макроцефалия → судороги, мышечная спастичность, потеря зрения
— Ювенильный
о Дебют в возрасте 4-5 лет; наиболее медленно прогрессирующий вариант БК
• Клинический профиль:
о Раннее развитие тяжелой гипотонии и макроцефалия
2. Демография:
• Этническая принадлежность
о ↑ риск у евреев-ашкеназов (носительство в одном из 40 случаев)
3. Течение и прогноз:
• Неумолимо прогрессирующее нейродегенеративное заболевание: хроническое вегетативное состояние с вегетативными кризами → летальный исход к концу первой декады
4. Лечение:
• Методов лечения с доказанной эффективностью не существует (угнетение синтеза NAA путем нарушения работы гена Nat8l у мышиной модели)
д) Диагностическая памятка. Советы по интерпретации изображений:
• Отек-набухание головного мозга с ↑ интенсивности сигнала от белого вещества на Т2-ВИ и ДВИ, вовлечение БШ и таламусов
е) Список литературы:
1. Guo F et al: Ablating N-acetylaspartate prevents leukdystrophy in a Canavan disease model. Ann Neurol. 77(5):884-8, 2015
2. Baslow MH et al: Canavan disease, a rare early-onset human spongiform leukodystrophy: insights into its genesis and possible clinical interventions. Biochimie. 95(4):946-56, 2013
3. van der Knaap MS et al: Defining and categorizing leukoencephalopathies of unknown origin: MR imaging approach. Radiology. 213(1):121-33, 1999
— Вернуться в оглавление раздела «Лучевая медицина»
Редактор: Искандер Милевски. Дата публикации: 24.4.2019
Болезнь Канавана
Проявляющееся в раннем детстве неврологическое заболевание, сопровождающееся нарушением моторики, гипотонией мышц, приступами эпилепсии, слепотой и макроцефалией, характеризующееся дефицитом фермента аспартоацилазы, называется спонгиозной дегенерацией, или болезнью Канавана.
По какой причине развивается болезнь Канавана?
Развитие патологии ведёт к демиелинизации нервных волокон головного мозга. Заболевание имеет генномутационную природу развития. Необходимо отметить, что данная патология относится к разряду редко встречаемых неврологических заболеваний. В подавляющем большинстве случаев заболевание развивается на первом году жизни ребёнка. К сожалению, приходится констатировать неутешительные результаты современных методов терапии. Неврологи относят патологию к разряду лейкодистрофии. Причиной развития патологии является мутация гена ASPA, который находится на семнадцатой хромосоме, отвечающего за выработку фермента аспартоацилазы, расщепляющего отдельные молекулы аспарагиновый кислоты, формирующейся в тканях нервной системы. Дефицит фермента неизбежно ведёт к переизбытку аспарагиновой кислоты, в следствие чего происходит разрушение миелиновой оболочки. Данный патологический процесс оставляет нервные клетки незащищенными и значительно ухудшает передачу нейронных импульсов. Болезнь Канавана относят к группе дегенеративных неврологических заболеваний.
В качестве основных симптомов болезни Канавана выделяют:
Как правило, к двухлетнему возрасту атрофируется зрительный нерв, что приводит к полной потере зрения.
Высокую концентрацию аспарагиновой кислоты позволяет установить общий анализ мочи. Для точной диагностики необходимо провести биохимический анализ крови, диагностику ДНК, магнитно-резонансную томографию. После подтверждения диагноза болезни Канавана невролог назначает симптоматическую терапию.
Как мы уже говорили выше, прогноз неутешительный. В большинстве случаев летальный исход наступает до достижения ребёнком десятилетнего возраста. Сегодня в специализированных клиниках проводят искусственную замену матированного гена на здоровый. Это позволяет значительно продлить жизнь больному, однако летальный исход неизбежен. Все, чего пока удалось добиться врачам в области лечения болезни Канавана — это увеличить продолжительность жизни больного до двадцати лет. На сегодняшний день отсутствует также специфическая профилактика данной патологии.
Болезнь Канавана
Внимание! Информация носит ознакомительный характер и не предназначена для постановки диагноза и назначения лечения. Всегда консультируйтесь с профильным врачом!
Что такое болезнь Канавана?
Болезнь Канавана (также называемая спонгиозная дегенерация, болезнь Канавана — ван-Богарта — Бертранда) — это редкое генетическое неврологическое заболевание, характеризующееся губчатой дегенерацией белого вещества в мозге. Больные дети при рождении кажутся нормальными, но обычно в возрасте 3-6 месяцев начитают появляться первые симптомы. Симптомы могут включать ненормально большую голову (макроцефалия), отсутствие контроля над головой, пониженный мышечный тонус, приводящий к вялости, и задержки в достижении основных этапов развития, таких как самостоятельное сидение и ходьба.
У большинства затронутых детей к 10 годам развиваются опасные для жизни осложнения. Болезнь Канавана возникает из-за мутаций в гене аспартоацилазы (ген ASPA), влияющий на распад (метаболизм) N-ацетил-L-аспарагиновой кислоты (NAA). Наследуется как аутосомно-рецессивное состояние.
Болезнь Канавана относится к группе заболеваний, известных как лейкодистрофии. Лейкодистрофии представляют собой группу редких, прогрессирующих, метаболических, генетических нарушений, поражающих головной мозг, спинной мозг и часто нервы вне центральной нервной системы (периферические нервы).
Каждый тип лейкодистрофии вызван дефектом, влияющей на определенный ген, приводящий к аномальному развитию одного из по меньшей мере 10 различных химических веществ, которые составляют белое вещество мозга. Белое вещество — ткань, состоящая из нервных волокон. Многие из этих нервных волокон покрыты набором жиров (липидов) и белков, известных как миелин. Миелин, который в совокупности можно назвать миелиновой оболочкой, защищает нервные волокна, действует как изолятор и увеличивает скорость передачи нервных сигналов.
Признаки и симптомы
Симптомы и прогрессирование болезни Канавана варьируется от случая к случаю. Расстройство обычно проявляется в возрасте 3-6 месяцев, и начальные симптомы обычно включают:
Пострадавшие дети могут быть безразличными (апатичными), вялыми или раздражительными. У некоторых больных возникает проблема с глотанием (дисфагия), что приводит к трудностям при кормлении.
У пострадавших детей наблюдаются задержки в достижении основных этапов развития (например, дети не могут сидеть или стоять без посторонней помощи), и большинство из них никогда самостоятельно не ходят. Прогрессирующая потеря способностей, требующих координации умственной и мышечной деятельности (психомоторная регрессия) и умственной отсталости, также становятся очевидными в младенчестве. Большинство пострадавших детей могут научиться улыбаться, смеяться, поднимать голову и социально взаимодействовать.
Дополнительные симптомы, затрагивающее больных, включают:
Атрофия зрительного нерва может привести к снижению зрительной реакции. В большинстве случаев слух не затрагивается, но потеря слуха возможна.
С возрастом у больных детей гипотония может в конечном итоге перерасти в спастичность, состояние, характеризующееся непроизвольными мышечными спазмами, приводящими к медленным, скованным движениям ног. У больных детей может наблюдаться децеребрационная ригидность (повышение тонуса мышц-разгибателей и относительное расслабление мышц-сгибателей) или паралич.
Болезнь Канавана в конечном итоге приводит к опасным для жизни осложнениям; однако тяжесть и прогрессирование заболевания варьируется. У некоторых больных опасные для жизни осложнения развиваются в младенчестве, у других — после подросткового возраста.
Причины
Болезнь Канавана вызвана нарушениями или изменениями (мутациями) гена аспартоацилазы (ASPA). Эта мутация наследуется как аутосомно-рецессивный признак. Генетические заболевания определяются комбинацией генов определенного признака, находящегося на хромосомах, полученных от отца и матери.
Рецессивные генетические нарушения возникают, когда человек наследует один и тот же аномальный ген по одному признаку от каждого родителя. Если человек получает один нормальный ген и один ген с болезнью, человек будет носителем заболевания, обычно бессимптомным. Риск того, что два родителя-носителя передадут оба дефектных гена и, следовательно, заведут больного ребенка, составляет 25% с каждой беременностью. Риск рождения ребенка-носителя как родители, составляет 50% с каждой беременностью. Риск унаследовать нормальные гены от обоих родителей и быть генетически здоровым для конкретно этой болезни составляет 25%. Риск одинаков для мужчин и женщин.
Дефектный ген, ответственный за болезнь Канавана, был сопоставлен с хромосомой 17 (17pter-p13). Хромосомы присутствуют в ядре клеток человека и несут его генетическую информацию. Клетки человеческого тела обычно имеют 46 хромосом. Пары человеческих хромосом пронумерованы от 1 до 22, а половые хромосомы обозначены X и Y. У мужчин есть одна Х и одна Y-хромосома, а у женщин две Х-хромосомы. Каждая хромосома имеет короткое плечо, обозначенное «p», и длинное плечо, обозначенное «q». Хромосомы далее подразделяются на множество полос, которые пронумерованы. Например, «хромосома 11p13» относится к полосе 13 на коротком плече хромосомы 11. Пронумерованные полосы указывают местоположение тысяч генов, присутствующих в каждой хромосоме.
ASPA содержит инструкции по разработке (кодированию) аспартоацилазы, фермента, расщепляющего (метаболизирующего) N-ацетил-L-аспарагиновую кислоту (NAA). NAA — это соединение, которое, по мнению исследователей, играет жизненно важную роль в поддержании белого вещества мозга. Дефицит или неактивная аспартоацилаза приводит к накоплению NAA в ткани мозга. Симптомы болезни Канавана являются результатом повреждения белого вещества из-за ненормально высокого уровня NAA.
Затронутые группы населения
Заболевание поражает мужчин и женщин в равных количествах. Затрагивает все этнические группы, но встречается с большей частотой у ашкеназских евреев. В этой группе населения, по оценкам, частота носителей болезни достигает 1 на 40-58 человек. Риск рождения больного ребенка у ашкеназских еврейских родителей, составляет от 1 на 6400 до 1 на 13456 человек. Частота носителей гена в других популяциях неизвестна, но, скорее всего, намного ниже. Общая заболеваемость болезнью Канавана среди населения в целом неизвестна.
Диагностика
Диагноз болезни Канавана может быть заподозрен у детей с характерными признаками расстройства (например, плохой контроль головы, макроцефалия и проч. признаки). Диагноз может быть подтвержден тщательной клинической оценкой, подробным анамнезом пациента и различными специализированными исследованиями. Такие исследования могут включать газовую хроматографию-масс-спектрометрию, устройство, обнаруживающую повышенные уровни NAA в моче. Повышенные уровни NAA также могут быть обнаружены в крови и спинномозговой жидкости (СМЖ).
Исследование определенных клеток соединительной ткани кожи (культивируемых фибробластов) также может выявить дефицит фермента аспартоацилазы. Аспартоацилазная активность также отсутствует в лейкоцитах.
Пренатальная диагностика заболевания доступна через амниоцентез путем измерения уровня NAA в жидкости, окружающей развивающийся плод (амниотическая жидкость) на 16-18 неделе беременности. Если у обоих родителей известны мутации гена ASPA, то доступна пренатальная диагностика с помощью отбора образцов ворсин хориона, при котором образцы плацентарных клеток удаляются на 10-12 недели беременности для выявления мутаций.
Схожие по симптомам расстройства
Симптомы следующих расстройств могут быть похожи на симптомы болезни Канавана. Сравнения могут быть полезны для дифференциальной диагностики.
Лечение болезни Канавана
Лечение болезни Канавана направлено на конкретные симптомы, проявляющиеся у каждого больного. Поддерживающая терапия может облегчить некоторый дискомфорт. Физическая терапия и раннее вмешательство помогут улучшить осанку и коммуникативные навыки, соответственно. Если возникают проблемы с глотанием, для обеспечения правильного питания и увлажнения помогут питательные трубки. Эпилепсию лечат противоэпилептическими (противосудорожными) препаратами.
Прогноз
Прогноз при болезни Канавана плохой. Ожидаемая продолжительность жизни переменная. Некоторые дети умирают в первые несколько лет жизни, в то время как другие могут дожить до 10 лет, хотя некоторые больные доживают и до 20 лет. Прогноз часто зависит от клинического течения болезни, а также от уровня оказываемой медицинской помощи.
Высшее образование (Кардиология). Врач-кардиолог, терапевт, врач функциональной диагностики. Хорошо разбираюсь в диагностике и терапии заболеваний дыхательной системы, желудочно-кишечного тракта и сердечно-сосудистой системы. Закончила академию (очно), за плечами большой опыт работ.
Специальность: Кардиолог, Терапевт, Врач функциональной диагностики.